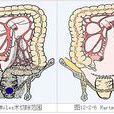
手術簡介
Miles手術作為直腸下段癌和
肛管癌的
根治性手術,普遍套用於臨床。切除範圍廣、功能性損壞大及永久性腸造口等因素,對病人術後的某些正常功能——如排便功能、排尿功能、性功能等影響較大;手術併發症和術後腸造口所出現的問題嚴重影響了病人術後的生活和生存質量。正確的
圍手術期處理手術前準確估計病變範圍和手術切除範圍,術中正確和安全地操作及術後正確處理腸造口,是減少對病人正常功能的影響、提高病人術後生活和生存質量的關鍵。
適應症
1.全身一般狀態較好,重要臟器功能可耐受手術者。
3.進展期直腸癌,浸潤型瀰漫性生長、
黏液腺癌或年輕病人,無遠隔臟器轉移者。
4.進展期直腸癌,雖為限局型、分化型癌,但
淋巴結已有明顯轉移,或癌周有明顯浸潤者,亦應行本手術。
5.進展期直腸癌,限局型,但位於直腸下段(肛緣6厘米以內),施行根治手術,切除癌腫
遠側腸管和周圍組織,切除必須包括
肛提肌時。
圍術期處理
1) 該手術範圍比較大,對病人的全身干擾也較大,尤其是年老者及合併有其他系統、器官疾 病者,術後發生合併症的機會就相對較多,因此,術後應對病人作全面的監護。如
BP、P、R、T等。
2) 對合併有心肺功能障礙及明顯貧血者,術後第一日應間斷
吸氧。
3) 全麻患者在醒後可改為頭高位,
硬膜外麻醉患者於術後6h後可改為半坐位,以利腹腔及腹膜後間隙的滲出物及時排入盆腔及骶前腔,以減少
腹腔感染的機會。
4) 術後3日內應給予甲氰米胍或
雷尼替丁800mg/日,或絡賽克2.0g/日,預防
應激性潰瘍的發生。
5) 術後應注意雙下肢有否
靜脈血栓形成,有否
淋巴回流障礙發生,如出現,則給予相應處理,如下肢抬高、溶栓製劑等。
6) 術後應持續
胃腸減壓,直至造瘺口中有糞便或氣體排出後一天,再拔出
胃管為宜。待
腸鳴音恢復較完全時,先抽淨胃內容物後,向胃管內注入生豆油100~150g並在30min後,在
足三里穴位以
新斯的明1mg作穴位封閉,待自造瘺口排出生豆油後拔除胃管。次日起可進流食,以後可逐漸增加進食。
7) 術後應足量補液,進食後逐漸減量,以保持
水電解質的平衡及保持能量供應。
9) 術後應注意加強留置導尿的護理。Miles手術由於進行了擴大
淋巴結清除,盆腔
植物神經的損傷,術後排尿功能多有障礙,因此術後留置尿管的護理至關重要。
(2)術後第二天起即可以試驗關閉
導尿管,每日3~4h開放一次,待有尿意後,可按時開放。
(3)術後一周左右起每日實行
膀胱沖洗,如果用雙腔或三腔導尿管,可持續點滴沖洗。
(4)可根據尿意情況及殘餘尿量情況,於一周左右拔出導尿管。
(5)拔出尿管後如仍不能自行排尿或
排尿困難,可用針灸方法,以刺激
膀胱肌的收縮,加速膀胱功能的恢復。
(6)留置導尿期間,進食後可投以尿路消炎劑,如
奧復星等。
(7)如二周后仍不能自行排尿者,可每周更換新的導尿管一次。
10) 術後應嚴密觀察造瘺口的情況:注意有無血運障礙。有極個別病例,於根部結紮腸系膜下動脈,而脾曲的
血管吻合弓不健全者,發生了造瘺口的血運障礙。因此術後第一日必須檢查造瘺口的血運情況,如有障礙,立即重新造瘺。待排氣排便後,注意儘量減少糞便污染周圍,如污染嚴重可造成造瘺口與皮膚間縫線的脫落,使造瘺口回縮,輕微或部分回縮者,可每日數次換藥,待周圍形成肉芽組織後,二期部分縫合,或自行癒合。此種情況,造瘺口往往較低,有的甚至低於皮膚,患者感到不方便,難以護理者也必須重新造瘺。如術後造瘺口癒合正常,可於一周后適當擴口,以防狹窄(但由於目前均採用外翻造瘺的方法,多無漿膜炎,很少有狹窄發生)。
11) 會陰部創面的處理:因該手術骶前創面過大,術後必須注意創面出血情況。如填塞的大油紗中含血量過大,血壓下降,說明骶前創面中可能有新鮮出血,此時應拔出紗布,進行止血。
手術方式
(一)體位:本手術須經腹部及會陰部兩處進行,所以應取
膀胱截石位,同時麻醉後將手術台搖成頭低足高位,使手術台與水平面大約成15°角左右,這樣有利於腹腔內的小腸移向上腹部,能很好的顯露下腹腔及盆腔,有利於操作。截石位時的軀體與大腿之間、大小腿之間的角度均應擺在舒適的功能位置上,以防止損傷
髖關節及膝關節周圍的韌帶及損傷腓總神經。
(二)消毒:消毒應包括腹部及會陰部兩部分,腹部上至乳頭水平,會陰部直達大腿的上2/3。以
碘酊、
酒精消毒、或以絡和碘、
洗必泰均可,陰囊最好用
新潔爾滅消毒,女性患者應進行陰道消毒。然後鋪足夠厚度的無菌單。
(三)切口:以選擇腹部正中切口最方便,同時有利於兩側淋巴結的清除。術者應站在患者的左側,切口自
恥骨聯合向上,左側或右側繞臍直達其上10cm左右。本人的體會是以左側繞臍較為方便,有利於左側
結腸的游離。因造瘺口的位置低於臍,不會增加污染機會。
(四)切開腹壁:在上述選定的切口處,切開皮膚、
皮下脂肪、
腹白線,向下切開
錐狀肌,直達恥骨聯合。然後採用透光照射的方法切開
腹膜前脂肪及腹膜,向下推開
膀胱,以免損傷。同時腹膜切開儘量在中線,這樣有利於關腹。如果想一側推開膀胱,偏向另一方切開腹膜,則給關腹時縫合腹膜增加一些困難。
(五)腹腔及盆腔檢查:開腹後應注意有無
腹水,依次檢查肝臟有無轉移以及轉移的程度,仔細檢查全部腹膜有無播種結節,檢查
大網膜上有無轉移結節,再依次檢查上腹部的胰腺、脾、胃等以及雙腎,再沿
腹主動脈及
腸系膜下動脈走行探查上方及側方
淋巴結有無腫大,以及植物神經有否受浸潤,髂血管有無受浸潤等,最後探查原發病灶,主要確定病灶的位置是否已侵犯周圍的組織以及與其他器官和骶前筋膜的關係,然後再根據術前檢查綜合判斷採用根治性術式的切除範圍。
(六)腹腔無瘤技術:探查結束後,開始手術前,首先以大塊紗墊將所有小腸推向上腹腔、使之與術區隔離。再以紗布帶在腫瘤的上方結紮直腸上部,以防止腸腔內的脫落癌細胞沿腸壁向上移動,這樣以紗布帶結紮後提起直腸也有利於操作。找到
腸系膜下靜脈向其中注入
5-Fu 250mg,向紗布帶以下的直腸腔內注射5-Fu 250mg。
(七)游離
乙狀結腸及直腸上段系膜及清除
淋巴結:助手將乙狀結腸提向右側,此時常常可見
乙狀結腸系膜與側盆壁(腹壁)之間生理性粘連,逐一分離之。然後在乙狀結腸系膜左側的最低部剪開一小孔,以
血管鉗提起後,如無嚴重浸潤,
腹膜即與後面的組織分開,用長剪刀在腹膜下作
鈍性分離出一隧道後擴大腹膜開口。向下直達腹膜返折處後,再向前轉折,剪開直腸
膀胱(或直腸
子宮)凹表面的腹膜。接著游離松解腹膜後的
結締組織,並找到左側
輸尿管,以紗布帶提起,同時游離出左
精索動靜脈,以免損傷。將乙狀結腸翻向左側,在
腹主動脈的前面剪開
乙狀結腸系膜的右側葉,同樣以剪刀先作鈍性分離後,剪開或是以剪刀切開右側葉,向上達
腸系膜下動脈根部,向下直達右側腹膜返折處,並與在左側腹膜的剪開處會合。在
下腔靜脈的右側緣處找出右輸尿管,以紗布帶提起,以免損傷。當游離開了
乙狀結腸左、右側系膜後,在腸系膜下動脈與腹主動脈的夾角中,術者以左手的食指及中指從右側向左側深入,將腸系膜下動脈牽直,助手將乙狀結腸展平。此時術者以左手仔細觸摸,判定腸系膜下動脈的走行及其分支的走行,並確定其自腹主動脈發出處,剪開腹主動脈前
結締組織,直達腹主動脈的
固有膜,顯露出腸系膜下動脈根部,將其周圍的結締組織全部清除,自根部向下,以左手引導扶持,清除沿該動脈走行的結締組織並清除顯露出
乙狀結腸諸分支及直腸上動脈,在終末支乙狀
結腸動脈分出的下方結紮切斷直腸上動脈;也可以在
腸系膜下動脈根部2 cm處結紮切斷。自腸系膜下動脈根部高度,在其左側約2cm處可找到
腸系膜下靜脈清除其周圍的結締組織,在與腸系膜下動脈相同的高度結紮切斷之。分離切除左右髂總動脈前的脂肪
淋巴組織。
(八)游離直腸:按照全
直腸系膜切除術(total mesorectalexcision,TME)原則游離直腸.在直腸固有筋膜與盆壁
筋膜間隙內進行,勿損傷下腹下神經、盆
神經叢及骶前
靜脈叢。先分離其後部及側部,下達
尾骨尖及兩側提肛肌平面,再分離直腸前方至前列腺尖端平面。
1)前方的游離:
淋巴結清除結束後,以
血管鉗將盆底
腹膜最低點剪開處的前葉夾起,助手將前面的
膀胱或
子宮陰道用深部拉鉤向前上,此時可見到稍呈堅韌的膜狀組織,即為Denonvillies筋膜,在此筋膜的前方進行游離,即可見到
精囊腺與前列腺(
精囊距肛緣的高度約為5cm,前列腺上緣距肛緣高度約為4cm),向下沿此間隙進行游離,儘量達低位(因腹部游離越低,會陰部操作越容易),如無明顯浸潤,可達前列腺的下極,只要層次認準,很少有出血。
2)直腸後方的游離:清除淋巴結之後,在
腹主動脈分叉部的下方,仔細解剖出骶前筋膜,在骶前筋膜的壁層與髒層之間進行游離。以電刀或長剪刀自上而下在此間隙中游離,此時可以見到位於骶前筋膜深面的骶中動脈及骶前
靜脈叢,注意一定不要損傷骶前筋膜的壁層及髒層,否則易造成癌細胞的擴散及難以收拾的大量出血。如癌腫無明顯的浸潤,則骶前間隙僅為疏鬆的
結締組織,很容易分離,當達到第3
骶椎水平時,可見到比較堅韌、緻密的Waldeyer筋膜(在直腸後壁固有筋膜的第3
骶骨水平,與骶前筋膜之間連線著一膜狀的筋膜,稱之為Waldeyer筋膜,也稱骶骨直腸筋膜)同樣以長剪刀靠近骶前筋膜剪斷之,否則易損傷直腸壁。繼續向下游離直達
肛提肌處。後壁的游離一般不至於造成出血。
3)側壁的游離:沿後壁游離的邊緣向左右側延伸,沿
髂內動脈向下游離。當達
腹膜返折下約2cm處,髂內動脈與直腸側壁之間可見到稍堅韌的
結締組織,即直腸側韌帶,銳性剪斷之(靠近血管處),然後清除膀胱直腸間隙中的結締組織。同時於根部結紮切斷直腸中動脈。至此,直腸的游離結束。接著分兩組同時進行腹壁造設
人工肛門及會陰部的操作。
(九)會陰部的操作:會陰部操作之前,一定縫閉肛門。切口:會陰部切口不宜過小,其界限為:前為
會陰中點,後為
尾骨尖,兩側為坐骨節結。作一橢圓形切口,先以
手術刀切開皮膚,環行一周,然後術者與助手分別牽開皮膚的內緣與外緣,用電刀切開
皮下脂肪組織,直至顯露出
臀大肌前緣及肌纖維,兩側達坐骨結節,及會陰淺橫肌的後緣為界線,繼續向深層以
電刀清除
坐骨直腸凹中的脂肪組織,直達
肛提肌的下方。在坐骨直腸凹脂肪中的最深處有直腸下動脈自
髂內動脈延續而來,其走行方向為由外向內,於根部切斷結紮之。切斷肛提肌:先在直腸與尾骨之間,切斷
肛管尾骨韌帶,然後逐漸向兩側沿骨盆的側壁,在肛提肌的止點處,依次切斷肛提肌中的
髂骨尾骨肌、
恥骨尾骨肌及
恥骨直腸肌。至此,會陰部操作中的後面及兩側的創面均可與腹腔中游離的創面相通。此時可將
乙狀結腸的斷端及要切除的肛管自直腸後壁相通了的孔道翻出至肛門外。以左手用力前拉提出的肛管,並以拇指及食指將前壁剩餘的相連部分組織夾住,從前壁切開的創面中仔細解剖出前列腺包膜(女性為陰道後壁)與Denonvilliers筋膜之間的界限,自外向內仔細游離,可用
電刀進行。逐步向內進行,直達
會陰體部,先於
會陰淺橫肌後方切斷
肛門外括約肌淺部的交叉纖維,向深進行達會陰深橫肌及
恥骨直腸肌,沿會陰深橫肌的後緣切斷恥骨直腸肌。此時可根據觸摸下的
導尿管位置的位置,判定
尿道的正常位置,進行操作,以免損傷。切斷恥骨直腸肌後,可見到直腸尿道肌,其後方連線直腸
縱肌,前方連線
尿道膜部。判定正確位置後切斷。再向上切斷會陰三角韌帶,可與腹部創面相通,然後將標本移除。直腸前壁的腫瘤,常常使Denonvilliers筋膜與前列腺的包膜或女性的陰道後壁粘連甚至浸潤,此時行前壁游離時,常常造成前列腺包膜撕裂出血,或陰道後部外膜的出血,因該部的靜脈叢豐富,極易出血,所以,①游離時一定要找好層次,儘量從腹部進行游離,這樣層次可能會更清楚,儘量減少
會陰的游離;②一旦發生該部出血,應儘量縫合止血,單純結紮或電灼往往不確切,不易奏效;③如果腫瘤浸潤,可行前列腺或陰道後壁的部分切除,然後進行前列腺的縫合或陰道修補。
(十)腹壁造設
人工肛門:當在預定線處切斷
乙狀結腸後,會陰部操作開始的同時,腹部手術組即可進行人工肛門的造設。目前國內外均採用經
腹膜外一次性開放造瘺法。造口部位的選擇:常選擇的造口的部位有二種,一種為臍與左側
髂前上棘連線的中外1/3,另一種為左
腹直肌外緣與髂前上棘與其連線交點的外上角處。首先在腹腔內在預定造瘺口的高度,提起乙狀結腸,剪開處的外側腹膜作潛行游離,上下約10cm左右,直繞過前
腹壁,大約達腹直肌中線水平。術者以左手深入潛行隧道中,作引導,然後在預定造瘺口處,消毒,助手以止血鉗提起,預定造口部的中點,半徑約2cm,作圓形切口,切開皮膚,在以電刀與該處腹壁相垂直切除一直徑為4cm的圓柱形脂肪,深達腹直肌前鞘或腹外斜
肌腱膜,長度與皮膚切除範圍相當。在十字型分開腹直肌或切開
腹外斜肌,顯露出
腹直肌後鞘,或
腹橫筋膜,將其十字切開,切開的長度要充分,但也不宜過大。不充分,會使腸道內容物通過受阻,過大也易造成切口旁疝。此時應不要損傷已游離的側
腹膜。用4把血管鉗子將腹直肌後鞘提起。經已游離的側腹膜外將擬行造瘺的
乙狀結腸拉出腹壁之外,拉出時要注意乙狀結腸不可扭曲,應使
乙狀結腸系膜對準
恥骨聯合。拉出腸管的斷端一般以高出皮膚2~3cm為宜。然後將乙狀結腸的相應高度先在深層與腹直肌後鞘作一圈縫合固定,注意勿損傷乙狀結腸的血管,影響造瘺腸管的血運。再將腸管的斷端與皮膚的真皮層作一周環形,外翻縫合,針距不宜過大,宜縫合12~16針為宜。另外,因作外翻時系膜緣外因系膜脂肪較多,不易外翻,因此縫合時,應儘量偏低,而其他部位稍高,這樣外翻後,造瘺口一周腸管高度一致。 縫合固定側
腹膜與拉出的
乙狀結腸,以封閉腸管外側的孔隙以免造成
內疝,先將剪開的乙狀結腸外側的側腹膜的上部斜行蓋於乙狀
結腸上,作間斷縫合固定,再將其下方的切緣與
乙狀結腸系膜縫合固定。注意蓋於乙狀結腸上面的腹膜一定要鬆弛,不可勒住了乙狀結腸,至此,
人工肛門造設結束。
(十一)關閉腹腔及會陰部創口:上述操作結束後,反覆沖洗腹腔,沖洗液自骶前創面中流出。最後再以含有5-Fu的鹽水沖洗,沖洗後檢查有無
出血點,一一結紮止血後,縫合剪開的後腹膜。閉合盆底腹膜時應注意:①針距不可過大,以不大於0.8cm為宜,否則極易造成
內疝;②宜提起兩側的
腹膜,在其邊緣縫合,如縫合過多時,一是易誤縫
輸尿管,二是縮小了腹腔而增大了骶前腔的容積,延遲骶前腔的癒合;③勿將盆底腹膜縫合成很尖的圓錐形,而儘量縫合成一比較圓滑的創面,否則小腸移至盆腔後易粘連成角造成梗阻。後腹膜縫合完後,清查腹腔並將全部小腸按順序置回原來的位置,再將
大網膜覆蓋其上,清點器械、敷料無誤後逐層關閉腹腔。同時
會陰組人員於骶前腔里放置膠管引流二枚,在一側或二側坐骨節結的內側另開口引出。最後封閉創口(可一層縫合,如果允許也可二層縫合)。固定
引流管,會陰創面如果過大,縫合時有張力,估計
一期癒合有困難時,也可以不置引流,不予以縫合,而以大塊
凡士林紗布敷貼創面後,以大紗布填塞,手術結束。術後2~3天,拔出大紗布,然後以1/5000的PP溶液反覆沖洗,
坐浴,待其自然癒合。
併發症
Miles術常見併發症有出血、感染、副損傷、
人工肛門併發症\
腸梗阻等。
優缺點
在治療上認為miles手術是中
低位直腸癌治療的金標準。該術式的腹部永久性
人工肛門經典術式為左下腹臍與
髂前上棘連線中外1/3處造瘺,
結腸末端脫出鉗夾外置活袖式外翻與皮膚縫合,形成蕈狀凸出,配帶糞袋。此術式有如下缺點:①人工肛門的位置不易掌握;②縫扎殘端腸管
邊緣動脈或造瘺口太緊導致吻合口壞死;③腸管游離不充分,張力過大,與腹壁縫合不牢,肥胖或術後嚴重腹脹等均可導致腸管回縮,若輕度回縮,可經換藥和
擴肛治癒,否則需手術重新造瘺。④人工肛門術後
水腫持續時間長;⑤排泄物、器具刺激易導致周圍皮膚炎症;⑥褲帶刺激突出的人工肛門,從而易感染。
研究進展
保肛手術
與Miles手術比較,具有操作簡單、手術時間短等優點,更重要的是避免了永久性人造肛門給患者帶來的精神及肉體上的雙重痛苦,且避免
人工肛門的許多併發症, 提高生存質量。保肛術包括局部切除術、直腸癌拖出吻合術、各種拉出式直腸切除術、會陰部造瘺術等。如果腫瘤基底距肛門6 cm,可行超低位雙吻合技術保肛術;腫瘤基底距肛門5 cm,可予改良Bacon術(
結腸經肛門拉出術)、Parks術(結腸
肛管吻合術)等;不管何種術式,必須保證近切緣(OW)、遠切緣(AW)、外科切緣(EW)無癌細胞殘留;保留肛門完整結構的內外
括約肌,齒線上1 cm黏膜及支配他們的血管和神經。但是如果不切實際的一味追求保肛,則會導致患者術後肛門墜脹感明顯、
大便失禁、
排便困難、疼痛劇烈等併發症,不僅沒有提高生活質量,反而讓患者痛不欲生、生不如死。目前,下段直腸癌保肛一直是國內外爭論的焦點。目前認為認為保肛治療適應證應根據癌腫病期、大小、浸潤深度、病理類型、距
齒線距離等情況決定:①腫瘤距
齒狀線不少於2 cm;直徑<3 cm,或小於腸周徑的1/2,可被推動,癌周組織無浸潤;②中、高分化癌;③術中病理排除癌細胞殘留;④已有遠處轉移,預期生存期較短的病人,如具備保肛的局部條件且腫瘤已引起梗阻必須手術時;⑤高、
中分化腺癌大於腸周徑的1/2但≤3/4周,且距齒狀線4 cm以上;
低分化腺癌、
黏液腺癌,未浸透深肌層,環周度≤1/2周且距齒狀線6 cm以上;⑥近
肛管部, 但患者堅決拒絕Miles手術者。總之,保肛手術應該把腫瘤的根治放在第一位,在不降低根治原則的前提下最大限度的提高保肛機率,同時保留的肛門具有完整的感覺、控制功能;嚴格掌握保肛手術治療直腸癌的適應證是預防併發症和減少復發的關鍵。
直腸癌的全系膜切除
直腸在胚胎期有其系膜,發育完成後系膜成為直腸周圍脂肪組織,它們借疏鬆筋膜與周圍器官相隔,直腸癌的大部分局部浸潤局限於此
脂肪組織內,由
盆筋膜髒層包繞直腸後方及側方的的血管、淋巴、脂肪組織,稱為
直腸系膜,在明視下將直腸“系膜”和直腸一併
銳性分離,這就是所謂的全系膜切除(Total Mesorectal Exicision,TME)。由於直腸癌在還沒有區域或局部淋巴轉移的情況下,直腸系膜中已存在癌細胞巢或癌結節;而這種系膜中的癌細胞播撒,不論是腹
會陰切除術、保肛手術或擴大根治術,癌細胞都會遺留或種在手術野中,所以以往的直腸癌術後局部復發居高不下。而TME切除了存在於人
直腸系膜中的腫瘤結節,這種結節可以存在於腫瘤上、下5 cm範圍,超過腫瘤向上下沿腸管侵犯的距離;切除保持完整的直腸系膜,避免撕裂包繞直腸的
盆筋膜髒層,減少腫瘤的術中播散,保證了根治手術的質量,使局部復發率下降到前所未有的水平 。有報告稱採用TME後直腸癌的局部復發率可降到5%左右。另外TME操作不但保證了手術的根治性,也提高了手術的成功率,更使手術時自主神經的顯露十分清晰,為進一步改善術後
膀胱生殖功能提供了解剖學基礎、創造了條件,從而使患者手術後的生活質量包括排便控制功能和泌尿生殖功能兩方面都有了明顯的提高。TME的手術操作不但降低了手術後的局部復發率,由於在正常解剖層次中操作,手術的創傷減小了,手術變得容易,手術時間縮短,術後恢復更快,實際上體現了微創的概念,這正是TME的重大意義之所在。
腹腔鏡技術
1991年腹腔鏡被套用於大腸外科,腹腔鏡下直腸癌切除主要適用於尚局限於腸壁、無周圍組織、臟器侵犯的直腸上段癌;對已明確病變已無法切除的晚期
大腸癌也可以通過腹腔鏡進行
結腸造口以解除梗阻。因腹腔鏡下直腸癌切除術被認為能減少術中出血,降低術後疼痛及有利於腸功能的恢復而得到了廣泛的認同;但同時由於存在腫瘤切除的徹底性、轉移、復發等問題,尚存在較多爭議。
腫瘤根治手術可以通過微創手術來完成,無疑是一個新理念,而微創的最終目標同樣著眼於提高療效,包括延長壽命和改善生活質量。
微創外科是現代醫學發展的一個重要方向,腹腔鏡技術在大腸癌外科中雖取得了許多令人鼓舞的成果,但其廣泛套用尚需大宗長期臨床隨訪資料的支持。
經肛門內鏡下局部切除(transanal endoscopic microsurgery,TEM)
TEM是近年發展起來的一種直腸癌局部切除新方法,是經過
肛門鏡,採用與手術腹腔鏡類似的方法將直腸局部的腫瘤作局部的擴大切除。通過這種技術手術者可以完成直腸壁的全層切除,其手術適應證是T1N0M0的患者。由於對手術技術和設備要求高,價格昂貴,在我國還很少開展此類手術。
直腸癌手術方式發生革命性變化,TEM被廣泛採用。Miles術長期被當作直腸癌外科治療的“金標準”, 考慮其破壞性及對排尿和性功能的影響,將其當作“金標準”是不恰當的 。如今TEM日益成為直腸癌外科治療新的“金標準”。