惠妥滋與其他抗病毒藥物聯合使用,去羥肌苷分散片用於治療I型HIV感染。主要毒性是胰腺炎和外周神經病。腹瀉,神經損害,寒顫/發熱,紅斑/瘙癢,腹痛,乏力,頭痛,疼痛,噁心、嘔吐,抑鬱,高脂血症。本藥慎與四環素,含鎂或鋁的抗酸藥合用。若藥物的吸收受胃酸度的影響(例如酮康唑,氨苯碸),則應在本品之前至少2hr服用。
基本介紹
- 中文名:惠妥滋
- 外文名:Didanosine Dispersible Buffered Tablets
- 商品名稱:惠妥滋
- 通用名:去羥肌苷分散片
簡介,藥理作用,藥代動力學,簡介,成人,分布,消除,兒童,兒童的分布,兒童的消除,代謝,微生物學,適應症,用法用量,成人,兒童,孕婦及哺乳期婦女用藥,不良反應,用藥禁忌,注意事項,成人劑量,胰腺炎,外周神經病變,肝功能衰竭,視網膜色素沉著和視覺改變,對妊娠及哺乳的影響,哺乳期母親,過量處理,相互作用,簡介,別嘌呤醇,更昔洛韋,喹諾酮類抗生素,與其他抗病毒藥物的相互作用,
簡介
通用名:去羥肌苷分散片
商品名稱:惠妥滋 惠妥滋
惠妥滋
 惠妥滋
惠妥滋英文名:Didanosine Dispersible Buffered Tablets
漢語拼音:HUituozi
主要成分:去羥肌苷
分子式:C10H12N4O3
分子量:236.2
藥理作用
本藥為可分散緩衝片。去羥肌苷是白色結晶粉末,分子式為C10H12N4O3,分子量為236.2。去羥肌苷在25℃和pH約為6時的溶解度為27.3mg/mL,在酸性溶液中不穩定,在pH<3和37℃時,10%的去羥肌苷在2分鐘內分解為次黃嘌呤。本藥的緩衝劑為碳酸鈣和氫氧化鎂,此外尚含無活性成分天門冬醯胺、山梨酸,微晶纖維素等。去羥肌苷為一種合成的嘌呤核苷類似物,具有抗人類免疫缺陷病毒(HIV)的活性。去羥肌苷是一種脫氧核苷類似物,(在人類原細胞培養及已建立的細胞系中,抑制離體試驗的HIV的複製)。去羥肌苷進入細胞後,被細胞轉化為抗病毒的活性代謝產物三磷酸雙脫氧核苷酸(ddATP)
。由離體細胞培養研究中得知,ddATP細胞內半衰期為8-24小時,脫氧核苷酸的共性(去羥肌苷類化合物)是缺乏3-自由羥基。在核酸複製時,一般都具有的核酸3-羥基,是隨後核酸5-單磷酸共價結合的受體,其存在是DNA鏈延長所必需的。ddATP缺乏3-位上的羥基,ddATP進入病毒DNA後,導致鏈的終止,從而抑制病毒複製。此外,ddATP進一步通過競爭性抑制三磷酸核苷與ddATP同功酶活性結合部位,干擾HLA-RBA依賴DNA多聚酶逆轉錄酶而抑制病毒。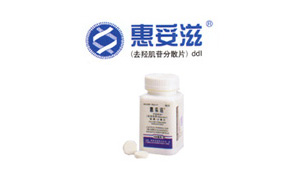 惠妥滋
惠妥滋
 惠妥滋
惠妥滋藥代動力學
簡介
吸收雙脫氧肌苷。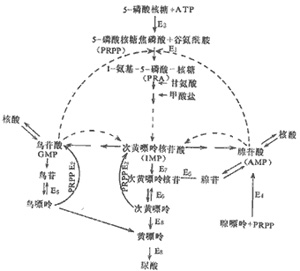 惠妥滋
惠妥滋
 惠妥滋
惠妥滋成人
69名愛滋病或嚴重的愛滋病相關綜合徵的成人病人參與藥代動力學的評估。這些病人的肌酐清除率>60m L/分,無肝功能損傷。病人接受60分鐘靜脈給藥,每天1-2次,共2周,每天總劑量範圍是0.8-33mg/kg。口服相當於靜脈給藥2倍的劑量,再給藥4周。口服劑型是凍乾粉末,其組成同本品兒科口服粉末一樣。成人的吸收和劑量呈線性關係,雖然病人間存在著很大的變異,在臨床給藥的劑量範圍,病人的血藥峰值和曲線下面積隨著劑量的增加也成比例地增加。若劑量小於等於7mg/kg,絕對生物利用率平均值在單次劑量給藥和給藥4周后分別是33%(±14)和37(±14%)。穩態的藥代動力學參數同最初靜脈給藥與口服藥所得的值無顯著差異。
分布
成人靜脈給藥後的平均分布容積是54±15L。在5例成人的研究中,靜滴本品後1小時,
本品在腦脊液中平均濃度為血漿的21%。 尿酸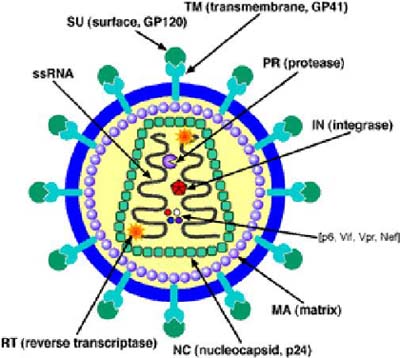 惠妥滋
惠妥滋
 惠妥滋
惠妥滋消除
成人口服給予本品後,平均的消除半衰期為1.5(±0.6)小時,總清除率均值大約是800(±200)mLl/分。去羥肌苷口服或靜脈給藥平均腎清除率大約是400(±160)mL/分。這表明除腎小球濾過外,還有腎小管主動分泌同去羥肌苷的清除有關。單劑量靜脈或口服給藥的平均腎重攝取率大約為55(±17)%和20(±8)%。無論靜脈或口服給藥均無蓄積作用。
兒童
在兩個兒科研究中,評估了去羥肌苷的藥代動力學。在一研究中,16個兒童和4個青少年接受了劑量範圍40-90mg/m2或倍數的單劑量的靜脈給藥。另一組口服80-180mg/m2的雙脫氧肌苷,一天兩次;在另一研究中,48個兒科病人接受單劑量靜脈給藥,然後加倍其劑量,一天三次,口服劑量範圍是20-180mg/m2。口服劑型是凍乾粉末,其組成同本品兒科口服粉末相同。兒童的吸收和劑量呈線性關係,雖然病人間存在顯著差異,兩組的血藥峰值和曲線下面積同劑量增加成正比,結果同成人相似。ACTG/
ST的絕對生物利用度是32(±12)%,第一次口服劑量和穩態血藥濃度是42(±18)%。NCI研究也表明,口服吸收去羥肌苷的個體差異大,其平均絕對生物利用度是19(±17)%。 惠妥滋
惠妥滋
 惠妥滋
惠妥滋兒童的分布
研究表明,靜脈給藥的分布容積平均是36.1(±12.8)L/m2,在這個研究中,從7個病人單劑量靜脈給藥或口服劑量後1.5-3.5小時收集到的腦脊液樣本中的去羥缺苷的濃度範圍為0.04-0.12μg/mL。這些CSF濃度相應於同時間的血漿濃度的12%-85%(平均46%)。
兒童的消除
研究還表明,平均消除半衰期在口服給藥後是0.8(±0.2)小時。在靜脈給藥後平均總清除率是535(±205)mL/分/m2。穩態時,靜脈或口服給藥後的平均腎清除率大約是240(±90)mL/分/m2。穩態時,腎的重吸收率是21(±11)%。口服給藥平均26天后,去羥肌苷無蓄積的證據。
 惠妥滋
惠妥滋代謝
去羥肌苷的代謝在人體未曾測定。將14C標記的去羥肌苷以單一靜脈注射或口服給於狗發現,去羥肌苷被大量代謝。口服給藥後,尿囊素即尿中的標誌代謝物,平均占所給的放射性標記量的61%。尿中檢出的三種嘌呤代謝產物是次黃嘌呤、黃嘌呤和尿酸。口服給予雄性和雌性大鼠14C標記的雙脫氧肌苷後,相似的代謝產物也同樣在大鼠血漿中發現。由糖苷分子鍵繼發於酶性或化學性水解後的雙脫氧核糖分子的代謝情況尚未被確定。基於動物研究的數據,可以推論在人體內雙脫氧肌苷的代謝過程同內源性嘌呤代謝途徑一致。推測此代謝產物具有去羥肌苷的抗病毒活性,在試管實驗中,半衰期為8-24小時。在細胞內ddATP的半衰期,細胞內ddATP在體內實驗的半衰期則尚未被測定。
微生物學
體外的HIV對去羥肌苷的敏感性同人體的HIV複製的抑制或臨床治療反應之間的關係尚未確定。體外試驗敏感性的變化很大,受以下因素的影響,依據病毒感染和雙脫氧肌苷治療之間的時機,所用的特殊培養及所採用的細胞類型與數量及做試驗的實驗室。此外,在臨床試驗中,目前所用方法的可靠性尚未確定。於體外試驗中,去羥肌苷顯示其抗病毒活性,在多種的HIV感染的T細胞,單核細胞/巨嗜細胞培養中,於T細胞中抑制50%病毒複製所需藥物濃度(ID50)為2.5-10uM(1uM=0.24μg/mL),單核細胞/巨嗜細胞ID50為0.01-0.1uM。在感染HIV-1的H9細胞,HIV-p24限制性蛋白為加入10uM雙脫氧肌苷阻斷,但感染了HIV-1(HTLV-IIIB)的ATH8細胞則需用>10uM才能完全起效。已報導用HT4-6C細胞嗜
菌體計數(合胞體)減少測試試驗,表明雙脫氧肌苷的ID50。對於HIV-1是2.1uM,對於HIV-2是5.6uM。用該分析系統測定的疊氮胸苷的ID50值依次為HIV-1是0.05uM,HIV-2是0.08uM。但是,培養的人MT-2感染細胞,雙脫氧肌苷的ID50報導值HIV-1為1uM,而HIV-2為10uM。而疊氮胸苷的ID50值分別為1.3uM和大於>100uM。從雙脫氧肌苷治療的病人中分離出的HIVJ顯示對雙脫氧肌苷的敏感性減低,雙脫氧肌苷的ID50增加2-3倍。但是,這些發現的臨床重要性還未被證實。而從總體的人群中分離的HIV對雙脫氧肌苷耐藥的情況尚不知道。 惠妥滋
惠妥滋
 惠妥滋
惠妥滋適應症
與其他抗病毒藥物聯合使用,去羥肌苷分散片用於治療I型HIV感染。START2是一個多中心、隨機、開放(open-label)研究,比較去羥肌苷分散片(200毫克,每天2次)/司坦夫定/茚地那韋和齊多夫定/拉米夫定/茚地那韋兩者在205例初治病人中的療效。通過48周的觀察,兩種方案在對HIVRNA水平的抑制和CD4細胞數目的增加方面效果相近。AI454-148也是隨機、開放、多中心的研究,它比較去羥肌苷分散片(400毫克,僅每日一次)加司坦夫定(40毫克,每日兩次)及奈非那韋(750毫克,每日三次),與齊多夫定(300毫克,每日兩次)加拉米夫定(150毫克,每日兩次)及奈非那韋(750毫克,每日三次),兩者在756例初治的病人中的治療效果,這些病人基線水平上CD4細胞計數的平均值是340個細胞/立方毫米(範圍是80-1568個細胞/立方毫米),血漿HIV-1RNA的平均值是4.69log10拷貝數/毫升(範圍是2.6-5.9log10拷貝數/毫升)。兩個治療組48周后,CD4細胞計數的平均值增加了188個細胞/立方毫米。在兩項隨機雙盲研究中(ACTG116A,1989-1992;ACTG116B/117,1989-1991),分別收集了617個和913個有HIV症狀或已接受治療一年以上的病例,比較了去羥肌苷(每日兩次)和齊多夫定(每日三次)的療效。結果表明,在初次接受治療的患者中(ACTG116A),兩者對HIV疾病的進展的作用相同
;接受去羥肌苷分散片治療患者的死亡率為26%,接受齊多夫定治療患者的死亡率為21%。先前接受過齊多夫定治療的患者(ACTG116B/117),去羥肌苷分散片治療患者的HIV疾病的進展和死亡率(32%)比齊多夫定治療組(41%)低。然而,兩組的存活率相同。另有一項兒童患者的隨機雙盲研究(ACTG152,1991-1995)。此項研究收集了831個患者。這些患者已接受了齊多夫定(180mg/m2,每6小時一次)、去羥肌苷(120mg/m2,每12小時一次)或齊多夫定(120mg/m2,每6小時一次)加用去羥肌苷(90mg/m2,每12小時一次)一年半以上治療。與齊多夫定單藥治療比較,去羥肌苷治療或去羥肌苷與齊多夫定合用的患者,其HIV疾病的進展和死亡率較低。研究證明,抗逆轉錄病毒藥物單藥治療的臨床有效性,包括去羥肌苷分散片在內,都具有時間限制性。兒科病人在使用去羥肌苷分散片方面有在成人和兒科病人中進行的充足的和嚴格的對照研究證據支持。在對HIV感染進展期病人的擴大研究項目中,65歲以上病人胰腺炎發生的頻率(10%)大於年輕病人(5%)。去羥肌苷臨床研究的65歲以上研究對象的數目不夠,尚不能判斷與年輕病人的反應相比有無差異。去羥肌苷基本上通過腎臟排泌,對於腎功能不全的病人毒性反應的危險性可能更大。由於老年病人常會有腎功能的減退,治療時應注意劑量的選擇。此外,應監測腎功能,隨時調整劑量。 惠妥滋
惠妥滋
 惠妥滋
惠妥滋用法用量
成人
起始薦劑量依賴於體重,如體重>60kg者,200mgbid或250mgbid。體重小於等於60kg者,125mgbid或167mgbid。劑量間隔應是12小時,所有規格的本品應在飯前至少30分鐘給藥。成人應每劑量服2片以便提供有足夠的緩衝液來阻止胃酸降解去羥肌苷。
兒童
推薦的劑量間隔是12小時。所有規格的本品應在飯前至少30分鐘給藥。根據兒童的體表面積推薦劑量,100-300mg/m2/天的兒童劑量目前正在進一步在對照臨床試驗評價之中。因為兒童最合適的本品劑量尚確立,一些研究人員建議將300mg/m2/天的劑量分為三天劑量。例如體表面積為1.1-1.4m2者,給予125mgbid;體表面積為0.8-1.0m2者,給予95mgbid;體表面積為0.5-0.7m2者,給予62mgbid;體表面積小於等於0.4m2者,給予31mgbid。
孕婦及哺乳期婦女用藥
本藥屬於妊娠B類。按臨床劑量形成的血漿濃度折算,12倍的去羥肌苷對大鼠的生育力和胎兒無影響;14.2倍的去羥肌苷對家兔的生育力和胎兒也無影響。12倍的去羥肌苷對雌性大及其幼仔在哺乳中期和晚期有輕度毒性。這些大鼠進食量和體重減少,而後代的體格和功能發育均不受影響。第二代無明顯變化。有實驗顯示,去羥肌苷能通過大鼠的胎盤轉運給胎鼠。對妊娠婦女尚未有充分核實的研究。動物生殖實驗並不能完全預測人類對藥物的反應。因此,妊娠期除非確實需要時,才應該使用本藥。為監控孕婦服用本藥及其它抗病毒藥物對胎兒的影響,醫生應對服藥的患者進行登記。美國疾病控制中心建議,為減少產後HIV的傳染,HIV感染的母親不要給新生兒哺乳。大鼠實驗發現,去羥肌苷及其代謝物可經乳汁分泌。目前還不知道去羥肌苷是否在人類的乳汁中分泌。
不良反應
本品的主要毒性是胰腺炎和外周神經病變。發生率大於等於5%不良反應有腹瀉、神經病變、寒顫/發熱、皮疹/瘙癢、腹痛、乏力、頭痛、噁心、嘔吐、感染、胰腺炎、肺炎、肉瘤、抑鬱、高脂血症。
用藥禁忌
對去羥肌苷和其他配方成分有明顯過敏的患者,禁用去羥肌苷分散片。
1.胰腺炎無論在未接受治療患者,還是曾接受治療患者,也無論免疫抑制的程度,單獨使用或者合用去羥肌苷分散片,均會產生致命或非致命的胰腺炎。若懷疑患者患有胰腺炎,應暫停使用去羥肌苷分散片。一旦確定有胰腺炎,應停止使用去羥肌苷分散片。合用司坦夫定的患者,無論是否同時合用羥基脲,發生胰腺炎的可能性均較大。為了維持生命,必須使用有胰腺毒性的藥物時,建議暫停使用去羥肌苷分散片。有胰腺炎危險因素的患者,儘量避免使用去羥肌苷分散片,一定需要使用時,需格外小心。HIV感染的晚期患者,其發生胰腺炎的可能性高,需密切觀察。腎功能損害的患者,若劑量不作調整也較容易發生胰腺炎。胰腺炎的發生率與劑量有關。在三期研究中發現,若劑量超過推薦劑量,其發生率為1%到10%,而採用推薦劑量時的發生率為1%到7%。小兒研究發現,首次劑量低於300mg/m2/日時,胰腺炎發生率為3%(2/60);高劑量時,發生率為13%(5/38)。兒童患者出現胰腺炎症狀或體徵時,應暫停使用去羥肌苷分散片。一旦確診有胰腺炎,應停止使用去羥肌苷分散片。
2.乳酸中毒和並有脂肪變性的重度肝腫大單獨使用核苷類藥物或者聯合用藥,包括去羥肌苷和其他抗病毒藥物,均會產生乳酸中毒和並有脂肪變性的肝腫大,甚至會引起死亡。這些情況多發生在女性。肥胖和長期的核苷攝入可能是引起上述情況的危險因素。若患者有患肝臟疾病的危險因素,使用去羥肌苷分散片需謹慎。因這些情況也發生在無危險因素的患者,所以用藥也需注意。臨床上或實驗室檢查一旦出現乳酸中毒或明顯的肝毒性(包括肝腫大和脂肪變性,轉氨酶可能不升高),去羥肌苷分散片治療應暫緩。
3.視網膜改變和視神經炎,在成人和兒童患者中,均有視網膜改變和視神經炎的發生。服用去羥肌苷分散片的患者應定期接受視網膜檢查。
注意事項
成人劑量
片劑應徹底咀嚼,用力壓碎或在服用前溶解在至少1盎司水中,攪拌直至完全混勻,立即飲用全部溶液。若需要另外調味,溶液可用1盎司的蘋果水稀釋,攪拌進一步稀釋的溶液後立即服用。加有蘋果汁的溶液在室溫62-73°F可穩定1小時。病人表現出視經損傷的症狀時,可以降低劑量,根據症狀決定是否停用本品。雖然沒有足夠的資料為中度腎損傷病人提供特別的劑量調整,腎衰需要透析的病人應考慮減少劑量,建議一次性給予每天劑量的1/4。雖然沒有足夠的資料為肝損傷病人提供特別的劑量調整,但這些病人應考慮調整劑量。
胰腺炎
胰腺炎是本品的主要臨床毒性,在有些病例是致命的。一旦接受本品治療的患者出現腹痛、噁心、嘔吐或生化指標升高時,應考慮胰腺炎的可能性。在這種情況下,應停用本品直至排除胰腺炎的診斷。如果需要使用已知有胰腺毒性的其他藥物(例如靜脈給予噴他脒治療時),應考慮停用本品。在一項本品的研究中,治療24位既往有胰腺炎患者,其中8例(30%)發生胰腺炎,因此,給予這類患者本品治療時應特別注意。具有胰腺炎高危因素的患者,諸如有胰腺炎病史,飲酒者,甘油三脂升高,或晚期的HIV感染患者,應予密切觀察。腎功能損傷者若在治療時劑量不作調整,則發生胰腺炎的危險性增加。兒科研究時,在最初劑量低於300mg/m2/天的60個患者中,有2位(3%)發生胰腺炎。高劑量治療組38位患者中有5位(13%)發生胰腺炎。這類兒科病人應停用本品直至排除胰腺炎的診斷。
外周神經病變
用本品治療的病人可發生外周神經病變。其發生率同用藥劑量相關。應監測患者是否發生神經病變,其特徵通常是肢端麻木、刺痛或手腳疼痛。在有神經病變的病史或曾接受有神經毒性的藥物治療的患者中,本品導致神經病變更為常見。這些患者在本品治療期間,出現神經病變的危險性可能增高。用本品治療的兒童患者中,神經病變極少見報導,但因在患兒中難以測定神經體徵和症狀,醫生應警惕此事件發生的可能性。
肝功能衰竭
在一項試驗中,將本品的兩個劑量同疊氮胸苷比較,3或4級肝功能實驗異常的一年發生率分別為本品高劑量組21%,本品推薦劑量組13%,疊氮胸苷組是1.3-9%,(高劑量本品同疊氮胸苷相比,P=0.05,本品推薦劑量同疊氮胸苷相比P=0.42)。在另一項試驗中,3或4級的肝功能異常在一年中的發生率分別是:本品高劑量組13%,推薦劑量組13%,而疊氮胸苷組為7%(高劑量組同疊氮胸苷組相比,P=0.15,而推薦劑量組同疊氮胸苷組相比,P=0.08)。病因未明的致死性肝功能衰竭在本品的1期研究是1/170,而在美國擴大研究項目中則為14/7806。在前一項試驗中,有3例患者出現無法解釋的肝功能衰竭。在後一項試驗中則無如此報導。極少收到有關於肝炎,包括暴發性肝炎的報告,這可作為不良反應監視之用。
視網膜色素沉著和視覺改變
有報導在接受本品等於或大於推薦劑量的兒童患者發生視網膜病變和視神經炎。視網膜色素沉著和視神經炎在成人已有報導。接受本品的兒童每6個月或發生視力改變時,應擴瞳檢查視網膜。對於使用本品的成年人患者,也應考慮進行定期的視網膜檢查。
對妊娠及哺乳的影響
懷孕分類B生殖研究已在大鼠和兔子身上進行,根據血漿水平所用劑量達到人所使用的劑量的12和14.2倍,沒有發現損傷生育和胎兒的證據。在大約12倍於人類的劑量時,雙脫氧肌苷對雌大鼠和幼鼠在哺乳中期和晚期有輕度毒性。這些大鼠表現納呆,增生的下降,但其後代的體格生長和功能發育沒有損傷,在F2代無主要變化。大鼠研究表明了雙脫氧肌苷和/或它的代謝產物是通過胎盤轉給胎兒的。對孕婦無足夠和很好對照的方法。因為動物的生殖研究不能完全預測人類的反應,此藥只能在明顯需要才可在懷孕期使用。
哺乳期母親
尚不知雙脫氧肌苷是否可通過人乳分泌。大鼠研究表明口服給藥後,雙脫氧肌苷和/或其代謝產物可分泌於哺乳期大鼠乳汁中。因許多藥物可分泌至人乳中,哺乳兒可能會受本品的不良影響,因此,服用本品(雙脫氧肌苷)的母親應停止哺乳。
過量處理
本品(去羥肌苷)過量尚無已知的解毒劑。在I期研究中,本品最初給予的劑量是目前推薦劑量的10倍,研究表明慢性長期過量的併發症有:胰腺炎,外周神經損傷,腹瀉,高尿酸血症或可能有肝功能損傷。雙脫氧肌苷不能通過腹膜透析清除,但可部分經血液透析清除。
相互作用
簡介
藥物相互作用研究表明,惠妥滋與daspone、洛哌丁胺、甲氧氯普胺、奈韋拉平、雷尼替丁、利福布汀、利托那韋、司坦夫定、磺胺加惡唑、甲氧苄啶和齊多夫定,在藥物代謝動力學上均無臨床的相互作用。其中,與daspone、奈韋拉平、利福布汀、利托那韋、司坦夫定和齊多夫定相互作用的研究是多劑量研究;與洛哌丁胺、甲氧氯普胺、雷尼替丁、磺胺加惡唑和甲氧苄啶是單劑量研究,其穩態動力學的影響不明。去羥肌苷分散片與已知對胰腺有毒性的藥物合用,會增加胰腺毒性,需格外謹慎,只有當無其他治療方案或必須使用時,方可採用此治療方案。有神經病變病史的和同時使用如司坦夫定有神經毒性藥物的患者,較易發生外周神經病變。
別嘌呤醇
在兩個腎功能減退的患者(肌酐清除率分別為15和18mL/min)單劑量200mg的去羥肌苷分散片與別嘌呤醇(300mg/日)同時使用,結果去羥肌苷的AUC增加了四倍。至於在腎功能正常的患者,別嘌呤醇對去羥肌苷藥物代謝動力學的影響不明。
抗酸藥物:服用去羥肌苷分散片,同時服用含鎂或鋁的抗酸藥物,兩者的抗酸成分會加重不良反應。吸收受胃中酸度影響的藥物:諸如酮康唑和伊曲康唑需至少在服用去羥肌苷分散片前兩小時服用。
更昔洛韋
在服用更昔洛韋前兩小時或同時服用去羥肌苷分散片,後者穩態AUC將增加至111(+14%)(n=12)。在服用更昔洛韋前兩小時服用去羥肌苷分散片,前者的穩態AUC減少21(±17%),而同時服用對更昔洛韋的AUC無影響(n=12)。
喹諾酮類抗生素
因抗酸成分如鎂、鈣和鋁會降低環丙沙星的血漿濃度,去羥肌苷分散片應在服用環丙沙星後2小時或前6小時服用。在8個HIV感染的患者中,當環丙沙星在服用市售的去羥肌苷分散片分散片兩小時前服用,環丙沙星的穩態AUC下降26%(95%可信限為14%,37%)。在12個健康受試者中,同時給予環丙沙星和去羥肌苷安慰劑,前者AUC下降15倍。有一個受試者在服用去羥肌苷安慰劑前服用環丙沙星,後者的AUC減少50%以上。抗酸成分如鎂、鈣和鋁會降低喹諾酮類抗生素的血漿濃度。若需服用去羥肌苷分散片,須參閱相應的喹諾酮包裝里的說明書,以決定兩藥使用的間隔時間。
