概述
消除反應 (e離去基團imination reaction) 又稱
脫去反應或
消去反應,是一種有機反應,一般為一
有機化合物分子和其他物質反應,失去部分原子或
官能團(稱為離去基)。反應後的分子會產生多鍵,為
不飽和有機化合物。消除反應分為下列兩種:
β消除反應:較常見,一般生成
烯類。
α消除反應:生成
卡賓類化合物。 離去基所接的碳為α碳,其上的氫為
α氫,而隔壁相鄰接的碳及氫則為β碳及β氫。化合物會失去β氫原子的稱為 β消除反應,會失去α氫原子的稱為α消除反應。
分類
消除反應按失去的兩個基團在分子中的相對位置進行分類,可分為以下三類:
 消除反應
消除反應(1)β-消除
β-消除又稱為1,2-消除,處於相鄰原子上的兩個基團失去後在這兩個原子之間生成π鍵(見
共價鍵)的反應。若相鄰的兩個原子都是碳原子,則會發生成烯消除反應。
(2)α-消除
α-消除又稱1,1-消除為同一原子上的兩個基團失去後該原子形成不帶電荷的低價結構(如卡賓或
氮烯)的反應。
(3)1,3-消除
1,3-消除為分別連在1,3-或更遠的相對位置上的兩個基團消除後得到環狀產物的反應。這些反應也可看為分子內取代反應。
反應速率
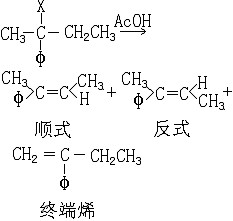 消除反應
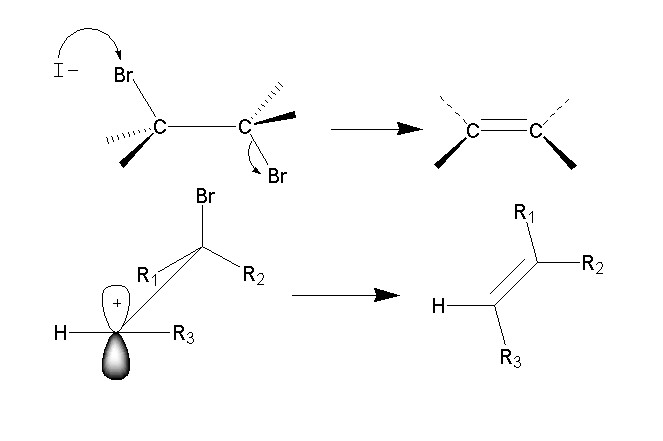
消除反應在離子型1,2-消除反應中,帶著成鍵電子對一起從反應物分子的1位或α位碳原子上斷裂下來的基團稱為
離去基團(離去基團),而另一個失去基團往往是連在2位或β碳原子上的氫,稱為β氫原子。例如,1-溴丁烷與氫氧化鉀在乙醇中共熱,溴帶著鍵合電子對斷裂下來成為溴離子,β氫原子以質子形式斷裂下來與鹼中和,同時在1和2位之間形成烯鍵。
這類消除反應的速率與鹵代烷結構有關,在相同條件下以三級鹵代烷最快,二級鹵代烷次之,一級鹵代烷最慢。由於鹼都是親核
試劑,以鹼為試劑的消除反應常伴有
親核取代反應,同時也可能發生
重排反應,三種反應之間的競爭與鹵代烷結構、試劑性能和反應條件等因素有關,強鹼和高溫有利於發生消除反應。
消除規則
霍夫曼消除
霍夫曼消除為四級銨鹼加熱分解生成烯烴的反應,主要得到雙鍵上取代基最少的取代乙烯。這是A.W.von霍夫曼於1881年提出的規律,稱為
霍夫曼規則。
熱消除反應
一般在氣相進行,是不需要酸或鹼催化的
單分子反應。反應物通過環狀
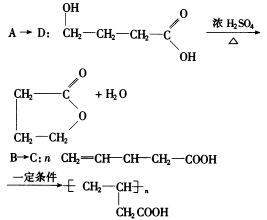
過渡態直接把β氫轉移到離去基團上,同時生成π鍵。羧酸酯加熱至約400℃,便發生熱消除。
黃原酸酯可在約200℃發生熱消除;三級胺
氧化物加熱至150℃左右也發生熱消除。
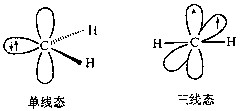 消除反應
消除反應扎伊采夫消除
二級和三級鹵代烷分別有二和三個β碳原子,如其結構不相同,雖有可能得到幾個不同的消除產物,但主要得到雙鍵上取代基最多的取代乙烯。這是Α.М.扎伊采夫於1875年總結出的規律,稱為
扎伊采夫規則。醇在酸性條件下加熱失水生成烯烴,也以得到扎伊采夫產物為主。
 消除反應
消除反應扎伊采夫規則:鹵代烷脫鹵化氫時,氫原子總是從含氫較少的β碳原子上脫去。也可表述為
鹵代烷脫鹵化氫時,主要生成雙鍵碳原子上含有較多取代基的
烯烴。
反應機理
在離子型反應中,按有關價鍵發生變化的先後順序不同,可分三種反應機理。
E1消除
單分子消除反應(E1) 反應物先電離,離去基團斷裂下來,同時生成一個
碳正離子,然後失去 β氫原子並生成π 鍵。反應分兩步進行,決定速率這一步(決速步)只有反應物分子參加。故
E1的速率與反應物的濃度成正比,與鹼的濃度無關。
E1CB消除
共軛鹼單分子消除反應(E1CB) 反應物先與鹼作用,失去β氫原子,生成反應物的共軛鹼
碳負離子,然後從這個碳負離子失去離去基團並生成π鍵。在生成π鍵的步驟中只有共軛鹼碳負離子參加。
E1CB也分兩步進行,
反應速率不僅與反應物濃度成正比,也與鹼的濃度有關,其關係較複雜,在多數情況下也成正比。一般說來,只有β碳原子上連有硝基、羰基或氰基等足以穩定碳負離子的強吸電子基團的反應物,才能按
E1CB機理進行反應。
E2消除
雙分子消除反應(E2) 反應一步完成,離去基團的斷裂、β氫原子與鹼中和、π 鍵的生成三者協同進行(見
協同反應),反應物和鹼同時參加反應。
E2的速率與反應物濃度和鹼濃度都成正比。上述三種機理以
E2最普遍,但並非所有
E2都完全協同。有些
E2中,β氫的斷裂稍先於離去基團的離去,情況在一定程度上與
E1CB相似,稱為“接近
E1CB的
E2”;另一些
E2的情況剛好相反,離去基團的離去稍先於β氫的斷裂,在一定程度上與
E1相似,稱為“接近
E1的
E2”。一般的
E1、“接近
E1的
E2”和典型的
E2等反應都以發生扎伊采夫消除為主,而
E1CB和“接近
E1CB的
E2”卻以發生霍夫曼消除為主。
總結
在
E1C和
E1CB中,反應均分兩步進行,各自的活性中間體碳正離子和碳負離子都具平面結構,一般不存在立體選擇性問題。但在
E2中,只有離去基團、α和β碳及β氫四者處於共平面的
空間位置,才有利於
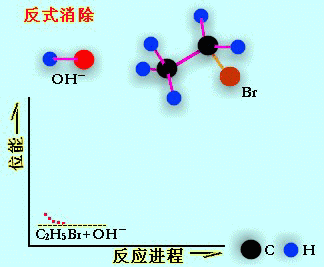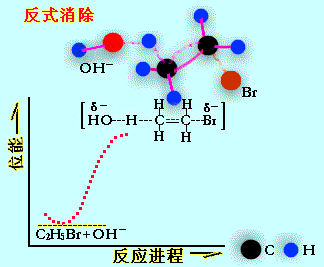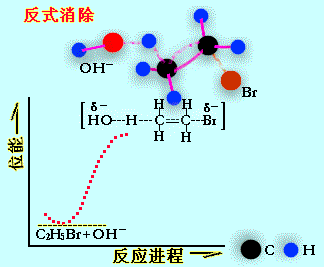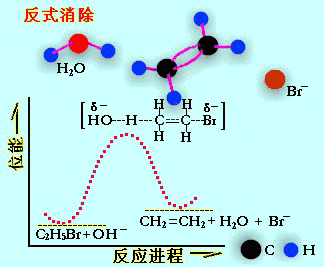
協同反應的進行,而符合這種要求的空間排列有兩種:離去基團和β氫在α、β碳同一邊時,發生順式消除;離去基團和β氫在α、β碳的兩邊時,發生反式消除。在大多數情況下,
E2為反式消除,但不排除順式消除的可能性,甚至有些
反應物由於結構的限制,只能發生順式消除。
有些反應物在 β碳原子上連有比氫更容易被
路易斯鹼(見
酸鹼理論)作用的基團或者根本沒有 β氫,它們就有可能發生不涉及失去 β氫的消除。連二鹵代烷在碘
離子或鋅的作用下發生的脫鹵反應和 α,α-二
烷基β-
鹵代酸的脫羧反應都屬於這種情況。

 消除反應
消除反應 消除反應
消除反應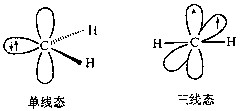 消除反應
消除反應 消除反應
消除反應