介紹
病因
臨床表現
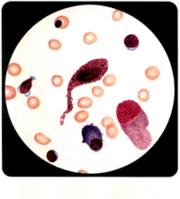 先天性再生障礙性貧血病理圖
先天性再生障礙性貧血病理圖 先天性再生障礙性貧血病理圖
先天性再生障礙性貧血病理圖介紹由於DBA頗為少見,其確切的發病率難以確定。歐洲回顧性研究表明DBA在≤15歲兒童中年發病率約為1.5/100萬~5.0/100萬。 先天性再生障礙性貧血發生於嬰幼兒,多數...
先天性純紅細胞再生障礙性貧血又名Diamond-Blackfan anemia(DBA),是以單純紅系再生障礙和先天性畸形為特徵的遺傳性疾病,是一種少見的先天性純紅細胞再生障礙性貧血...
再生障礙性貧血簡稱再障,是一組由多種病因所致的骨髓造血功能衰竭性綜合徵,以骨髓造血細胞增生減低和外周血全血細胞減少為特徵,臨床以貧血、出血和感染為主要表現。...
《兒童再生障礙性貧血》一片由青島大學醫學院製作,人民衛生出版社出版發行,是國家衛生部的醫學視聽教材,主要講述了兒童再生障礙性貧血的病理、病因、治療等內容,適合...
障礙性貧血分為先天性和獲得性,獲得性又分為原發性和繼發性,通常再生障礙性貧血指的是繼發性的。它的特徵有:造血幹細胞和造血微環境功能障礙,造血紅髓被脂肪...
再生障礙性貧血診斷標準一般為三低一高(即白細胞、紅細胞、血小板低;淋巴細胞高)。...... 再生障礙性貧血(aplastic anemia,AA,簡稱再障),再障分先天性和獲得性兩...
小兒純紅細胞再生障礙性貧血(PRCA)是僅有紅細胞系統的發育障礙,白細胞與血小板無改變。個別病例可在骨髓中表現為幼紅細胞系列成熟停頓於早期階段,出現原紅細胞小簇...
再生障礙性貧血(Aplastic anemia,AA)簡稱再障,是由多種原因引起的骨髓造血幹細胞缺陷、造血微環境損傷以及免疫機制改變,導致骨髓造血功能衰竭,出現以全血細胞減少為...
醫譯【醫】Acquired aplastic anemia概述獲得性再生障礙性貧血1(acquired aplastic anemia)是一種獲得性骨髓造血功能衰竭症。主要表現為骨髓造血功能低下,全血細胞減少...
再生障礙性貧血(簡稱再障):是由多種原因引起的骨髓造血功能衰竭的一組綜合病徵。一般表現為貧血、出血、感染、發熱(高燒或低燒),並伴有走路乏力,頭暈等症狀。血液...
單純紅細胞再生障礙性貧血(pure red cell aplasia)簡稱純紅再障;系骨髓紅細胞系列選擇性再生障礙所致一組少見的綜合徵。國內文獻報告已超過100例。發病機制多數與...
再生障礙性貧血(簡稱再障)是一組由於化學、物理、生物因素及不明原因所致的骨髓幹細胞或,及造血微環境損傷,以致紅髓向心性萎縮,被脂肪髓代替,血中全血細胞減少。...
純紅細胞再生障礙性貧血(純紅再障,PRCA)是指因骨髓中紅系細胞顯著減少或缺如所致的一種貧血。1922年Kaznelson首先將此病從再生障礙性貧血中分出,此後這種病漸漸...
再生障礙性貧血(簡稱再障)是由於生物、化學、物理等多種因素導致造血組織功能減退或衰竭而引起全血細胞(紅細胞計數、白細胞計數、血小板)減少,其臨床表現為貧血、出血...
單純紅細胞再生障礙性貧血系骨髓紅細胞系列選擇性再生障礙所致一組少見的綜合徵,簡稱“純紅再障”。可分為急性和慢性兩類。前者常發生於病毒感染、溶血性貧血或服用...
肝炎後再生障礙性貧血,簡稱肝炎後再障,是一種發生在急性或慢性肝炎後期,以外周全血細胞減少,骨髓三系細胞增生下降,臨床以貧血、出血及感染為特徵的疾病。本病好發...
貧血症是由於身體無法製造足夠的血紅蛋白(一種將氧氣輸送到血紅細胞和身體各個...造血不良貧血 核成熟障礙 骨髓造血功能減低 失血性貧血 急性失血性貧血 慢性失血...
先天性紅細胞生成異常性貧血(congenitaldyserythropoietic anemia 簡稱CDA)的特點是:①無效造血(紅細胞與幼紅細胞在骨髓內破壞);②骨髓中出現較多胞體較大的多核紅...
小兒先天性紅細胞生成異常性貧血疾病診斷 須與其他造血異常性貧血鑑別,如再生障礙性貧血、紅白血病、骨髓硬化症和核蛋白合成障礙包括維生素B12或葉酸缺乏。Ⅱ型的血清...
肝炎再生障礙性貧血綜合徵又稱肝炎並發再生障礙性貧血或肝炎後再生障礙性貧血,常為兒童和青年的肝炎致死性併發症。目前一般認為本病徵是一個獨立的疾病。...
肝炎再生障礙性貧血綜合徵又稱肝炎並發再生障礙性貧血或肝炎後再生障礙性貧血,常為兒童和青年的肝炎致死性併發症,目前一般認為本病徵是一個獨立的疾病。臨床有面色...
重型再障,是重型再生障礙性貧血的簡稱。重型再障起病急,進展迅速,常以出血和感染髮熱為首起及主要表現。病初貧血常不明顯,但隨著病程發展,呈進行性進展。幾乎均有...
屬於先天性再障,稱為Fanconi貧血(范可尼貧血),這類病人除有典型再障表現外,還...2. 骨髓象 與再生障礙性貧血相同。可有灶性增生,可出現巨幼樣幼紅細胞。骨髓...
