基本介紹
- 中文名:肽鍵
- 外文名:peptide bond
- 別名:醯胺鍵
- 化學式:-CO-NH-
- 作用:連結胺基酸
形成原理
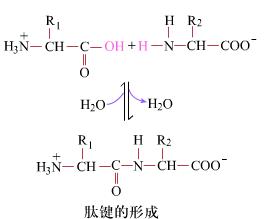 肽鍵的形成
肽鍵的形成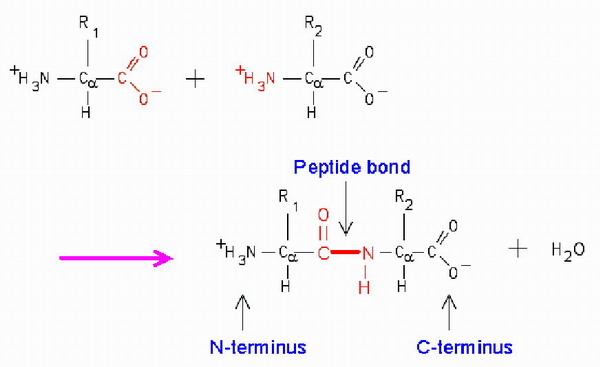
 肽鍵的形成
肽鍵的形成肽鍵是一分子胺基酸的α-羧基和一分子胺基酸的α-氨基脫水縮合形成的醯胺鍵,即-CO-NH-中第二個“-”代表的鍵。胺基酸借肽鍵聯結成多肽鏈。是蛋白質分子中的主要...
肽鍵一分子胺基酸的α-羧基和一分子胺基酸的α-氨基脫水縮合形成的醯胺鍵,即-CO-NH-。胺基酸借肽鍵聯結成多肽鏈。...
特殊的如:環二肽,可以存在兩個肽鍵。二肽是一大類物質的統稱,其不同,除構成胺基酸種類可不同外,結構也可不同,例如:環狀二肽稱為環二肽,鏈狀則稱二肽鏈。...
兩個胺基酸分子(可以相同,也可以不同),在酸或鹼存在的條件下加熱,通過一分子的氨基與另一分子的羧基間脫去一分子水,縮合形成肽鍵的化合物,稱為成肽反應。...
肽鍵(peptidebond)編輯 鎖定 本詞條缺少信息欄、名片圖,補充相關內容使詞條更完整,還能快速升級,趕緊來編輯吧!一個胺基酸的羧基與另一個胺基酸的氨基縮合,除去一...
一個胺基酸的氨基與另一個胺基酸的羧基可以縮合成肽,形成的醯胺基在蛋白質化學中稱為肽鍵。胺基酸的分子最小,蛋白質最大,兩個或以上的胺基酸脫水縮合形成若干個...
肽是兩個或兩個以上的胺基酸以肽鍵相連的化合物,在人體內起重要生理作用,發揮生理功能。具有活性的多肽稱為活性肽,又稱生物活性肽或生物活性多肽。中文...
肽單位(peptide unit)又稱為肽基(peptide group),肽鍵的所有四個原子和與之相連的兩個α-碳原子所組成的基團。是肽鍵主鏈上的重複結構。是由參與肽鏈形成的氮...
(4)外顯肽的連線 連線的兩個外顯肽的(硫)酯鍵自發進行的轉醯基反應,以更穩定的醯胺肽鍵取代(硫)酯鍵,將N端C端外顯肽用天然肽鍵連線起來。...
組成多肽的胺基酸在相互結合時,由於其部分基團參與了肽鍵的形成而失去一分子水,因此把多肽中的胺基酸單位稱為胺基酸殘基。即由肽鍵連結的胺基酸失水部分。...
醯胺鍵是一種帶負電性的官能團。在有機化學中,醯胺鍵是-CO-NH-,其中碳氧成雙鍵,氮氫成單鍵。肽鍵都是醯胺鍵,醯胺鍵包括肽鍵但不等同於肽鍵。醯胺鍵所指的...
肽鏈peptide chain,化學名詞;每兩個胺基酸相互連線形成一個肽鍵,多個胺基酸相互連線就形成了多個肽鍵,由多個胺基酸相互連線形成的含有多個肽鍵的一條鏈狀結構稱為...
由兩個胺基酸分子縮合而成的化合物,叫做二肽(含有一個肽鍵)。以此類推,由多個胺基酸分子縮合而成的,含有多個肽鍵的化合物叫做多肽。...
蛋白酶按水解底物的部位可分為內肽酶以及外肽酶,前者水解蛋白質中間部分的肽鍵,後者則自蛋白質的氨基或羧基末端逐步降解胺基酸殘基。...
雙縮脲試劑本是用來檢測雙縮脲,由於蛋白質分子中含有很多與雙縮脲結構相似的肽鍵,因此也能與銅離子在鹼性溶液中發生雙縮脲反應。當底物中含有肽鍵時(多肽),試液...
