重排及其主要形式
重排有兩大類,一類屬無規則重排,主要在經類中出現,這類重排用正常裂解規律無法解釋的另一類重排則是根據定規律進行的,它對於我們研充分子結構是非常有益這類重排的特徵是有兩個鍵發生斷裂,對OE
·+而言,在發生原子間的重排生成個新OE
·+的同時脫去箇中性分子。表現在質譜圖上的特點是:如果該OE
·+是不含氮或含偶數個氮的質量為偶數的離子,則生成的碎片離子一定是個偶數質量的離子反之。如果該OE
·+含奇數個氮的質量為奇數的離子,那么生成的碎片離子一定是具有偶數質量的。即:
母離子¬·+—→ 子離子¬·+ + 中性分子(重排)
因此,根據碎片離子與母離子質量奇偶數相同的關係,就能推測所發生的裂解是重排裂解解。並很容易將重排裂解與簡單裂解區分開來。
重排的主要幾種形式:
凡具有γ-H的醛、酮、羧酸、酯、烯烴、側鏈芳烴以及含硫羰基、雙鍵氮等的化合物,經過六元環空向排列的過渡狀態,γ-H重排轉移到電離的雙鍵碳或雜原子上,同時烯丙鍵(α-β鍵)斷裂生成一個不飽和的中性碎片及一OE·+ 。它是美國質譜學家麥克拉弗蒂(F.W.Mclafferty) 發現和提出的。我們可用下面的通式說明麥氏重排的機理。
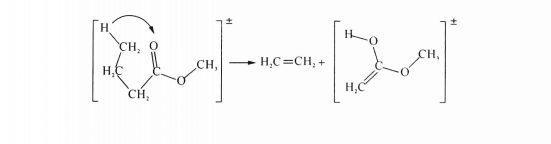 麥氏重排的機理
麥氏重排的機理麥氏重排的規律性很強,對解析質譜很有意義。由簡單裂解或重排產生的碎片離子,若能滿足麥氏重排條件(結構中有不飽和基團以及有γ-H),還能進一步引起麥氏重排。
(2)、逆Dies-Alder重排(RDA)
這種重排是由狄爾斯-阿爾德反應的逆向過程所造成的鍵斷裂而引起的重排。具有環己烯緯構(含有內雙鍵)類型的化合物可發生RDA裂解。結果一般都形成一個共軛二烯自由基正離子及一個烯烴中性碎片。
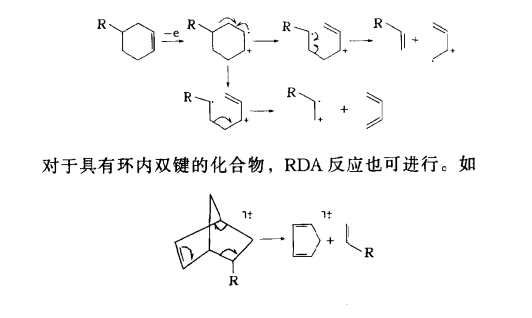 RDA 重排反應式
RDA 重排反應式但是不要認為正電荷定留在共軛二烯碎片上,有時也可能在烯烴碎片上或兩者兼有之,這就要看裂解過渡狀態所形成的正離子的穩定性了。過渡狀態的正離子越穩定,按這種過渡狀態裂解而產生的離子比例就越高。RDA裂解可能是自由基中心或電核中心誘發的。
(3)、非六元環重排
醇、鹵代烴、硫醇、醚及胺等可以經過環狀過渡態發生非六元環重排裂解。在重排過程中,氫原子與官能團結合,脫去一個中性小分子。這種氫原子的遷移沒有選擇性,某些芳香化合物及碎片離子也能發生這種重排。如
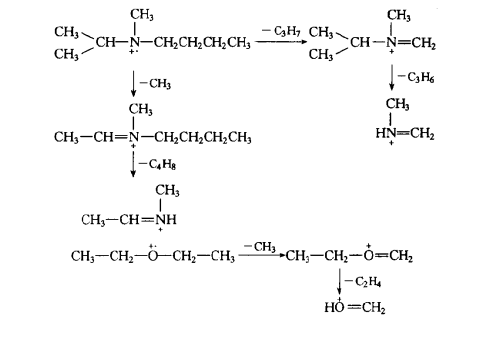 非六元環重排式例
非六元環重排式例重排離子的套用
重排方式很多,但有些重排南由於是無規律重排,其結果很難預測,稱為任意重排,這樣的重排對結構的測定無用處。多數重排是有規律的,它包括分子內
氫原子的遷移和鍵的兩次斷裂,生成穩定的重排離子。這種類型的重排對化合物結構的推測是很有用的。如麥氏重排、逆Diels—Alder重排、親核性重排等對預測化合物結構是非常有幫助的。
重排離子峰可以從離子的質量數與它相應的分子離子來識別。通常不發生重排的簡單裂解,質量為偶數的分子離子裂解得到質量為奇數的碎片離子;質量為奇數的分子裂解為偶數或奇數(與N原子的奇偶和是否存在於碎片中有關)的碎片離子。若觀察到不符合此規律(如質量為偶數的分子離子裂解得到質量為偶數的碎片離子),則可能發生了重排。
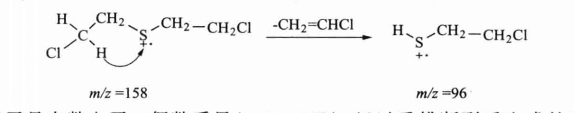 芥子氣分子重排式 左邊m/z=158 右邊m/z=96
芥子氣分子重排式 左邊m/z=158 右邊m/z=96芥子氣離子是奇數電子一偶數質量(m/z=158),經過重排斷裂後生成的碎片仍是奇數電子一偶數質量(m/z=96)。
相關拓展
碎片離子是由於離子源的能量過高,分子離子在離子源中碎裂而形成的如下表。碎片離子峰的信息有助於推斷分子結構。
鍵類型 | C—C | C—N | C—O | C—S | C—H | C—F | C—Cl | C—Br | C—I |
單鍵 | 345 | 304 | 359 | 272 | 409 | 485 | 338 | 284 | 213 |
雙建 | 607 | 615 | 748 | 535 | | | | | |
三鍵 | 835 | 889 | | | | | | | |
一般來說,強度最大的質譜峰對應最穩定的碎片離子。通過分析各種碎片離子峰的相對強度,通常能夠獲得整個分子的結構的信息。但是通過此方法獲得分子拼接結構不總是合理的,因為碎片離子並不只是通過分子離子一次碎裂而形成,可能會進一步碎裂或重排,因此要準確進行定性分析最好與標準圖譜進行比較。
對於只有一根化學鍵斷開的簡單斷裂(斷裂產物是原分子中已經存在的結構單元,沒有發生重排),有幾條經驗規則可以適用,但不是對所有化合物都適用,應謹慎適用。
(1)鍵能小的共價鍵先斷裂。
(2)碳鏈分支處易發生斷裂,分支越多,越容易斷裂。這是由於碳原子具有以下穩定順序:+CR3 > +CHR2 >+CH2R> +CH3。
(3)形成共軛效應更強體系的碎片,其斷裂幾率更大。
 麥氏重排的機理
麥氏重排的機理 RDA 重排反應式
RDA 重排反應式 非六元環重排式例
非六元環重排式例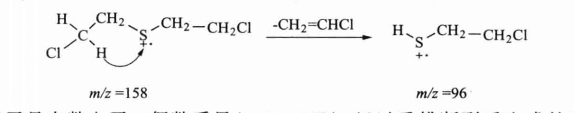 芥子氣分子重排式 左邊m/z=158 右邊m/z=96
芥子氣分子重排式 左邊m/z=158 右邊m/z=96