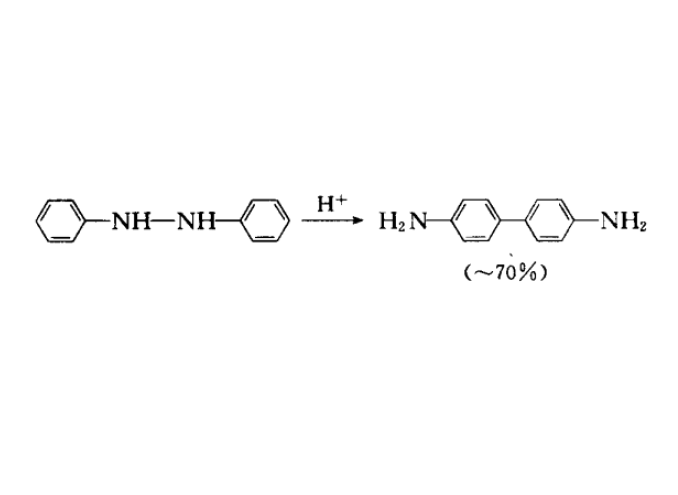
聯苯胺重排反應即氫化偶氮苯類經σ遷移反應重排為4,4'-二氨基聯苯的反應。重排在強酸存在下進行,4,4'-二氨基聯苯是主要產物。
基本介紹
- 中文名:Benzidine重排
- 別名:聯苯胺重排
- 機理:σ遷移反應重排
- 主要產物:4,4'-二氨基聯苯
- 領域:有機合成
簡介,反應特點,反應機理,反應舉例,
簡介
1862年,Hofmann在還原偶氮苯時得到了聯苯胺產物,即4,4'-二氨基聯苯( 對聯苯胺) ,發現了聯苯胺重排反應。從此,開始了對聯苯胺重排反應的機理和套用研究。在聯苯胺重排反應中,不僅可以生成主產物對聯苯胺,在某些條件下還可以得到鄰對聯苯胺、鄰聯苯胺、鄰半聯胺和對半聯胺。在Stille和Suzuki偶聯反應報導以前,聯苯胺重排和Ullmann反應是合成聯苯類化合物的重要方法,在合成上得到廣泛套用。
聯苯胺重排被發現至今已有150年歷史,在這150年間,對其重排反應機理研究一直沒有中斷過,先後提出了極性過渡態理論,π絡合物理論,雙自由基理論和陽離子自由基對理論,以及環質子化理論。但雙自由基和陽離子自由基對理論及環質子化理論由於都沒有強有力的和可接受的實驗信息支持,基本沒有生命力,在此不再做進一步的介紹。
直至20世紀80年代,Shine等通過同位素標記動力學實驗才證實了鄰聯苯胺和對聯苯胺的形成是通過[3,3]和[5,5]σ遷移反應實現的。但在聯苯胺重排反應中,副產物的形成機理至今仍困擾著有機化學家。在20世紀末就已經確證了鄰聯苯胺和對聯苯胺的形成是通過σ遷移反應實現的,並且國外的教科書也都以σ遷移反應來解釋聯苯胺重排反應的機理。
反應特點
反應也產生2,2'-和2,4'-二氨基聯苯。當對位有不易脫落的取代基時,也產生2-和4-氨基二苯胺。
反應產物和動力學受芳環上取代基的影響。
有些取代基(特別是受電子基)可脫落,容易程度從SO3H,СО2Н>RC(O),Cl>OR遞減。
N-叔醯胺RC(O)NR、仲氨基-NR2與烷基不脫落。
重排也可在惰性溶劑與80-130°C的無酸條件下發生(熱重排)。溶劑極性越強,重排也越快。不過熱重排的區域選擇性不如酸催化的重排。
芳環有一個對位被封閉時,重排得對半聯苯胺。兩個對位都被封閉,則得鄰半聯苯胺。
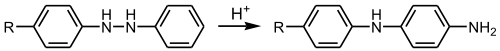 鄰半聯苯胺
鄰半聯苯胺反應機理
反應是分子內的,用不同的二芳肼進行反應,不得到交叉產物。機理中,首先兩個氮被質子化,後發生重排,得到的4,4'-二亞胺聯苯再去質子,得產物。
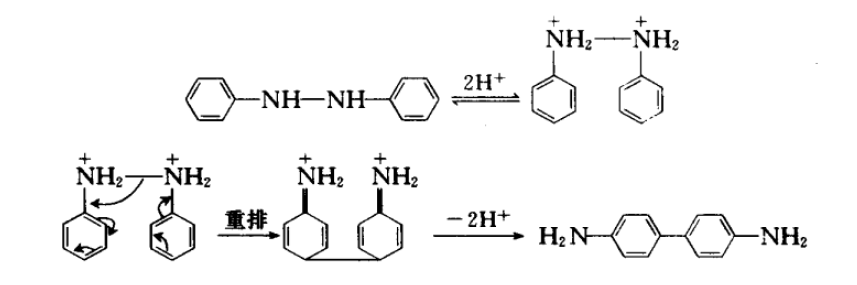 反應機理
反應機理反應舉例
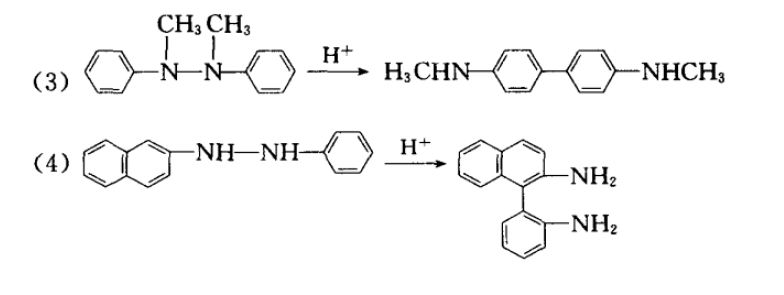 反應舉例
反應舉例