諾爾吡咯合成(Knorr吡咯合成)是一個常用的合成吡咯衍生物的有機反應,由德國化學家路德維希·諾爾(Ludwig Knorr)首先報導。肼或取代肼和1,3-二羰基化合物反應得到吡唑或吡唑酮的反應。此反應與Paal–Knorr 吡咯合成法類似。
基本介紹
- 中文名:Knorr吡咯合成
- 發現人:德維希·諾爾
- 產物:吡咯衍生物
- 領域:有機合成
反應特點
反應機理
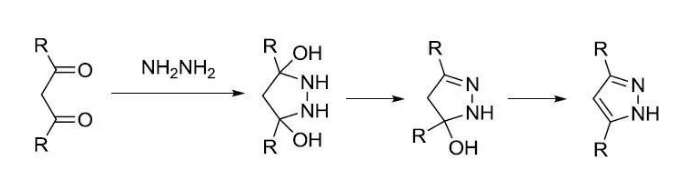 機理1
機理1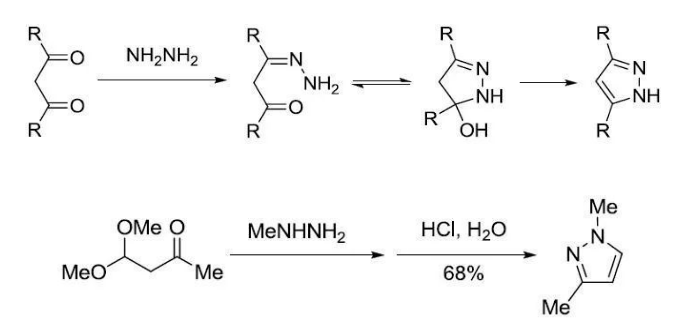 機理2
機理2反應舉例
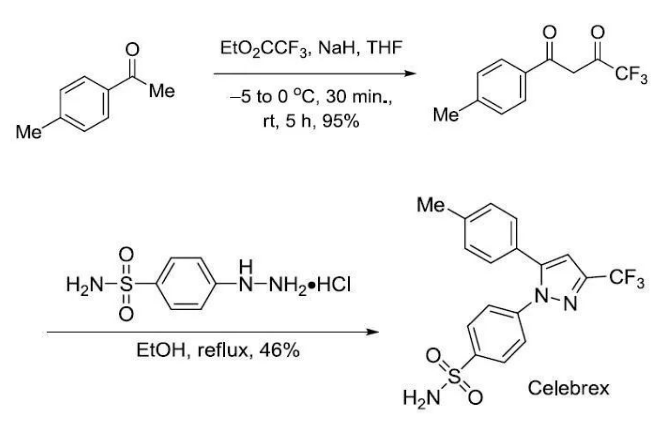 反應舉例
反應舉例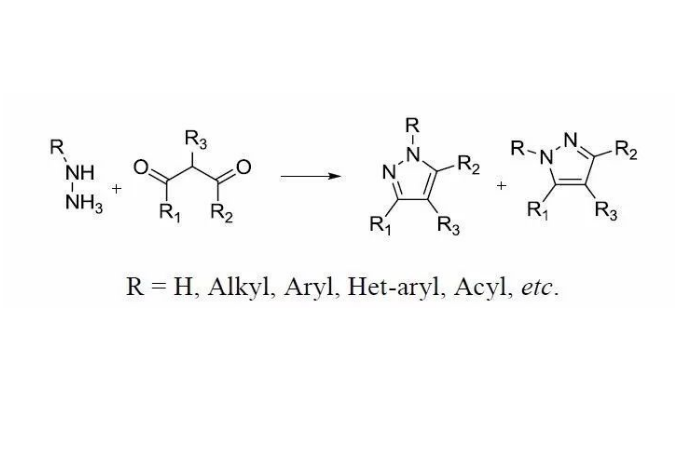
諾爾吡咯合成(Knorr吡咯合成)是一個常用的合成吡咯衍生物的有機反應,由德國化學家路德維希·諾爾(Ludwig Knorr)首先報導。肼或取代肼和1,3-二羰基化合物反應得到吡唑或吡唑酮的反應。此反應與Paal–Knorr 吡咯合成法類似。
 機理1
機理1 機理2
機理2 反應舉例
反應舉例諾爾吡咯合成(Knorr吡咯合成)是一個常用的合成吡咯衍生物的有機反應,由德國化學家路德維希·諾爾(Ludwig Knorr)首先報導。肼或取代肼和1,3-二羰基化合物反應得到...
諾爾吡咯合成(Knorr吡咯合成)是一個常用的合成吡咯衍生物的有機反應,由德國化學家路德維希·諾爾(Ludwig Knorr)首先報導。...
定義 帕爾一克諾爾A比咯合成paal-Knorr pyrrole synthesis也稱克諾爾沛白爾it比咯合成{ Knorr-paal pyrrvle synthesis )。指1.4一二默基化合物與氨或伯胺縮合形成...
帕爾-克諾爾合成(Paal-Knorr合成)是由1,4-二羰基化合物作原料環化製取呋喃、噻吩或吡咯類化合物的一種方法。它以化學家卡爾·帕爾(Carl Paal)和路德維希·克諾爾...
Conrad-Limpach合成(4-羥基喹啉或其衍生物) 120Doebner反應(合成喹啉類衍生物) 120Knorr反應(合成吡咯類衍生物) 120第四節其他 121...
1,4-二羰基化合物在無水的酸性條件下脫水,生成呋喃及其衍生物。1,4-二羰基化合物與氨或硫化物反應,可得吡咯、噻吩及其衍生物。 Paal-Knorr反應-呋喃合成法反應...
2,5-二甲基吡咯是一種化學物質,分子式 C6H9N分子量 95.15。...2. 甲酸催化的室溫無溶劑條件下利用Paal-Knorr反應合成吡咯衍生物的方法[J]. ...
第四節含一個氮原子的芳香雜環化合物的合成161 一、吡咯及其衍生物的合成161 1. Paal-Knorr吡咯合成法162 2.Barton-Zard吡咯合成法163 3. Van Leusen吡咯合成法...
Hegedus吲哚合成389Heine反應390Hinsberg噻吩合成法390Hoch-Campbell氮雜環丙烷合成391Huisgen 1,3-偶極環加成反應392Kinugasa反應394Knorr吡咯合成395...
