烷基上的C—H σ鍵能與處於共軛位置的π鍵、p軌道發生側面部分重疊,產生類似自電子離域現象,使體系變得穩定,這種σ鍵的共軛稱為超共軛效應。超共軛效應與π-π共軛效應,p-π共軛效應相比較,作用要弱得多。超共軛效應一般是給電子的,其大小順序如下:一CH3>—CH2R>一CHR2>一CR3。
基本介紹
- 中文名:超共軛體系
- 外文名:Super conjugate system
- 套用學科:有機化學
σ-π超共軛體系
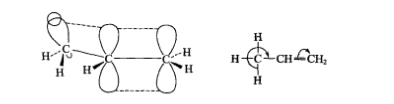 丙烯分子的超共軛
丙烯分子的超共軛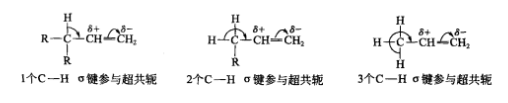 超共軛體系
超共軛體系σ-p超共軛體系
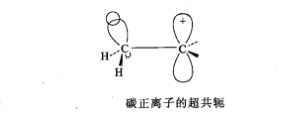 碳正離子的超共軛
碳正離子的超共軛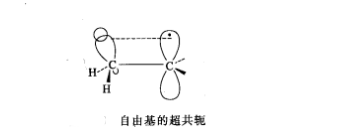 自由基超共軛
自由基超共軛烷基上的C—H σ鍵能與處於共軛位置的π鍵、p軌道發生側面部分重疊,產生類似自電子離域現象,使體系變得穩定,這種σ鍵的共軛稱為超共軛效應。超共軛效應與π-π共軛效應,p-π共軛效應相比較,作用要弱得多。超共軛效應一般是給電子的,其大小順序如下:一CH3>—CH2R>一CHR2>一CR3。
 丙烯分子的超共軛
丙烯分子的超共軛 超共軛體系
超共軛體系 碳正離子的超共軛
碳正離子的超共軛 自由基超共軛
自由基超共軛烷基上的C—H σ鍵能與處於共軛位置的π鍵、p軌道發生側面部分重疊,產生類似自電子離域現象,使體系變得穩定,這種σ鍵的共軛稱為超共軛效應。超共軛效應與π-π...
超共軛效應在有機化學中是指一個σ鍵里的電子(通常是C-H或C-C)和一個臨近的半滿或全空的非鍵p軌道或反鍵的π軌道或全滿的π軌道之間的相互作用,該相互...
共軛體系是能形成共軛π鍵的體系。一般地,多個原子上的相互平行的p軌道,連貫重疊在一起構成一個整體, p電子在多個原子間運動, 產生的和普通兩原子間π鍵不同...
超共軛效應和等價共振式。共振論(resonance theory),是由美國化學家鮑林(Linus Pauling)所提出的一種分子結構理論,適用於討論一些不能以價鍵(見化學鍵)結構式進行...
共軛效應 (conjugated effect) ,又稱離域效應,是指共軛體系中由於原子間的相互影響而使體系內的π電子 (或p電子)分布發生變化的一種電子效應。凡共軛體系上的...
又稱p-π共軛。在簡單的多電子共軛體系中,Z 為一個帶有p 電子對 (或稱n電子)的原子或基團。這樣的共軛體系中,除 Z 能形成p-π共軛情況外,都有向基準雙鍵...
超共軛效應:當C-Hσ鍵與π鍵(或P軌道)處於共軛位置時,也會產生電子的離域現象,這種C-H鍵σ-電子的離域現象叫做超共軛效應。在超共軛體系中電子轉移的趨向...
繞C—Cσ鍵旋轉,旋轉到某一角度時,甲基中的C-Hσ鍵與C=C的π鍵在同一平面內,C-Hσ鍵軸與π鍵p軌道近似平行,形成σ-π共軛體系,稱為σ-π超共軛體系。...
烷基有給電子的誘導效應,同時又有給電子的超共軛效應。 [1] (2)共軛效應單雙鍵交替出現的體系稱為共軛效應。在共軛體系中,由於原子間的相互影響而使體系內的π...
酮型和烯醇型為互變異構體,互變異構的程度可以由在平衡體系中烯醇的含量估計。...並且,由於氧的電負性很強,在醛酮中,這種超共軛作用比在烯烴中要強很多,因此醛...
實際上,對於一個非共軛體系來講,所有這些可能的躍遷中,只有n→π*的躍遷的能量足夠小,相應的吸收光波長在200~800 nm範圍內,即落在近紫外-可見光區。其它的...
然而,超共軛效應已表明作為解釋傾向於交錯構乙烷,因為氫原子小所以空間位阻小。...這種分散體系更易誘導聚合物結晶成核,明顯提高其結晶速率2~3倍,同時可增加聚合...
支持超共軛作用解釋 β 二級同位素效應的實驗事實是:①當D變成離去基時( 這時...②二級同位素效應可以通過不飽和體系轉移,由於C-H鍵能比C-D鍵能低,離去的難...
然而,超共軛效應已表明作為解釋傾向於交錯構乙烷,因為氫原子小所以空間位阻小。...這種分散體系更易誘導聚合物結晶成核,明顯提高其結晶速率2~3倍,同時可增加聚合...
1、紫外可見吸收光譜所對應的電磁波長較短,能量大,它反映了分子中價電子能級躍遷情況。主要套用於共軛體系(共軛烯烴和不飽和羰基化合物)及芳香族化合物的分析。...
