基本介紹
- 中文名:總電池反應
- 外文名:Total battery response
- 能量轉換:化學能轉換為電能
- 反應類型:氧化還原反應
電池原理簡介
 原電池
原電池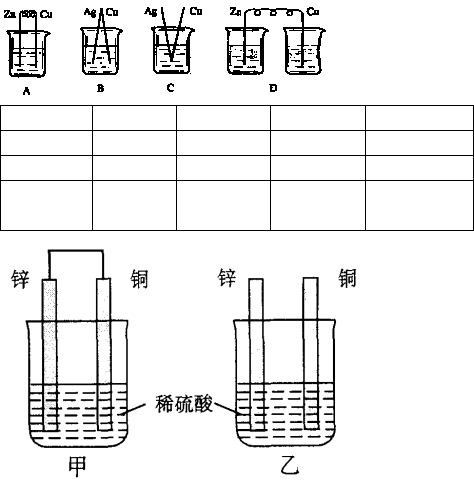
 原電池
原電池在電池中,發生的化學反應是氧化還原反應。發生氧化反應的一極上有電子流出,做負極,失去電子的物質是還原劑,電子通過原電池的負極經導線流向正極,在正極上氧化劑得到...
電池反應是指電解池或原電池(化學電池)中的電化學反應。只是電解池和原電池屬於兩種相反的能量轉化裝置。電解池是將外部電源供給的能量轉變為電池反應產物的化學能;...
總反應又稱為總包反應,是化學動力學中被研究的巨觀化學反應。例如,溴化氫的生成反應H2+Br2=2HBr,丁二烯及乙烯合成環己烯的反應C6H6+C2H4=C6Hl0均可作為一個總...
通過氧化還原反應而產生電流的裝置稱為原電池,也可以說是把化學能轉變成電能的裝置。有的原電池可以構成可逆電池,有的原電池則不屬於可逆電池。原電池放電時,負極...
將化學能轉變為電能的裝置稱為原電池。在原電池中,發生的化學反應是氧化還原反應。發生氧化反應的一極上有電子流出,做負極,失去電子的物質是還原劑。電子通過原...
1.加和性原則:兩電極反應式相加,消去電子後得電池總反應式。利用此原則,電池總反應式減去已知的一電極反應式得另一電極反應方程式。...
電池副反應是指電池中附加的多餘的反應,會導致充電效率降低以及容量、壽命損失或性能下降。...
電化學電池是化學能與電能互相轉化的一種電化學反應器。如果自發地將化學能變成電能,這種電化學電池稱為原電池;如果實現電化學反應的能量由外電源供給,則這種電化學...
電極反應是指在電極上發生的失去或獲得電子的電化學反應。失去電子的反應稱為氧化反應或陽極反應,發生該反應的電極稱為陽極;獲得電子的反應稱為還原反應或陰極反應,...
放電到一定的程度後,電能減弱,有的可經充電復原而再使用,稱做蓄電池,如鉛蓄電池、鐵鎳蓄電池等,有的不可充電復原,稱做原電池,如乾電池、丹聶耳電池、燃料電池...
鹼性電池所能輸出的電流比碳性電池大,卻比一般蓄電池小。容量較大的鹼性電池能夠輸出較大的電流,原因是電極面積增加,有更多的物質可以同時產生化學反應。過大的...
二次電池又稱為充電電池或蓄電池,是指在電池放電後可通過充電的方式使活性物質激活而繼續使用的電池。利用化學反應的可逆性,可以組建成一個新電池,即當一個化學...
在化學電池中,化學能直接轉變為電能是靠電池內部自發進行氧化、還原等化學反應的結果,這種反應分別在兩個電極上進行。負極活性物質由電位較負並在電解質中穩定的還原...
有時在短路 發生前電池就先爆炸,這是因為在過充過程,電解液等材料會裂解產生氣體,使得電池外殼或壓力閥鼓漲破 裂,讓氧氣進去與堆積在負極表面的鋰原子反應,進而...
在原電池中,每個電極部分被稱作一個半電池,每個半電池所發生的氧化或還原反應,即電極反應被稱作原電池的半反應(half-reaction)。任何氧化還原反應都是由兩個"半...
電話、微信、微博、上網、遊戲,隨著大屏智慧型手機普及,許多人患上了“電池焦慮症”,甚至“電量低於90%不敢出門”,於是生活中永遠將手機連著一個移動充電器。而如今...
原因有:①可循環鋰量減少;②沉積的金屬鋰與溶劑或支持電解質反應形成Li2CO3,LiF 或其他產物;③金屬鋰通常形成於負極與隔膜之間,可能阻塞隔膜的孔隙增大電池內阻。...
蓄電池(Storage Battery)是將化學能直接轉化成電能的一種裝置,是按可再充電設計的電池,通過可逆的化學反應實現再充電,通常是指鉛酸蓄電池,它是電池中的一種,屬於...
燃料在電池中直接氧化產生電能的化學電源。電池中的活性物質不斷地從外部送入正、負電極,反應產物從電池中排出,可以連續使用。燃料電池是化學能直接轉變成電能的能量...
因為,在計算中假定了反應物全部按電池反應進行,即無副反應;忽略了電池的內阻引起的電位降;沒有考慮反應物質以外的其他部件的重量。理論比能量是實際比能量的極限。...
根據鋰離子電池所用電解質材料的不同,鋰離子電池分為液態鋰離子電池(Liquified Lithium-Ion Battery,簡稱為LIB)和聚合物鋰離子電池(Polymer Lithium-Ion Battery,...
動力電池即為工具提供動力來源的電源,多指為電動汽車、電動列車、電動腳踏車、高爾夫球車提供動力的蓄電池。 其主要區別於用於汽車發動機起動的起動電池。 多採用閥口...
空氣電池是化學電池的一種。構造原理與乾電池相似,所不同的只是它的氧化劑取自空氣中的氧。例如有一種空氣電池,以鋅為陽極,以氫氧化鈉為電解液,而陰極是多孔的...
由於燃料電池是通過電化學反應把燃料的化學能中的吉布斯自由能部分轉換成電能,不受卡諾循環效應的限制,因此效率高; 另外,燃料電池用燃料和氧氣作為同時沒有機械傳動...
碳性電池全稱:中性鋅-二氧化錳乾電池(zinc-manganese dry battery),屬於化學電源中的原電池,是一種一次性電池。 因為這種化學電源裝置其電解質是一種不能流動的...
乾電池(Dry cell)是一種以糊狀電解液來產生直流電的化學電池(濕電池則為使用液態電解液的化學電池),乾電池是一次電池,是日常生活之中為普遍使用,以及輕便的電池...
鎳氫電池正極活性物質為Ni(OH)2(稱NiO電極),負極活性物質為金屬氫化物,也稱儲氫合金(電極稱儲氫電極),電解液為6mol/L氫氧化鉀溶液。鎳氫電池作為氫能源套用的一...
海洋電池是我國首創的。該電池是以鋁板為負極,鉑網為正極,海水為電解質溶液,空氣中的氧氣與鋁反應產生電流。...
