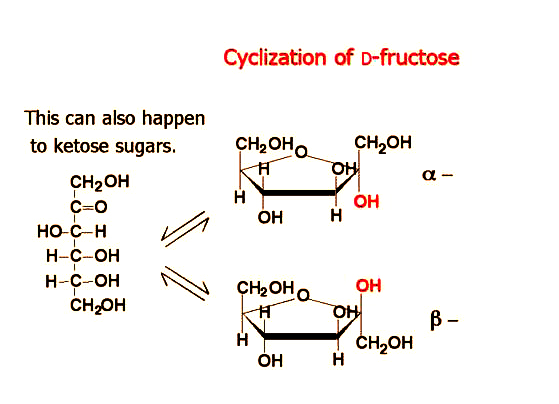
簡述
桐酸、
亞麻酸、亞油酸等,在加熱、鹼異構化與催化等反應中會環化。桐酸甲酯在180℃開始環化反應。用尿素分離出直鏈化合物後,環化單體經鹵化,脫鹵化氫的芳化,再氧化得到磷苯二甲酸而獲得證實。
亞麻酸酯,亞麻子油在二氧化碳保護下,加熱到275℃並保持十二小時,得到單環化合物。環化物有毒,所以,加熱到220℃以上的亞麻子油不宜食用,平常烹調一般不超出此溫度。
鹼異構化油也發現有環狀物,例如,亞麻子油用鹼異構化加熱到295℃時,可得到環化物,產率30~32%。若不用
乙二醇而用水作溶劑,同樣生成環狀物,雖然得率少些,但費用低,環化催化劑有硒、鈀。吸附在硅藻土上的鎳,再加3%的硫,可用於製備芳化脂肪酸,產率7%。氫化動植物油時,如氫的用量少,溫度高,油的不飽和程度高,則有利生成環狀物。氫化油中的環化物不含雙鍵。
含雙鍵的環化脂肪酸,用於製造醇酸樹脂,比天然且旨肪酸優越,乾燥時間縮短,硬度好,抗化學試劑能力強。氫化的環狀脂肪酸酯,適用於低溫潤滑劑,抗氧化,也適用於高性能透平機、飛機。環狀飽和勇旨肪酸所成的醯胺、胺,熔點特別低,有些醯胺與腈,可做乙烯類塑膠增塑劑,因能形成穩定透明的凝膠,環狀醇可用於化妝品。
環化反應
在
有機化合物分子中形成新的碳環或雜環的反應稱做環合反應,也稱閉環或成環縮合。在形成碳環時,當然是以形成碳—碳鍵來完成環合反應的。在形成含有雜原子的環狀結構時,它可以是以形成碳一碳鍵的方式來完成環合反應,也可以是以形成碳—雜原子鍵(C—N、C—O、C—S鍵等)來完成環合反應,有時也可以是在兩個雜原子之間成鍵(N—N、N—S鍵等)來完成環合反應。例如:
N—N鍵環合反應:
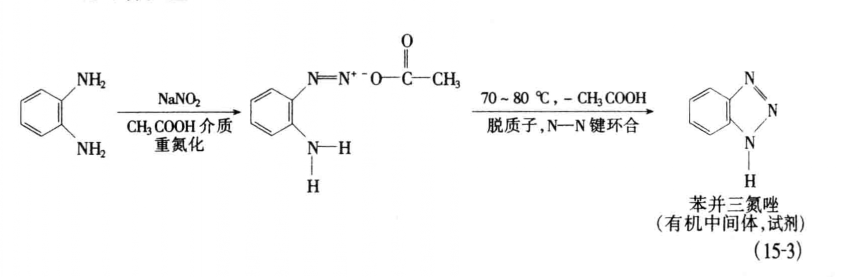 N—N鍵環合反應
N—N鍵環合反應C—C鍵環合反應:
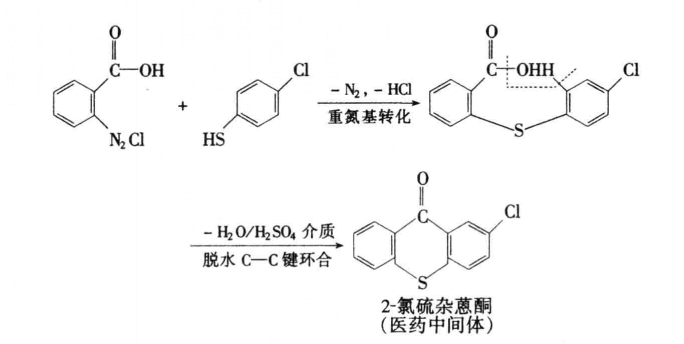 C—C鍵環合反應
C—C鍵環合反應C—S鍵環合反應:
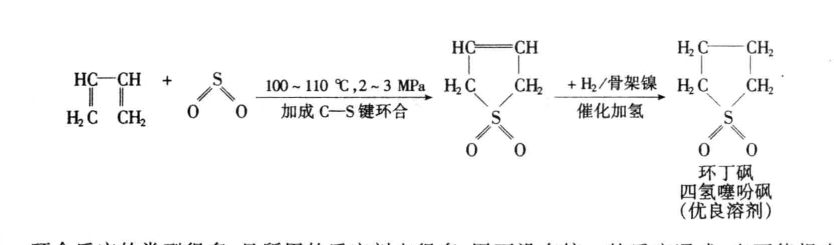 C—S鍵環合反應
C—S鍵環合反應環化反應的類型很多,且所用的反應劑也很多,因而沒有統一的反應通式,也不能提出一般的反應歷程和比較系統的一般規律。但是,根據大量事實可以歸納出以下規律:
①絕大多數環合反應都是由兩個分子之間先在適當位置發生反應、成鍵、連線成一個分子,但是還沒有形成新的環狀結構。然後,在這個分子內部的適當位置發生環合反應而形成新的環狀結構。
②具有芳香性的六元碳環以及五元和六元雜環都比較穩定,且易形成。
③有一些環合反應是由兩個分子之間在兩個適當位置同時發生反應,成鍵而形成新的環狀結構,這類反應叫做協同反應。除了少數以雙鍵加成方式形成環狀結構的環合反應以外,大多數環合反應在形成環狀結構時,總是脫落某些簡單的小分子。
環化取代重排
環化取代
重排在反應式中用符號“rd”表示,是由自由基位置引發而發生的環化反應,反應過程中發生原化學鍵斷裂(
自由基被取代下來)同時生成新鍵。環化取代重排在含飽和雜原子的長鏈烷基化合物中可見。例如ω-氯代十二烷中m/z 91(100)的含氯
碎片離子及m/z 105(25)的含氯碎片離子,都是由於環化取代重排產生的。
儘管在反應中氯給出電子的能力極弱,但生成的碳一氯鍵可以補償碳-碳鍵裂解所需的能量,這對反應是有利的。
鏈長大於6個碳原子的溴代烴,也可以通過環化取代重排,丟失R自由基,形成含溴的五元或六元環碎片離子,五元環溴離子更加穩定。
長鏈烷基鹵代烴、
硫醇、硫醚及伯胺類化合物也發生環化取代重排,生成較穩定的含硫、氮的環狀碎片離子。如下圖:
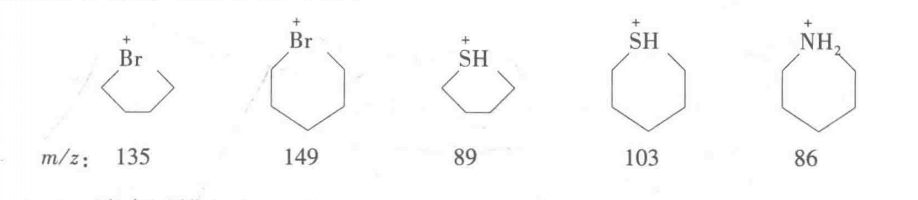 環狀碎片離子
環狀碎片離子環化聚合
非共軛雙烯的聚合生成高交聯熱固性產物是工業生產中一種重要的工藝過程,如對-苯二甲酸二烯丙基酯、雙(碳酸烯丙基)二乙二醇酯和馬來酸二烯丙基酯的聚合。但這些體系實測凝膠點總是高於理論預測值,這是由於二烯類單體進行分子內環化反應的緣故。也就是在共聚反應體系中,存在分子間的交聯反應(6.82)和分子內的環化反應(6.83)的競爭反應。
反應(6.82)說明,單體6-4聚合生成側基為雙鍵的線形聚合物,側基雙鍵進一步反應,生成交聯聚合物。同時,鏈自由基6-5會進攻分子內的側基雙鍵,分別形成環狀鏈自由基6-6和6-8,進一步聚合,生成含環的聚合物6-7和6-9。由於反應(6.83)消耗了側基雙鍵,導致聚合物的交聯度降低。當與單烯類單體共聚時,生成的共聚物結構更為複雜。例如,第二單體加到增長鏈末端二烯烴單元之前還是之後,才發生分子內環化,就會形成不同的環結構。
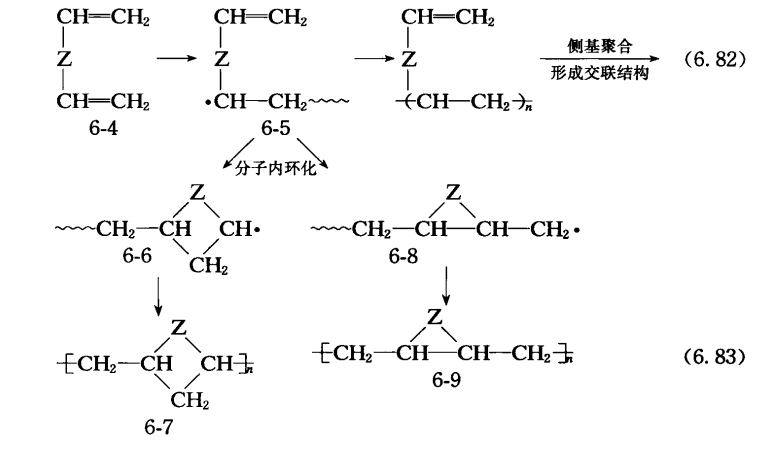 環化聚合反應圖
環化聚合反應圖不是所有雙烯類單體聚合時,都會發生交聯反應。有的單體,如雙烯丙基季銨鹽的自由基聚合生成了一個可溶、幾乎不含雙鍵的非交聯產物。此反應稱為分子內和分子間交替聚合,或稱環化聚合,生成的聚合物為主鏈含環狀結構的線形高分子。
環化反應對交聯影響程度,取決於聚合過程中形成環的大小。環化難易程度隨環的大小有如下順序:五、六元環>七元環>更大的環。當形成五、六元環時,成環聚合為主導反應。例如,(甲基)丙烯酸酐、二烯丙基季銨鹽和甲基丙烯酸烯丙基酯等1,6-二烯烴(Z含有三個成環原子)都能環化聚合,形成五元環或六元環的結構單元,或者兩種環兼而有之。形成五元環是動力學過程控制,經仲碳自由基完成環化過程;經較為穩定的叔碳自由基形成六元環的過程則屬於熱力學控制過程。二烯丙基季銨鹽、二乙烯基縮甲醛都毫無例外地形成五元環結構單元;丙烯酸酐形成五元環和六元環兩種結構單元;甲基丙烯酸酐只形成六元環一種結構單元。對於丙烯酸酐聚合,降低聚合溫度和溶劑極性可大大減小五元環結構單元的形成;而甲基丙烯酸酐的環化聚合則不受溫度和溶劑極性的影響。
分子間的聚合速率(Rp)分子內的環化速率(Rc)的相對大小與單體濃度相關,如下式所示。
Rp/Rc =2kp[M·][M]/kc[M·] =2kp[M]/kc
其中,[M]為二烯烴單體的濃度。由此可知,增加單體濃度有利於分子間的鏈增長反應。與分子間鏈增長反應相比,分子內的環化反應具有較高的活化能和較大的碰撞頻率因子,升高溫度和增加溶劑極性可提高環化聚合的機率。
不對稱的二烯烴如甲基丙烯酸烯丙基酯,它的兩個雙鍵具有不同的活性,其環化的可能性顯著降低。
 N—N鍵環合反應
N—N鍵環合反應 C—C鍵環合反應
C—C鍵環合反應 C—S鍵環合反應
C—S鍵環合反應 環狀碎片離子
環狀碎片離子 環化聚合反應圖
環化聚合反應圖