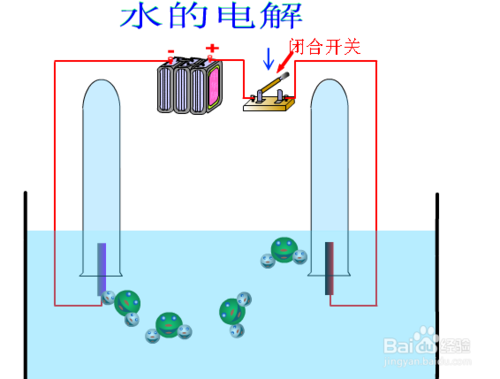
概念
電解水生產氫氣和氧氣是一個眾所周知的技術,其基本原理是水被直流電力轉換成氣態的氫和氧,也就是燃料電池逆過程。尼科爾森(Nicholson)和卡萊爾(Carlisle)在1800年首次證明水電解過程。法拉第在1934年明晰了水電解原理,提出了“電解”概念。從水中產生氫氣電解用於商業最早是由歐瑞康(Oerlikon)工程公司於1902年開始。
根據操作溫度,主要有兩種類型的電解器:低溫電解技術和高溫電解。LTE分為鹼性電解器和質子交換膜電解器兩種,它們均已實現商業化運行,可以實現約75%的能量效率。以氫氧化鉀水溶液(OH-)作為電解質的鹼性水電解技術是一項成熟技術,占有商業水電解器的絕大部分市場,未來主要的研發問題是在改進能源效率的同時,降低電解設備成本。鹼性電解質膜正在開發中,它的成功會為水電解技術帶來較大進步。
實驗的探討
原理
水在直流電的作用下,能分解成氫氣和氧氣。當電火花通過氫、氧混和氣體時,他們即化合成水。這兩個實驗都說明水是由氫、氧兩種元素組成的,從實驗結果還可以知道它們的體積比為2∶1。
準備
1.裝配霍夫曼電解器霍夫曼電解器是由兩支各為50毫升的刻度玻璃管所組成,上端各具一個活塞,下端與
三通管相連線。刻度管下用嵌有鉑電極的
橡皮塞塞緊,三通管的中間玻璃管上連線一支球形漏斗管。如圖7-26所示。
如果沒有霍夫曼電解器,可以用兩支
酸式滴定管裝配。在
滴定管的下端,裝一個帶有電極和直角玻璃導管的橡皮塞。電極可以用
鎳鉻絲、銅片或
不鏽鋼片製成。兩支直角玻璃導管用
T形管相連,再接上一支漏斗管作注入
電解液用。簡易裝置可只用兩支滴定管,倒立在水槽內,在管口處各插入一個電極即可。但要檢驗
電解水生成的氫氣和氧氣時,必須把滴定管從水槽中取出,倒過來檢驗。
如果連
滴定管也沒有,可以用兩支長約40厘米,
內徑約1厘米的玻璃管組裝。上端裝一個配有玻璃導管的單孔塞,用短玻璃管接上一支長約4厘米的尖嘴管作為排氣管,用彈簧夾控制氣流。下端裝一個帶有電極和直角玻璃管的
橡皮塞,直角玻璃管再與T形管和漏斗管相連線。玻璃管里所得氣體的體積可用刻度板來計量。先將玻璃管帶尖嘴管的一端向下豎直,卸去帶電極的橡皮塞,倒入3毫升水,使液體高出橡皮塞上玻璃管的口,沿液面畫一條線。再加入20毫升水,沿液面也畫一條線。將水倒出,把玻璃管橫放在一張白紙上,把玻璃管上標出的兩條線的距離畫成20等分,每一等分表示1毫升,標上數字。將所需部件裝配起來,連同標線紙一起固定在木板上,即成為
水電解器。
為了便於檢驗
電解水後所得的氫氣和氧氣,常在裝陰極的玻璃管上端用橡皮管接上一根彎曲的尖嘴玻管,以便讓氫氣緩緩流出。在裝陽極的玻璃管上用橡皮管接上一個空的
氯化鈣乾燥管,使流出的氧氣積集其中。
2.組裝水的合成器水的合成常在量氣管內進行,它是一支長約45厘米、內徑約1.3厘米的厚壁玻璃管,一端封閉,一端敞開。封閉的一端插入兩根鉑絲,絲端相距約2~3毫米。管上有刻度,有25毫升和50毫升兩種。如果沒有這種量氣管,可以自己組裝,取長約40~45厘米、內徑約1.2~1.5厘米的厚壁玻璃管一支,上端裝一插有兩根銅絲電極的橡皮塞。塞內的銅絲約留3厘米長,將1厘米向上彎折成一鉤子,用一根從廢電燈泡中取出的鎢絲(也可以用細電熱絲代替)相連線,鉗緊,使它固定在兩根銅絲之間。橡皮塞外的銅絲也約留3厘米長,捲成圓圈,以便跟導線相連線。
這樣組裝的水合成器,玻璃管口的橡皮塞必須塞得很緊,否則氫、氧爆炸時塞子會被膨脹的氣體彈出管口。玻璃管內氣體的體積可用上述方法所制的刻度板來量度,但可以簡單一些,只要分成4個等分就可以了。把玻璃管連同塞子一起倒轉豎直,分四次加水入內,每次3毫升,在管外沿水平面套上橡皮圈作出四個記號即可。
操作
1.水的電解打開
霍夫曼電解器兩邊刻度玻璃管上的活性塞,往球形漏斗里倒入濃度為1∶8的
稀硫酸溶液。待兩個刻度管里的液體將升到活塞時,傾倒的速度減慢,使液面稍稍超過兩個活塞。關閉活塞,用捲成細卷的濾紙條伸入活塞上的玻璃管中,吸去超過活塞的液體,再分別裝上檢驗氫氣和氧氣的裝置。在兩個電極的導線上串連一電鍵,和18伏的直流電源相連線。通電後兩極上即發生大量氣泡,4~5分鐘後,在陰極這一管
里約可積聚氫氣10毫升,在陽極這一管里約可積聚
氧氣5毫升。
理論上水電解後生成氫氣的體積應為氧氣的2倍。由於氧氣在水中的溶解度比氫氣略大,以及電極上產生的副反應等原因,一般所得氧氣的體積總是比理論值小。為了減小誤差,常在先通電一段時間,讓分解出來的氧氣溶解在陽極一方的液體裡,使它達到飽和,然後放去兩管內積聚的氣體,重新調整後再進行實驗。
2.水的合成先將量氣管盛滿水,倒轉放入水槽里,使敞口一端沒入水面下約3厘米。用排水法先通入氧氣6毫升,再通入氫氣6毫升,使兩者充分混和,然後將封閉一端露在管外的兩根鉑絲和
感應圈以及6~8伏
直流電源相連線,如圖7-33所示。
用電鍵使電路閉合,管內鉑絲之間即產生電火花,同時引起氫、氧混和氣體發生爆炸,使整個裝置強烈振動。爆炸時管內水面突然下降,隨即迅速回升到原體積的1/4處。表明4體積混和氣體中有3體積起了作用。
用玻璃管和帶有電極的橡皮塞組裝的水合成器的操作方法和上述基本相同,所不同的是可以不用感應圈。把橡皮塞上的兩個銅絲圈分別跟6伏直流電源和電鍵相連線。當電路閉合時,管中
鎢絲立即被燒斷,這時發生的火花就引起氫、氧混和氣體發生爆炸,結果使管內的氣體減少到原體積的1/4。
注意事項
1.
電解水時所用的電壓和酸溶液的濃度對釋出氣體的速度很有關係。採用18~24伏電壓和硫酸濃度為1∶6~1∶8時,兩極上產生氣體的速度較快,氣泡大,只需4~5分鐘即可積聚一定量的氣體,看到明顯的體積比。
2.電解水所得氧氣體積偏低的主要原因是由於副反應所造成的:
2H2SO4=2H+2HSO4
在陰極2H+2e=H2
在陽極2HSO4-2e=H2S2O8
H2S2O8+H2O=H2SO4+H2SO5
H2SO5+H2O=H2SO4+H2O2
陽極處所生成的過氧化氫在酸性溶液里比較穩定,不易分解出氧,所以
氧氣的體積就偏低了。氧氣和氫氣在水中溶解度的不同是次要的。
3.合成水時的量氣管必須緊緊地固定在鐵架台上,最好在玻璃水槽底墊一層塑膠片。
4.合成水時,氫氣和氧氣的體積比不要用2∶1,因為這時的爆炸力最強。為了預防玻璃管炸裂,可以用尼龍紗或塑膠紙做一個防護套罩在玻璃管的上部。
其它實驗方法
裝置Ⅰ
用500毫升燒杯作電解槽,電極用粗銅絲套上塑膠管制成,兩端各露出2厘米並彎成鉤形,一端扣在燒杯上,另一端作電極。用15%的氫氧化鈉溶液作
電解液,用兩支同樣大小的試管作集氣管。由於氫氧化鈉溶液有腐蝕性,裝置時可以先在試管內盛滿氫氧化鈉溶液,蓋上一張薄紙後倒轉過來,因
大氣壓強大於試管內液體的壓強,紙片不會落下。將試管倒插入液面下,用
鑷子夾去紙片,把試管套在電極上,並用有兩個圓孔的硬紙板將試管固定起來。電解時,接上6~12伏的
直流電源,兩極上即有很多氣泡發生。3分鐘後,陰極處可取得約16毫升氫氣,陽極處可取得約8毫升的氧氣。
要檢驗所得的氫氣和氧氣,可以將粗鐵絲的一端彎成一個圓圈,放上硬紙片,墊在試管口下把它取出,豎直後檢驗。
裝置Ⅱ
是用一個截去底的大鹽水瓶作
電解槽,電極是用兩根粗銅絲穿過橡皮塞而製成。為了使電解限制在小範圍內進行,用瓶頸作電解槽。先在瓶內注水高出電極3~4厘米,然後用
長頸漏斗將15%的氫氧化鈉溶液注入瓶頸的底部,將清水排擠到上層。用兩支大小相同的試管盛滿清水後倒立在電極上方,然後通電,同上述方法進行實驗。這個方法操作比較方便。
相關工藝
日本開發了固體高分子型水電解工藝,可把氟樹脂系的離子交換膜用作質子導電體的固體電解質。固體高分子電解質由於薄膜化,電解質電阻變小,有利於在高電流密度下進行電解運轉。
如使用固體氧化物電解質.就有可能套用使用水蒸氣的高溫水電解工藝i這種工藝理論分解電壓小,電能必需量變小,特別是作為電解反應阻力的過電位變小.所以可期望成為效率最高、以最低槽電壓電解運轉的電解法。
日本開發的固體高分子型水電解槽中,陰極為塗敷鉑的石墨電極材料,陽極為銥系合金及氧化銥,與離子交換膜組裝問隙為150~300um,從而實現了高效率。陰極基體為石墨.陽極基體多使用鈦。