基本介紹
- 中文名:氯化氫
- 外文名:hydrogen chloride、hydrochloride
- 技說明書編碼:995
- CAS編號:7647-01-0
- 分子式:HCl
- 分子量:36.4606
- 熔點:158.8K(-114.2℃)
- 沸點:187.9K(-85℃)
- 密度:1.477 g/L(25℃)(g)
- 溶解度:極易溶於水(1:500)
- 屬性:化學試劑
- 溶液酸鹼性:強酸性
- 安全術語:S:7-9-26-36-37-39-45
- 警示術語:R:23-24-25-35-37
- 外觀:無色氣體
物理性質
摩爾質量 | 36.4606 g/mol |
外觀 | 無色吸濕性氣體 |
密度 | 1.477 g/L(25℃)(氣) |
相對密度(水=1) | 1.19 |
相對蒸氣密度(空氣=1) | 1.27 |
熔點 | 158.8K(-114.2℃) |
沸點 | 187.9K(-85℃) |
溶解性(水) | 72g/100mL(20℃)(標準壓強) |
飽和蒸氣壓(Pa) | 4225.6(20℃) |
化學性質
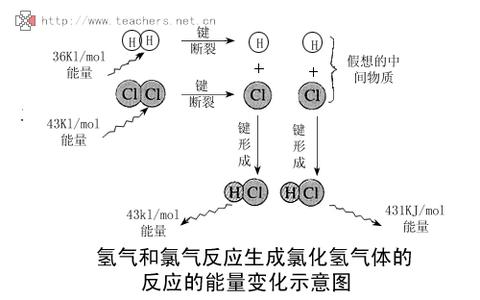 氫氣氯氣反應能量變化圖
氫氣氯氣反應能量變化圖
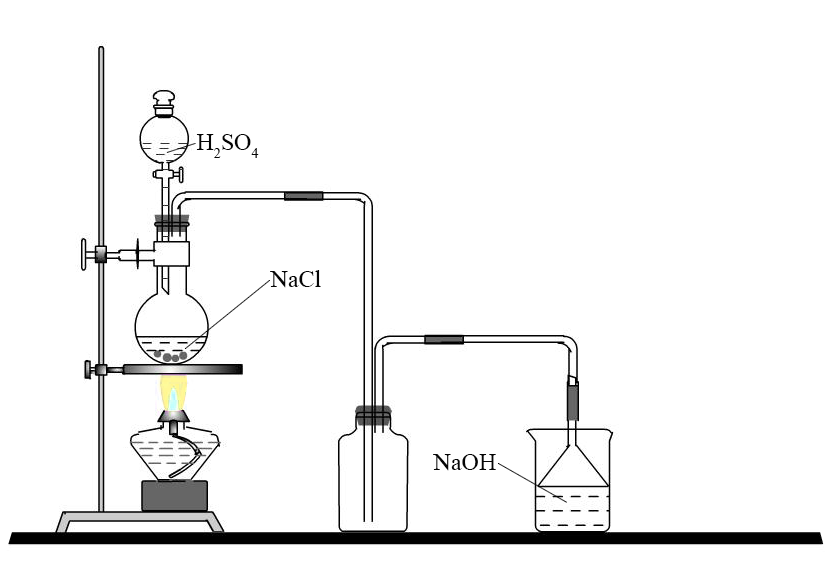 實驗室製取氯化氫
實驗室製取氯化氫