主要套用 用途:一種
稀有氣體 。用作電弧焊接(切割)不鏽鋼、鎂、鋁、和其它合金的
保護氣體 。還用於鋼鐵、鋁、鈦和鋯的冶煉中。放電時氬發出紫色輝光,又用於照明技術和填充日光燈、
光電管 、照明管等。
裝有氬氣的灰色鋼瓶 在釀酒的過程中,啤酒桶里的填充物,它可以把
氧氣 置換,以避免啤酒桶里的原料被氧化成乙酸。
熱處理工藝也用於代替氮氣和氨氣,效果更是超過氮氣和氨氣,不鏽鋼熱處理時採用氬氣保護折彎效果更好不易斷裂。
人體危害 健康危害:普通大氣壓下無毒。高濃度時,使氧分壓降低而發生窒息。氬濃度達50%以上,引起嚴重症狀;75%以上時,可在數分鐘內死亡。當空氣中氬濃度增高時,先出現呼吸加速,注意力不集中,共濟失調。繼之,疲倦乏力、煩躁不安、噁心、嘔吐、昏迷、抽搐,以致死亡。液態氬可致皮膚凍傷;眼部接觸可引起炎症。毒理學資料及環境行為危險特性:若遇高熱,容器內壓增大,有開裂和爆炸的危險
泄漏案例 烏魯木齊機場加氣站施工時氬氣泄漏致5死5傷
天山網訊(記者 田山 報導) 烏魯木齊市高新區一企業2名工人在烏魯木齊國際機場飛機維修基地加氣站旁一工程施工焊接過程中,發生氬氣泄漏窒息。機場機務維護人員及醫護人員在不明情況下進行施救,又造成多人昏迷。事故造成5人死亡、5人重傷。
事故發生後,自治區黨委副書記、自治區主席努爾·白克力立即作出批示,要求自治區安監局迅速趕赴事故現場,全力以赴搶救受傷人員,做好遇難人員的善後處置工作,徹查事故原因。
自治區安監局、烏魯木齊市等有關部門組織人員迅速趕赴醫院和事故現場,進行傷員搶救和事故處理工作。事故原因正在進一步調查中。
氬化合物 芬蘭科學家合成惰性氣體元素氬化合物
芬蘭
赫爾辛基大學 的科學家在24日出版的英國《
自然 》雜誌上報告說,他們首次合成了惰性氣體元素氬的
穩定化合物 ——
氟氬化氫 ,分子式為HArF。這樣,6種惰性氣體元素氦、氖、氬、氪、氙和氡中,就只有
原子量 最小的
氦 和
氖 尚未被合成穩定化合物了。惰性氣體可廣泛套用於工業、醫療、光學套用等領域,合成惰性氣體穩定化合物有助於科學家進一步研究惰性氣體的
化學性質 及其套用技術。
HArF模型 在惰性氣體元素的
原子 中,電子在各個電子層中的排列,剛好達到穩定數目。因此原子不容易失去或得到電子,也就很難與其它物質發生
化學反應 ,因此這些元素被稱為“
惰性氣體元素 ”。
在
原子量 較大、
電子數 較多的惰性氣體原子中,最外層的電子離原子核較遠,所受的束縛相對較弱。如果遇到吸引電子強的其他原子,這些最外層電子就會失去,從而發生化學反應。1962年,加拿大化學家首次合成了
氙 和
氟 的化合物。此後,
氡 和
氪 各自的化合物也出現了。
原子越小,電子所受約束越強,元素的“惰性”也越強,因此合成氦、氖和氬的化合物更加困難。赫爾辛基大學的科學家使用一種新技術,使氬與氟化氫在特定條件下發生反應,形成了
氟氬化氫 。它在低溫下是一種固態穩定物質,遇熱又會分解成氬和氟化氫。科學家認為,使用這種新技術,也可望分別製取出氦和氖的穩定化合物。
在加拿大工作的英國年輕化學家巴特列特(N.Bartlett)一直從事無機
氟化學 的研究。自1960年以來,文獻上報導了數種新的
鉑族金屬 氟化物,它們都是
強氧化劑 ,其中高價鉑的氟化物
六氟化鉑 (PtF6)的氧化性甚至比氟還要強。巴特列特首先用PtF6與等
摩爾 氧氣在室溫條件下混合反應,得到了一種深紅色固體,經
X射線衍射分析 和其他實驗確認此化合物的化學式為O2PtF6,其反應
方程式 為:
O2 +PtF6 →O2 PtF6
這是人類第一次製得O+2的鹽,證明PtF6是能夠氧化
氧分子 的強氧化劑。巴特列特頭腦機敏,善於聯想類比和推理。他考慮到O2的
第一電離能 是1175.7
千焦 /摩爾,氙的第一電離能是1175.5千焦/摩爾,比氧分子的第一電離能還略低,既然O2可以被PtF6氧化,那么氙也應能被PtF6氧化。他同時還計算了
晶格能 ,若生成XePtF6,其晶格能只比O2PtF6小41.84千焦/摩爾。這說明XePtF6一旦生成,也應能穩定存在。於是巴特列特根據以上推論,仿照合成O2PtF6的方法,將PtF6的蒸氣與等摩爾的氙混合,在室溫下竟然輕而易舉地得到了一種橙黃色固體XePtF6:
Xe+PtF6→XePtF6 該化合物在室溫下穩定,其蒸氣壓很低。它不溶於
非極性溶劑 四氯化碳 ,這說明它可能是離子型化合物。它在
真空 中加熱可以升華,遇水則迅速水解,並逸出氣體:
2XePtF6+6H2O→2Xe↑+O2↑+2PtO2+12HF
發現歷史 具有歷史意義的第一個含有
化學鍵 的“惰性”氣體化合物誕生了,從而很好地證明了巴特列特的正確構想。1962年6月,巴特列特在英國Proccedings of the Chemical Society雜誌上發表了一篇重要短文,正式向化學界公布了自己的實驗報告,一下震動了整個化學界。持續70年之久的關於稀有氣體在化學上完全惰性的傳統說法,首先從實踐上被推翻了。化學家們開始改變了原來的觀念,摘掉了冠以稀有氣體頭上名不副實的“惰性”的帽子,拆除了人為的樊籬,很快形成了一個合成和研究新的稀有氣體化合物的熱潮,開闢了一個稀有氣體化學的新天地。
認識上的障礙一旦拆除,更多的稀有氣體化合物很快被陸續合成出來。就在同年8月,柯拉森(H.H.Classen)在加熱加壓的情況下,以1∶5體積比混合氙與氟時,直接得到了XeF4,年底又製得了XeF2和XeF6。氙的氟化物的直接合成成功,更加激發了化學家合成稀有氣體化合物的熱情。在此後不長的時間內,人們相繼又合成了一系列不同價態的氙氟化合物、氙氟氧化物、氙氧酸鹽等,並對其物理化學性質、
分子結構 和化學鍵本質進行了廣泛的研究和探討,從而大大豐富和拓寬了稀有氣體化學的研究領域。到1963年初,關於氪和氡的一些化合物也陸續被合成出來了。至今,人們已經合成出了數以百計的稀有氣體化合物,但卻僅限於
原子序數 較大的氪、氙、氡,至於原子序數較小的氦、氖、氬,仍未製得它們的化合物,但有人已從理論上預測了合成這些化合物的可能性。1963年,皮門陶(Pimentaw)等人根據HeF2的
電子排布 與穩定的HF-2離子相似這一點,提出了利用
核反應 製備HeF2的3種構想:(1)製取TF-2,再利用氚〔3H(T)〕的β衰變合成HeF2:TF-2→HeF2+β;(2)用熱
中子輻射 LiF,生成HeF2;(3)直接用α粒子轟擊固態氟而產生HeF2。但
毛姆 等人則認為,HeF2和HF-2的電子排布雖然相似,但HF-2可以看成是一個H-跟兩個F原子作用成鍵,H-的
電離能 僅為22.44
千焦 /摩爾,而He的電離能卻高達 801.5千焦/摩爾,因此是否存在HeF2,在理論上是值得懷疑的,氦能否形成化合物,至今仍是個不解之謎。
急救處理 一:切斷氣源,迅速撤離泄漏污染區,處理泄漏事故人員戴自給
正壓式呼吸器 ,處理液氬應配帶防凍護具。若氣瓶泄漏而無法堵漏時,將氣瓶移至空曠安全處放。二、防護措施呼吸系統防護:一般不需特殊防護。但當作業場所空氣中
氧氣 濃度低於18%時,必須佩戴空氣呼吸器、氧氣呼吸器或長管面具
處置儲存 儲存注意
儲存於通風庫房,遠離火種、熱源;氣瓶應有防倒措施。大於10立方米低溫液體儲槽不能放在室內。瓶裝氣體產品為高壓充裝氣體,使用時應經減壓降壓後方可使用。包裝的氣瓶上均有使用的年限,凡到期的氣瓶必須送往有部門進行安全檢驗,方能繼續使用。每瓶氣體在使用到尾氣時,應保留瓶內余壓在0.5MPa,最小不得低於0.25MPa余壓,應將瓶閥關閉,以保證氣體質量和使用安全。瓶裝氣體產品在運輸儲存、使用時都應分類堆放,嚴禁可燃氣體與助燃氣體堆放在一起,不準靠近明火和熱源,應做到勿近火、勿沾油臘、勿爆曬、勿重拋、勿撞擊,嚴禁在氣瓶身上進行引弧或電弧,嚴禁野蠻裝卸。
正式壓呼吸器 消防注意
滅火方法:本品不燃。切斷氣源。噴水冷卻容器,可能的話將容器從火場移至空曠處
貯運注意事項
在貯運過程中輕裝輕卸,嚴防碰損,防止高溫。氬氣沒有腐蝕性,在常溫下可使用碳鋼、不鏽鋼、銅、銅合金、等通用金屬材料及一般的塑性材料和彈性材料。在低溫下常用聚四氟乙烯和聚三氟氯化乙烯聚合體來作墊圈、隔膜等。
安全防護 氬本身無毒,但在高濃度時有窒息作用。當空氣中氬氣濃度高於33%時,即氧氣濃度比平時減少 2/3以下時,就有窒息的危險。當氬氣濃度超過50% 時,出現嚴重症狀,濃度達75%以上時,能在數分鐘內死亡。
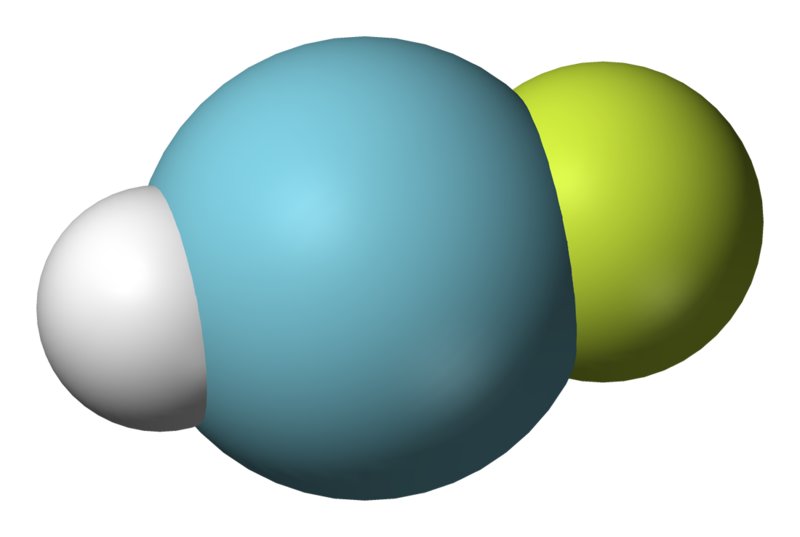 HArF模型
HArF模型 正式壓呼吸器
正式壓呼吸器
 HArF模型
HArF模型 正式壓呼吸器
正式壓呼吸器