物化性質
該物質Fe為+2價,S為-1價,較為特殊,整個原子團S
2為-2價。

立方體晶面上有與晶棱平行的條紋,各晶面上的條紋相互垂直。集合體呈緻密塊狀、粒狀或結核狀。淺黃(銅黃)色,條痕綠黑色,強金屬光澤,不透明,無解理,參差狀斷口。摩氏硬度較大,達6~6.5,小刀刻不動。比重4.9~5.2。在地表條件下易風化為褐鐵礦。
熔點:1171 ℃
密度:5.0 g/cm
溶解性:不溶於水和稀鹽酸,溶於硝酸並有硫磺析出
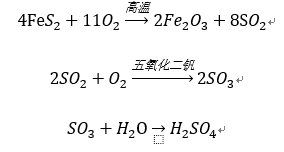 氧化反應生成三氧化二鐵、二氧化硫、硫酸反應方程式
氧化反應生成三氧化二鐵、二氧化硫、硫酸反應方程式FeS2作為黃鐵礦的主要成分,具有反磁性,室溫為非活性物質,溫度升高后變得活潑。在空氣中氧化成氧化鐵和二氧化硫,主要用於製造二氧化硫、硫酸及鋰電池。
同時黃鐵礦(pyrite)二硫化亞鐵是一種在自然界儲量非常豐富的無毒環境友好型間接帶隙半導體材料,帶隙寬度為0.95 eV。非常接近理想太陽能電池材料所需要的1.1 eV的要求,同時具有優良的光吸收能力,吸收係數達到105 cm-1。因此二硫化亞鐵材料是一種非常具有潛力的新型光伏材料。2009年相關文獻報導中,其在23種材料中居榜首成為最有潛力的代矽高效低價太陽電池材料。
分辨
由於黃鐵礦顏色與黃金相似,如何識別“愚人金”和真正的黃金的問題相應而生。解決辦法主要依據黃鐵礦的物化性質。首先,只要拿它在不帶釉的白瓷板上一划,一看劃出的條痕(即留在白瓷板上的粉末),就會真假分明了。金礦的條痕是金黃色的,
黃鐵礦的條痕是綠黑色的;其次,用手掂一下,手感特別重的是黃金,因為
自然金的比重是15.6~18.3 g/cm,而黃鐵礦只有4.9~5.2 g/cm。另外,放在硝酸里泡一泡,黃鐵礦溶於硝酸溶液,而真金不溶更不會反應生成氣泡!
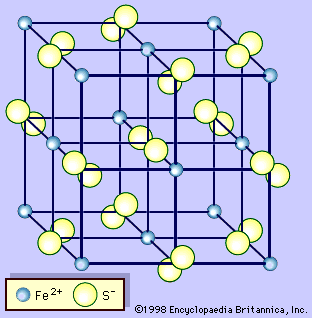 二硫化鐵立方晶型
二硫化鐵立方晶型存在方式
在自然界中FeS
2主要以白鐵礦和黃鐵礦兩種礦物形式存在,黃鐵礦是分布最廣泛的硫化物礦物,在各類岩石中都可出現。黃鐵礦是提取硫和製造硫酸的主要原料,它還是一種非常廉價的古寶石。在英國
維多利亞女王時代(公元1837~1901年),人們都喜歡飾用這種具有特殊形態和觀賞價值的寶石。它除了用於磨製寶石外,還可以做珠寶玉器和其它工藝品的底座。
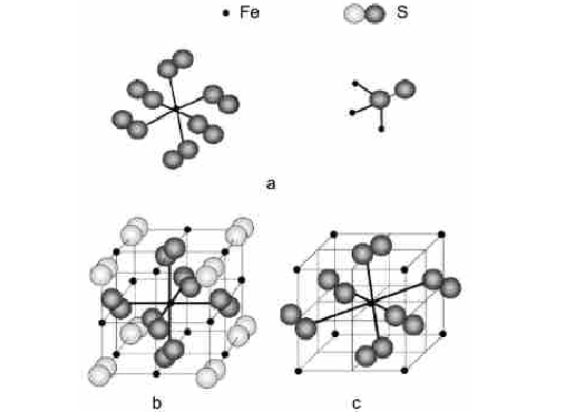 (a)陰陽離子配位形式; (b)立方晶系黃鐵礦; (c)斜方晶系白鐵礦
(a)陰陽離子配位形式; (b)立方晶系黃鐵礦; (c)斜方晶系白鐵礦從黃鐵礦化學組成方面分析其存在方式,一般而言,對於天然的黃鐵礦,硫偏離理想組分的量(質量百分數)在1.3 %以下,即對應於FeS2-x(x≤0.07)。在水存在的情況下,很容易發生如下氧化反應:
2FeS2+O2+2H2O→2FeSO4+2H2SO4
其中間產物有硫代硫酸鹽、亞硫酸鹽和硫等。由於黃鐵礦的摩爾體積比硫元素小,因此在氧化過程中產生的硫等不會導致表面膨脹,生成的表面氧化物可以有效防止繼續氧化。
用途
硫酸工業
在橡膠、造紙、紡織、食品、火柴等工業以及農業中均有重要用途。特別是國防工業上用以製造各種炸藥、發煙劑等。以硫鐵礦為原料製取硫酸,其礦渣可用來煉鐵、煉鋼。若爐渣含硫量較高,含鐵量不高時,可以用作水泥的附屬原料——混合料。
上游原料:柴油、工業導火索、雷管、煤、汽油、水泥、炸藥
下游產品:硫酸、氯磺酸、硫酸錳、二氧化硫、硫磺、鐵粉、過磷酸鈣、酚醛樹脂漆類、氨合成催化劑
金屬冶煉工業
硫化鐵礦這種主要成分為FeS2的礦石,含鐵量為46.6 %,而硫的含量達到53.4 %,呈現灰黃色,比重約為4.95~5.10。同時這種礦石常常含有許多其它較貴重的金屬,如銅、鎳、鋅、金、銀等;同時,硫鐵礦又常與銅、鉛、鋅、鉬等硫化礦床共生,並含有金、鈷、鉬及稀有元素硒等,能綜合回收利用。所以常被用做金屬冶煉工業的原料。
工業上常利用黃鐵礦制硫酸工藝的殘渣作為鋼鐵冶金原料使用。殘渣主要化學成分為Fe2O3,一般含鐵40 %~55 %,含硫1.5 %~2.0 %,硫酸渣作為金屬冶煉的原料,主要是利用其中含鐵成分,降低燒結原料的生產成本。燒結料中硫酸渣的陪加量一般在10 %以下。將硫酸渣進行處理,增加細度,提高其含鐵量,降低含硫量,可作為球團礦的原料。
光電材料
FeS2具有合適的禁頻寬度,較高的光吸收係數,可製作極薄(<200 nm)的太陽能薄膜電池,價格便宜資源豐富,無毒,具有很好的環境相容性,適合大規模生產,被認為是一種極具發展潛力的太陽能電極材料。所以商業電池的正極材料都採用天然的FeS2,但是天然FeS2由於雜質含量高、粒徑大等問題,其產品實際電化學性能與其理論值相差甚遠,需要進一步處理以提高其放電性能。
而人工合成的 FeS2由於純度高,粒徑小,晶粒粒徑的減小增強了Li嵌入FeS2形成LixFeS2的動力學特徵,因此合成的FeS2正極具有更高的比容量,其電化學性能要優於天然 FeS2,所以越來越多的科研工作者致力於合成 FeS2的研究。
(1) 天然FeS2的改性
將天然FeS2在氮氣中加熱後再用酸洗。實驗結果表明,經過改性處理後的FeS2中金屬氧化物和金屬硫化物雜質的含量明顯減少,並且處理後的FeS2的晶粒尺寸也要小於天然FeS2。晶粒小和純度高是Li/改性FeS2電池放電容量顯著增加的主要原因。
在有添加劑PZ 的條件下,用間歇式攪拌磨可製備粒度小於310μm的黃鐵礦超細粉體,最佳超細粉體製備工藝是:球料比為5:1,礦漿濃度為50 %,磨礦時間為4 h,給料粒度應儘可能小。但是黃鐵礦在超細粉磨過程中極易發生氧化,這是選礦行業中長期以來難以解決的問題。
在正極材料中加入金屬單質和氧化物以及增加電解液中無機鹽的含量,使Li/FeS2電池的放電容量和放電平台都有顯著改善。製造電池時最好採用複合添加劑,使電池在不同的放電制度下都有良好的性能,但主要考慮在重負載條件下的性能。最佳的生產條件為金屬0.5 %、氧化物3 %、無機鹽0.4 %。
通過在還原的FeS2正極材料微粒表面包覆一層很薄的離子導電保護膜(SEI膜)可以為全充電或全放電狀態下的正極活性物質提供保護,從而改善電池的電化學性能。包覆了SEI膜的正極活性物質裝配的電池在500次100 %放電循環中每個循環的容量衰減小於0.1 %。
用明膠/二甲基亞碸溶液對天然 FeS2 進行改性處理,取得了不錯的效果。FeS2正極材料的可逆比容量顯著增加可能歸因於明膠對FeS2晶粒的包覆,從而有效地減弱了在Li嵌入和脫出過程中電解液對正極材料的溶解作用。
(2) 合成FeS2的研究
電化學沉積法合成FeS2:電化學沉積法工藝簡單,成本低,容易大面積成膜,具有重要的研究價值。電化學沉積法製備FeS2薄膜與基片選擇、硫化溫度、硫化時間、硫化壓力等影響因素密切相關。
水熱法合成FeS2:水熱法是在特製的密閉反應容器(高壓釜)里,採用溶液為反應介質,通過對反應容器加熱,創造一個高溫、高壓的反應環境,使得通常難溶或不溶的物質溶解並且重結晶。在製備過程中S原子的引入有利於增加成核數目,提高FeS2微晶的結晶度;對於特定的水熱反應體系,隨著反應溫度的升高合成的FeS2粉體顆粒直徑將增大;在一定範圍內,反應時間對粉體粒徑的影響呈線性。
溶劑熱法合成FeS2:溶劑熱法就是在水熱法的基礎上,於特定的密閉反應器(高壓釜)中,採用有機溶劑作為反應體系,通過將反應體系加熱至一定溫度,在反應體系中產生高壓環境而進行無機合成與材料製備的一種有效的方法。反應時間和反應溫度是控制晶粒物相、線度及結晶完整性的重要參數;溶液的pH值則是影響晶粒粒度以及樣品分散性的重要參數;保護劑兼分散劑 PVP的加入,更有效地減少了團聚的形成。
機械球磨法合成 FeS2:在高能球磨過程中加入固態分散劑NaCl,得到了高分散的納米級FeS2晶粒。此外,固態分散劑NaCl的存在還促進了晶粒的形成和生長。
現階段人工合成FeS2的成本是阻礙其工業化的主要問題之一,而水熱法及溶劑法合成的FeS2由於其類似於天然FeS2礦石合成條件的獨特優勢,且工藝簡單,合成條件溫和,得到越來越多的關注。另一方面,FeS2具有優良的高溫電化學性能,因此Li/FeS2熱電池成為電動汽車最有吸引力的高能動力來源之一。
資源儲量
中國硫資源構成與世界硫資源相比有較大差別。在世界硫資源構成中,石油與天然氣中硫占較大比例,是硫的主要來源。與世界硫資源相比,中國石油多數為低硫油,酸性天然氣主要產於四川威遠一帶的氣田中,油氣中硫資源量合計占中國硫資源量的0.12%。而中國的硫鐵礦資源在世界上的豐富程度卻居首位,遙遙領先於世界其他所有國家;除單獨的硫鐵礦、伴生硫鐵礦外,煤系中的硫資源也主要是以硫鐵礦的形式存在,僅這三部分硫鐵礦資源量就占中國硫資源量的83.4%。我國硫鐵礦保有儲量達數十億噸,平均品位為18.28 %。硫鐵礦品位高於35 %的富礦僅占總儲量的4.5 %;絕大部分屬於含硫12~35 %的中低品位礦石,且含硫12~20 %的貧礦所占比重較大。著名的向山硫鐵礦的入選品位僅含硫10 %,因此大量被視作廢石的表外礦也被利用。著名產地還有廣東英德和雲浮、安徽馬鞍山、甘肅白銀廠等。
從中國硫儲量來看,硫儲量由硫鐵礦硫、伴生硫鐵礦硫和自然硫構成。而自然硫因採選技術尚處於試驗階段,短期內還難以開發利用。所以硫鐵礦和伴生硫鐵礦是中國當前以後相當一段時期的主要硫源。
毒理學數據
主要的刺激性影響
在皮膚上面:刺激皮膚和黏膜
在眼睛上面:刺激的影響
致敏作用:沒有已知的敏化現象
儲存方法
常溫密閉,陰涼通風乾燥
安全信息
危害:通常來說對水是無害的,若無政府許可,勿將材料排入周圍環境
安全術語:S26;S36;S37;S39
風險術語:S32;S36;S37;S38
危險品運輸編號:UN3178
危險類別:4.1
包裝等級:III
危險品標誌:易燃、刺激

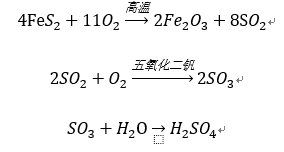 氧化反應生成三氧化二鐵、二氧化硫、硫酸反應方程式
氧化反應生成三氧化二鐵、二氧化硫、硫酸反應方程式 二硫化鐵立方晶型
二硫化鐵立方晶型 (a)陰陽離子配位形式; (b)立方晶系黃鐵礦; (c)斜方晶系白鐵礦
(a)陰陽離子配位形式; (b)立方晶系黃鐵礦; (c)斜方晶系白鐵礦
