基本介紹
- 中文名:硫酸鋁
- 英文名:Aluminium sulfate
- 別稱:硫酸鋁(3:2);明礬,硫酸鋁
- 化學式:Al2O12S3
- 分子量:342.15
- CAS登錄號:10043-01-3
- EINECS登錄號:233-135-0
- 熔點:770 °C (dec.)(lit.)
- 水溶性:soluble
- 密度:2.71 g/mL at 25 °C(lit.)
- 外觀:無味、白色、吸濕、有光澤的晶體或粉末。
- 套用:用於人造寶石和高級銨明礬的生產。
- 危險性符號:Xi,N
- 危險性描述:37/38-41-51/53-36/37/38
- 危險品運輸編號:UN 1760/3077
發現歷史,理化性質,物理性質,化學性質,計算化學數據,礦藏分布,製備方法,主要用途,鑑別試驗,注意事項,
發現歷史
中世紀,在歐洲有好幾家生產明礬的作坊。
16世紀,德國醫生兼自然科學歷史學家帕拉塞斯(Parace/sus PAT1949-1541)在鋁的歷史上寫下了新的一頁。他研究了許多物質和金屬,其中也包括明礬(硫酸鋁),證實它們是“某種礬土鹽”。這種礬土鹽的一種成份是當時還不知道的一種金屬氧化物,後來叫做氧化鋁。
1745年,德國化學家馬格拉夫終於能夠分離“礬土”了。這正是帕拉塞提到過的那種物質。
理化性質
物理性質
外觀與性狀:白色晶體,有甜味;
溶解性:溶於水,不溶於乙醇等。
工業品為灰白色片狀、粒狀或塊狀,因含低鐵鹽帶淡綠色,又因低價鐵鹽被氧化而使表面發黃。粗品為灰白色細晶結構多孔狀物。
極易溶於水,硫酸鋁在純硫酸中不能溶解(只是共存),在硫酸溶液中與硫酸共同溶解於水,所以硫酸鋁在硫酸中溶解度就是硫酸鋁在水中的溶解度。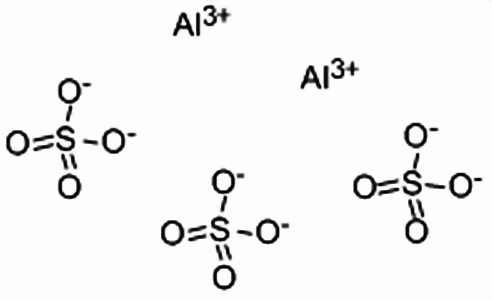 硫酸鋁化學結構式
硫酸鋁化學結構式
 硫酸鋁化學結構式
硫酸鋁化學結構式770℃分解為氧化鋁和三氧化硫。
有無水物和十八水合物。無水物為無色斜方晶系晶體。溶於水,水溶液顯酸性,微溶於乙醇。在水中的溶解度隨溫度的上升而增加。十八水合物(Al2·(SO4)3·18H2O)為無色單斜晶體。溶於水,不溶於乙醇。水溶液因水解而呈酸性。
相對密度(水=1):2.71
不同溫度(℃)時每100毫升水中的溶解克數:
31.2g/0℃ |
33.5g/10℃ |
36.4g/20℃ |
40.4g/30℃ |
45.8g/40℃ |
59.2g/60℃ |
73g/80℃ |
80.8g/90℃ |
89g/100℃ |
水中溶解度:
溫度(℃) | 溶解度(g) |
0 | 31.2 |
10 | 33.5 |
20 | 36.5 |
30 | 40.4 |
40 | 45.7 |
50 | 52.2 |
60 | 59.2 |
70 | 66.2 |
80 | 73.1 |
90 | 86.8 |
100 | 89.0 |
化學性質
不易風化而失去結晶水,比較穩定,加熱會失水,高溫會分解為氧化鋁和硫的氧化物。
水溶液呈酸性。水解後生成氫氧化鋁。水溶液長時間沸騰可生成鹼式硫酸鋁。無毒,粉塵能刺激眼睛。
水解產物有鹼式鹽和氫氧化鋁的膠狀沉澱。容易跟鉀、鈉、銨的鹽結合形成礬,如硫酸鋁鉀
kAl(SO4)2·12H2O。
加熱水合物時,猛烈膨脹,並變成海綿狀物,加熱至赤熱時,分解為三氧化硫和氧化鋁。
毒性:
ADI 未規定(FAO/WHO,2001)。
GRAS(FDA,§182.1125,2000)。
LD50:980±90 mg/kg(小鼠經口)
計算化學數據
1、疏水參數計算參考值(XlogP):未確定
2、氫鍵供體數量:0
3、氫鍵受體數量:8
4、可旋轉化學鍵數量:0
5、拓撲分子極性表面積(TPSA):161
6、重原子數量:12
7、表面電荷:0
8、複雜度:62.2
9、同位素原子數量:0
10、確定原子立構中心數量:0
11、不確定原子立構中心數量:0
12、確定化學鍵立構中心數量:0
13、不確定化學鍵立構中心數量:0
14、共價鍵單元數量:4
礦藏分布
明礬石,一種分布廣的造岩的硫酸鹽礦物,其含量超過K時稱鈉礬石或鈉明礬石,有時也有少量Fe3+代替Al3+。在火山岩例如流紋岩、粗面岩和安山岩內呈囊狀體或薄層產出,據認為它是由於這些岩石與逸出的含硫蒸氣進行化學反應形成的。 明礬石為中酸性火山噴出岩經過低溫熱液作用生成的蝕變產物。中國浙江蒼南、安徽廬山和福建福鼎的白堊系火山岩中都有大量產出。大的礦床在烏克蘭的別烈戈沃(Beregovo)附近、西班牙的阿爾梅利亞(Almeria)和澳大利亞新南威爾斯的布拉德拉(Bullah Delah)。
明礬石礦是浙江省的重要優勢礦種之一。探明資源儲量占全國總量的53%,居中國之首,主要分布在蒼南、平陽、瑞安三縣市,蕭山、鄞縣也有礦產地。
浙江省已探明資源儲量礦產地10處,其中蒼南礬山的雞籠山、水尾山,瑞安仙岩和蕭山岩山等4處為大型礦床;蒼南礬山的大崗山、瑞安平陽坑、鄞縣鳳凰山等3處為中型礦床。明礬石保有資源儲量9104萬噸(礦石量約2.25億噸)。
製備方法
硫酸法將鋁土礦粉碎至一定粒度,加人反應釜與硫酸反應,反應液經沉降,澄清液加入硫酸中和至中性或微鹼性,然後濃縮至115℃左右,經冷卻固化,粉碎製得成品。
化學反應方程式:

1.硫酸法:將鋁土礦粉碎至一定粒度.應釜與硫酸反應。由氫氧化鋁(或純的高嶺土或鋁礬土)與硫酸反應後,濾去不溶物再結晶而得。
2.將從酸性溶液中結晶生成的水合硫酸鋁晶體緩慢加熱,使其逐步脫水,最後將溫度升高到350℃,則完全脫水成為無水硫酸鋁。
主要用途
用作動物膠的有效交聯劑,並能提高動物膠的黏度。還用作脲醛膠黏劑的固化劑,20%水溶液固化速度較快。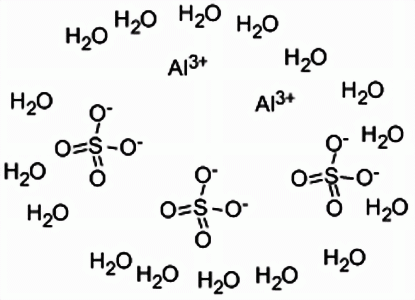 硫酸鋁化學結構式
硫酸鋁化學結構式
 硫酸鋁化學結構式
硫酸鋁化學結構式造紙工業中作為松香膠、蠟乳液等膠料的沉澱劑,水處理中作絮凝劑,還可作泡沫滅火器的內留劑,製造明礬、鋁白的原料,石油脫色、脫臭劑、某些藥物的原料等。還可製造人造寶石及高級銨明礬。砷含量不大於5mg/kg的產品可用於水處理絮凝劑。
1.造紙工業中用作紙張施膠劑,以增強紙張的抗水、防滲性能;
2.溶於水後能使水中的細小微粒和自然膠粒凝聚成大塊絮狀物,從而自水中除去,故用作供水和廢水的混凝劑;
6.白蛋白巴氏殺菌的穩定劑(包括液體或冷凍全蛋、蛋白或蛋黃);
7.可作原料,用於製造人造寶石和高級銨明礬,其他鋁酸鹽;
8.燃料工業中,在生產鉻黃和色淀染料時作沉澱劑,同時又起固色和填充劑作用。
淋洗對硫酸鋁改良蘇打鹽鹼土的輔助效果研究:該研究以松嫩平原中前郭地區中重度鹽鹼土為研究對象,採用實驗室模擬分析的形式,添加硫酸鋁改良後,再進行淋洗的效果進行了分析。分別選擇硫酸鋁的添加濃度為0%、0.2%、0.4%、0.6%、0.8%、1.0%、1.2%進行測定,研究了這七種情況在分別淋洗一次、兩次、三次後,土壤溶液中的主要離子濃度和變化趨勢,並對這七種濃度添加後的物理性質進行了測定。綜合各項試驗結果,得出以下結論。
淋洗有效改善了土壤的鹽化度。在硫酸鋁添加量一定的情況下,隨著淋洗次數的增加,硫酸根離子和氯離子等陰離子的濃度明顯下降。碳酸根和碳酸氫根也有明顯下降,但受空氣中二氧化碳的影響,下降速度並沒有硫酸根和氯離子快,但也明顯改善了土壤的離子結果,使土壤更適合作物生長。
淋洗有明顯的改善土壤化學成分的作用,但是添加入的硫酸鋁隨著淋洗也有大量的流逝,同時在震盪等作用下,第一次投入硫酸鋁形成的部分硫酸鋁水解膠體也被破壞,影響了硫酸鋁對土壤的改良效果。同時,淋洗震盪過程也破壞了土壤中原有的團聚體和微團聚體,多次淋洗使土壤的物理性質沒有改善,甚至在土壤溶液pH值方面產生負面效果。
當不淋洗土壤時,硫酸鋁的加入,有效改善了土壤性質,特別是對降低土壤鹼化度,效果明顯。土壤pH值、土壤容重、土壤顆粒粒徑等方面對土壤都有改善作用,並且效果明顯。鈣鎂等離子也隨著硫酸鋁的添加而被釋放出來,從一定程度上也起到了降低土壤鹽化度的作用。但單獨使用硫酸鋁改良,並不能全面的解決松嫩平原的土壤問題。由於土壤還有較高的鹽化度,硫酸鋁並沒有有效改善土壤的鹽化度問題,甚至添加硫酸鋁時土壤中鹽類物質的含量增加。因此,硫酸鋁只是將土壤類型從蘇打型轉化為硫酸型,問題被緩解,但是並未完全解決。
綜合硫酸鋁和淋洗這兩種改良方法的利弊,將兩種改良方式相結合,得到既可以改善土壤的鹼化度問題,也可以改善土壤的鹽化度問題,更好的改善土壤環境。在添加硫酸鋁為0.8%時,淋洗土壤兩次,研究人員指出可以取得最好的改善效果。
鑑別試驗
配10%試樣液,其鋁鹽(IT-2)和硫酸鹽(IT-29)試驗應呈陽性。溶解性極易溶於水,不溶於乙醇。按OT-42方法測定。5%水溶液的pH值2.9或以上,用玻璃電極測定。
含量分析:精確稱取試樣約4g,放入250ml容量瓶中,用水溶解並定容後混合。吸取該溶液10ml,放入250ml燒杯,加0.05mol/L的EDTA二鈉(乙二胺四乙酸二鈉)溶液25.0ml和pH 4.5的緩衝液(由77.1g醋酸銨和57ml冰醋酸加水定容至1000ml)20ml,文火煮沸5min。冷卻後,加乙醇.50ml和雙硫腙試液(TS-94)2ml。用0.05mol/L硫酸鋅液滴定至鮮明的玫紅色,同時進行空白滴定。每毫升0.05mol/L的EDTA二鈉(乙二胺四乙酸二鈉)相當於硫酸鋁Al2 (SO4)3的8.554mg或含水硫酸鋁16.66mg。
注意事項
燃爆危險:該品不燃,具刺激性。
健康危害:對眼睛、黏膜有一定的刺激作用。誤服大量硫酸鋁對口腔和胃產生刺激作用。
毒理學資料:小鼠經口LC50:6207mg/kg。
生態學資料:通常對水體是稍微有害的,不要將未稀釋或大量產品接觸地下水,水道或污水系統,未經政府許可勿將材料排入周圍環境。
皮膚接觸:脫去污染的衣著,用流動清水沖洗。
眼睛接觸:提起眼瞼,用流動清水或生理鹽水沖洗。就醫。
吸入:脫離現場至空氣新鮮處。如呼吸困難,給輸氧。就醫。
食入:飲足量溫水,催吐。就醫。
危險特性:未有特殊的燃燒爆炸特性。受高熱分解產生有毒的硫化物煙氣。
有害燃燒產物:自然分解產物未知。
滅火方法:消防人員必須穿全身防火防毒服,在上風向滅火。滅火時儘可能將容器從火場移至空曠處。
操作注意事項:密閉操作,局部排風。操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴自吸過濾式防塵口罩,戴化學安全防護眼鏡,穿防毒物滲透工作服,戴橡膠手套。避免產生粉塵。避免與氧化劑接觸。搬運時輕裝輕卸,防止包裝破損。配備泄漏應急處理設備。倒空的容器可能殘留有害物。
儲存注意事項:儲存於陰涼、通風的庫房。遠離火種、熱源。應與氧化劑分開存放,切忌混儲。儲區應備有合適的材料收容泄漏物。
儲運:起運時包裝要完整,裝載應穩妥。運輸過程中要確保容器不泄漏、不倒塌、不墜落、不損壞。嚴禁與氧化劑、食用化學品等混裝混運。運輸途中應防曝曬、雨淋,防高溫。車輛運輸完畢應進行徹底清掃。

