簡介
在過去幾十年中,隨著新的免疫學和分子生物學資料的獲得對霍奇金病(Hodgkin’s DiSease HD)認識進一步深入2種不同的淋巴瘤亞型被證實屬於這個範疇即經典型和結節性淋巴細胞為主型。大多數學者證實霍奇金病中腫瘤細胞(RS細胞)起自B淋巴細胞因此部分學者提出應將霍奇金病修正其名,稱為“霍奇金淋巴瘤”(Hodgkin’s lymphomaHL)。霍奇金淋巴瘤的定義為:霍奇金淋巴瘤是一種惡性淋巴瘤它在非腫瘤細胞的背景下含有特徵性RS細胞;並根據RS細胞的形態學和免疫表型及細胞背景的成分而區分亞型。1994年,國際淋巴瘤研究組由此提出了新的分型法作為修訂的歐美淋巴瘤分類法(REAL)的一部分;這些概念被歸入了WHO 2001年的淋巴細胞腫瘤的分型中。WHO分型中HL包括經典型霍奇金淋巴瘤(classical Hodgkin’s lymphoma)和結節性淋巴細胞為主型霍奇金淋巴瘤(Nodular lymphocytic predominance Hodgkin’s lymphoma)經典型霍奇金淋巴瘤又包括:結節硬化型(Nodular sclerosis)混合細胞型(mixed cellularity)、淋巴細胞削減型(lymphocytic depiction)和富於淋巴細胞的經典霍奇金淋巴瘤(lymphocyte-rich classical Hodgkin’s lymphoma)4種。
霍奇金淋巴瘤獨特的細胞組成和大多數其他的惡性腫瘤不同,它具有少量腫瘤細胞(Reed-Sternberg細胞和其變異型)及其典型的炎症背景由於惡性細胞即RS細胞和他們的變異型細胞通常占所有細胞的1%不到,這對研究帶來一定困難因此他們的性質一直是一個謎很多不同類型的細胞被假定為RS細胞的來源Reed在他原始的文獻中描述了RS細胞並推測RS細胞來源於“增生的(竇狀隙樣)內皮細胞”。最近套用顯微解剖分離單個的惡性細胞分子技術放大並分析他們的基因細胞的特性日益明確幾乎所有經典型霍奇金淋巴瘤和結節性淋巴細胞為主型霍奇金淋巴瘤患者的惡性細胞都顯示了單克隆B細胞起源。
Stein、
Hummel和
Chen概括了實驗室資料證實,RS細胞和淋巴細胞和(或)組織細胞均與生髮中心B細胞有關係在經典型霍奇金淋巴瘤,RS細胞可能由於重排的免疫球蛋白基因非翻譯區發生體細胞突變而不能合成免疫球蛋白在結節性淋巴細胞為主型霍奇金淋巴瘤免疫球蛋白的基因編碼區既完整並具有潛在的功能。
Peters於1950年制訂了本病的臨床分期方法,強調了解剖學對疾病的診斷性評估作用1952年,Kinmouth介紹了淋巴造影術,便於檢測盆腔和腹膜後淋巴結的病變在Stanford大學通過對65例病人剖腹和脾臟切除,對脾門主動脈旁和腸系膜淋巴結及肝臟活檢發現許多患者的脾臟頻繁受累這些診斷性操作提高了對疾病播散情況的了解以及與預後的關係有關內容被歸入1965年的Rye會議制訂的分期中,其進一步的修改是1971年Ann Arbor霍奇金病分期這一分期方法得到了廣泛的套用。此後,1989年和1993年又有了Cotswa分期和AJCC臨床分期,但均不及Ann Arbor普及。
Pusey(1902)和Senn(1903)率先套用Roentgen在1896年發現的X線檢查手段,報導了淋巴結病治療後的消退。鑒於幾乎所有的未治療區域都存在潛在的復發風險,1932年Gilbert建議淋巴瘤累及區和未累及區都應進行全身性治療Peters(1950)最早證實放射治療具有治癒性的療效。超高壓放射治療的發展, (Kalplan1962)使殺腫瘤的放射劑量(正常組織耐受範圍內)完全到達淋巴區域。目前在早期HL中單一放療的效果肯定也可與化療聯合。
HL的化療起源於戰爭時期芥氣工作的副產品。隨著對氮芥研究的進展一系列抗代謝藥物合成以及大量烷化劑和抗體從各種植物、真菌和微生物中提取出來DeVita和他的同事們率先套用高效聯合化療:“MOPP”(氮芥、長春新鹼丙卡巴肼潑尼松)方案,通過實驗性研究證實這些藥物無交叉毒性。之後米蘭研究所提出的ABVD方案被廣泛證明其療效優於MOPP方案從而取代MOPP方案成為晚期HL的金標準治療方案。聯合化療使進展期HL成為可治癒的疾病。
流行病學
1.分布 據流行病學調查霍奇金淋巴瘤(Hodgkin’s lymphomaHL)在世界各地的發病情況差異較大在歐美國家多發,占淋巴瘤的45%左右居淋巴瘤之首位而中國和日本發病率較低。1983年中國全國淋巴瘤協作組對9009例淋巴瘤回顧性資料分析結果,HL占8%與日本(7.6%)較接近。
2.年齡 HL確診時患者的中位年齡為26~31歲最初認為HL患者的第1個發病高峰為20~29歲,第2個發病高峰為60歲以上。現已明確第2個發病高峰源於錯誤的病理分型來自美國癌症研究院SEER(Surveillance,Epidemiology and End Results Program)的最新資料表明,上述錯誤分類的病例大部分為侵襲性非霍奇金淋巴瘤(non-Hodgkin’s lymphoma,NHL),而不是混合細胞型HL或淋巴細胞消減型HL。一般而言,結節硬化型(Nodular sclerosis,NS)最常見,70%以上的病例在40歲以下發病,無第二發病高峰。其他的組織學亞型如淋巴細胞為主型(lymphocytic predominanceLP),混合細胞型(mixed cellularityMC)和淋巴細胞消減型(lymphocytic depletion,LD)發病率較低但是隨著年齡增加發病率逐步增高。
3.性別 男性HL的發病率約為女性的1.4倍。男性發病高於女性主要見於小於10歲的兒童以及50多歲的老年人10歲和40歲之間的年齡段女性發病占主要地位,因為這一年齡段是NSHL的發病高峰而女性NSHL比男性NSHL更多見。
4.種族 HL主要是美國白色人種的惡性腫瘤,在所有HL病例中白色人種占90%以上。
5.風險因素 HL的病因仍不清楚現在認為與遺傳傾向(genetic susceptibility)和感染有關尤其是EB病毒感染與HL發病密切相關目前的流行病學資料都支持上述兩種病因,但是遺傳傾向和感染引起的HL亞型不同。
(1)感染因素:
①EB病毒感染:在開發中國家大部分HL病例為EBV陽性在已開發國家大約有40%~50%的HL病例與EBV感染有關這些病例主要為兒童和老年人,而在青年結節硬化型HL患者中較少見。例如,在肯亞(Kenya),100%的兒童病例為EBV潛在膜蛋白-1(Latent Membrane Protein-1LMP-1)陽性,其中的25例具有Ⅰ型和(或)Ⅱ型EBV病毒在這一研究中,只有63%的肯亞成年人為LMP-1陽性最近對1546例HL病例進行流行病學分析發現混合細胞型比結節硬化型,兒童比青年人男性比女性西班牙人(Hispanics)比白人的EBV陽性率顯著高。
2000年,美國的HL新發病人數約為7500,從20世紀70年代以來降低了16%左右在日本,對1955~1999年之間HL的EBV陽性率進行研究發現,隨著時間發展,EBV的總陽性率逐漸降低,1955~1969年為52%(23例中12例),1970~1984年為46%(39例中18例)1985~1999年為35%(44例中13例)。有趣的是,結節硬化型的EBV陽性率顯著降低,1955~1969年為45%,1970~1984年為21%1985~1999年為4%而其他經典型HL並不顯著降低,3個年段分別為63%,78%,67%。EBV的陽性率在一定程度上受到社會-經濟狀態和種族-遺傳背景的影響。在過去幾十年中,日本的生活水平有了顯著提高生活方式也發生了很大改變,從傳統型轉變為西方式。因此,在非工業化國家和工業化早期國家隨著工業化進展HL的EBV陽性率可能會降低。
當EBV存在於HL患者時在所有的腫瘤細胞中都可檢測到單克隆EBV基因組。但並非所有的HL患者EBV都為陽性而EBV病毒在淋巴系惡性腫瘤中所起的作用是什麼這些都有待進一步研究。
②HIV:HL是發生於HIV陽性人群的最常見的AIDS相關腫瘤,在HIV感染的患者中HL的發生率約增高7倍左右。目前已報導了300多例HIV感染的HL病例主要為歐洲國家(如義大利西班牙和法國),美國較少亞洲國家如日本和中國更少見。在HIV感染的患者中HL發病風險增高而且這一人群中HL的組織學類型、生物學行為以及預後與其他非HIV感染的HL患者有很大不同。HIV陽性且患有晚期HL的患者常具有結外病變。這些患者的預後因素常與HIV有關而不是HL。與非HIV感染的HL患者相比HIV感染的HL患者對化療的反應率較低、復發率更高感染性併發症更多見,總生存率更低而且與非HIV感染的HL不同大部分HIV相關HL病例中EBV為陽性(占80%~90%)。RS細胞(Reed-Sternberg cell)中EBV的LMP-1高度表達LMP-1作為持續被激活的腫瘤壞死因子受體樣分子發揮作用,導致促進細胞激活生長和生存的信號途徑被激活最終形成上述HIV相關HL特有的不良特徵。
(2)遺傳傾向:對雙胞胎進行研究證實,同卵雙胞胎比異卵雙胞胎的HL發病風險顯著高。但是一般而言,在所有HL患者中,家族性HL的發病率不到5%回顧性分析328例家族性HL患者發現,發病高峰為15~34歲而散發的HL發病年齡曲線較寬對60例各個家族中的HL患者進行研究未發現同一家族中所有患者的腫瘤組織中都存在EBV或EBV血清學陽性,而且10對同卵雙胞胎中只有1對同時為EBV陽性。這些資料表明EBV對家族性HL的發病不起主要作用。
(3)其他:其他風險因素還有接觸除莠劑和某些職業如木工家畜飼養和肉類加工。另外HL的發病還受社會經濟狀況的影響,那些出身於高階層家庭受過高等教育或小型家庭的人患HL的危險性增高在經濟比較落後的國家和地區,兒童和青年人HL發病率也高於經濟較發達的國家和地區。
病因
1.EBV HL是少數幾種流行病學傾向於感染為病因的惡性腫瘤之一.早期認為HL發病可能與EBV感染有關,這是由於一些研究證明有單核細胞增多症病史的病人HL復發風險增高,以及HL病人EBV抗原的滴度增高儘管長期以來對流行病學和血清學資料有所懷疑但一直到1987年Weiss等套用Southern blot方法才證實霍奇金淋巴瘤中存在EBV基因組,證明EBV與較多經典HL有關。目前,套用高度敏感的原位雜交技術18%~50%的霍奇金淋巴瘤為EBV(+)此外套用直接抗EBV探針檢測顯示一些霍奇金淋巴瘤組織樣本中很明顯存在EBV附加體DNA,提示EBV感染髮生於腫瘤細胞克隆性擴增之前。EBV(+)的惡性細胞表達病毒潛在膜蛋白(LMP1),此蛋白可防止B細胞凋亡(通過誘導Bcl-2可介導此效應發生)這一證據進一步證明EBV對霍奇金淋巴瘤發病起著積極的作用,轉基因動物模型實驗證明病毒潛在膜蛋白具有致癌作用。再有LMP1可上調很多細胞基因,包括CD23CD39、CD40和MHCⅡ類分子及細胞黏附分子如LFA-1LFA-3和ICAM-1。EBV基因組的檢測與混合細胞型霍奇金淋巴瘤有關有研究發現,在混合細胞型中EB病毒陽性病例的比例(58%)比結節硬化型(18%P<0.001)顯著增高。有關EB病毒感染的病因學說由於RS細胞中分離出EB病毒基因組而進一步得到證實。最近,有報導認為CD99下調是霍奇金-RS細胞產生的基本要求。而EBV潛在膜蛋白(LMP-1)的高表達可導致CD99下調,前者在EBV相關性霍奇金淋巴瘤的霍奇金-RS細胞中是高表達的。表明EBV LMP-1蛋白在CD99轉錄調節下調中起著重要作用,導致霍奇金-RS細胞的發生但EB病毒不能解釋所有的病例尤其是已開發國家中最常見的類型——結節硬化型在美國和歐洲,大部分HL與EBV無關,尤其是青年人,只有20%是EBV HRS+Deleclue等分析了一例復發HL病例原發腫瘤為EBV HRS+,但復發標本為EBV HRS-推測在疾病進展過程中病毒丟失,但無正式證據證明原發腫瘤和復發腫瘤克隆是一致的而且,此病人發病時僅5歲,因此不能代表典型青年人群體很清楚有些HL病例是EBV血清學陰性的因此EBV並不是所有病例的病因。
2.其他感染因素 在非EBV相關性病例中較為可能的病因是其他感染因素。皰疹病毒在自然界中分布廣泛可能與HL的發病有關最近,有研究顯示人類皰疹病毒-6(human herpesvinus-6,HHV-6)基因組整合至宿主淋巴細胞的DNA中而且HL病人HHV-6抗體滴度增高與老年人相比,抗體滴度在青年人中更高,在EBV HRS-病例中比EBV HRS+病例高。HHV-8是人類皰疹病毒家族中最新發現的病毒,雖然EBV和HHV-8之間基本無同源序列但有一些功能特徵相同EBV能上調許多細胞基因,而這些基因與HHV-8基因組有同源性但目前尚無證據表明HHV-8與HL發病有關。
多瘤病毒JC一直被認為與急性淋巴母細胞白血病的發病有關而此病與青年型HL在流行病學上有許多共同特徵。曾有人在HL中檢測SV40或親淋巴乳多空病毒,未得到陽性結果。套用PCR技術46例HL中檢測JC和BK未發現病毒基因組。其他研究也不支持腺病毒5和12人類T細胞淋巴瘤病毒ⅠⅡ或人反轉錄病毒5。
發病機制
1.基因異常 絕大多數經典霍奇金淋巴瘤患者伴有克隆性細胞遺傳學異常這種異常隨不同病例而不同且克隆內異常也為異質性,提示染色體不穩定許多病例顯示14q異常,類似B細胞性淋巴瘤但很少發生t(14;18)的異常。2個研究組套用螢光原位雜交技術(伴或不伴螢光免疫分型)發現所有霍奇金淋巴瘤病例的RS細胞顯示克隆數值異常。早期報導中約1/3的霍奇金淋巴瘤中發現Bcl-2重排但其他實驗室未檢測到Bcl-2重排而且在高反應性組織中如反應性扁桃體中也發現Bcl-2重排與EBV有關的轉化蛋白能夠上調培養細胞中的Bcl-2這一證據進一步表明Bcl-2表達與霍奇金淋巴瘤之間的關係。Bcl-2過度表達的免疫組化研究得到的結論並不一致。但是,Bcl-2表達似乎與組織學、EBV(+)或t(14;18)易位無關,Bcl-2表達的增強可能存在於背景細胞並且對霍奇金淋巴瘤的發病不起重要作用。但一個研究組套用細胞遺傳學分析法,明確證實了腫瘤細胞存在Bcl-2重排,而不發生t(14;18)。最近在霍奇金淋巴瘤中發現新的凋亡抑制因子Bcl-X(L),94%的霍奇金淋巴瘤中Bcl-X(L)為陽性,且大多數RS細胞為高強度表達。在非霍奇金淋巴瘤中表達率低(<20%),但網狀中心淋巴瘤除外。故推測Bcl-X(L)在RS中的異常表達對於凋亡的抑制可能是霍奇金淋巴瘤的發病原因未發現Bcl-X(L)與EBV表達存在相關性經免疫組化分析,在CD30+ 的霍奇金和其他淋巴瘤中已檢測到P53抑癌基因表達但是最近的研究發現,在8例霍奇金淋巴瘤中霍奇金和RS細胞都無P53突變。
最近,Humboldt等報導,從HL病人淋巴結活檢樣本中IκBα mRNA在HRS細胞中過度表達並檢測到IκBα基因突變,產生C端截斷的蛋白質推測此蛋白質不能抑制NF-κB-DNA結合活性,而防止HRS細胞凋亡,並引發增殖因此與HL發病有關。
NLPHL的細胞遺傳學資料很少而且細胞遺傳學異常的研究結果也不一致Tilly等報導的大系列HL中,只有1例NLPHL,此例NLPHL具有46XY核型。Hansmann等報導了一例高二倍體NLPHL,6q-+21,及幾個未明確的標誌研究發現,起源於NLPHL的DEV細胞系列具有下述核型異常:48,XXYt(3;14)(3;22)t(3;7)del3-2+12+mar分析HL的倍體情況,5例NLPHL中3例為非整倍體未檢測到四倍體,而四倍體常見於經典HLBcl-2基因重排只在一小部分病例中檢測到,套用免疫組化檢測Bcl-2蛋白表達,陽性病例數很少。據此推測,Bcl-2轉位可能對NLPHL發病不起重要作用。
2.HL患者腫瘤細胞的起源 長期以來一直認為HL中不同組織學類型代表同一疾病的形態學變異其中HRS細胞處於反應性背景中而每一組織亞型均有特徵性細胞組成在過去20年中人們逐漸發現上述概念只是部分正確如結節性淋巴細胞為主型HL與HL的其他類型不同是不同的生物學疾病。
(1)經典HL中HRS的細胞起源:最早有關HRS表達Ig的免疫組化研究如1974年Garvin等及隨後Taylor等他們的研究證實在HL活檢標本中可獲得HRS表達IgG的結果表明HRS起源於產生Ig的B細胞,但是其他免疫組化研究顯示HRS起源於非淋巴系細胞其後直到單克隆抗體技術的套用發現了CD30分子證明經典HL的HRS選擇性表達CD30,而正常個體只在一些活化的淋巴母細胞中表達。這一資料首次證明HRS為淋巴細胞起源。基因水平研究表明HRS發生克隆性Ig基因重排在Rajewsk系列中13例HL中檢測到12例stein也報導25例中檢測到24例發生重排證明95%的HLs為B細胞起源。序列分析證明在重排的V區具有高負荷的體細胞突變。由於一些經典HLs的HRS細胞表達一或多個T細胞抗原以及40%的HL中的細胞系列具有T細胞表型和基因型,故推測剩餘的5%經典HL起源於轉化的T細胞。但由於在HRS細胞中還未檢測到重排的TCR基因這一推測無法證實最近的研究發現經典HL起源於生髮中心B細胞而不是生髮中心後B細胞;B細胞系子代可發生兩種獨立的轉化,一種形成HRS細胞,另一種形成NHL;產生HL的轉化完全改變了普通祖細胞的形態學和免疫表型(不表達CD20、CDl0Bcl-6和IgM並下調突變機制,表達CD30和CDl5)而轉化為NHL的細胞或多或少保留了B細胞系祖先的特徵某一特定病例中的HRS細胞群體完全起源於單個轉化細胞,並克隆增殖。WHO(2001)分類中認為結節性淋巴細胞為主型霍奇金淋巴瘤起自生髮中心母細胞分化階段的B細胞,而經典型霍奇金淋巴瘤98%起自生髮中心分化階段中的成熟B細胞。
(2)NLPHL中淋巴細胞和(或)組織細胞(H和L)的細胞起源:淋巴細胞為主型HL,是特徵性的腫瘤細胞[淋巴細胞和(或)組織細胞]的亞型與進行性轉化的生髮中心的巨大結節有關免疫組化研究表明(H和L)細胞是B細胞系列因為它們表達大量B細胞標誌包括CD19CD20CD22,CD79a和J鏈且最近的分子學研究也提示:H和L細胞是轉化的中心母細胞在主要的克隆群體中,免疫球蛋白重鏈持續發生體細胞高突變在已開發國家EBV很少與H和L細胞有關聯,可能與本病發病無關H和L細胞常被CD3+CD4+、CD57+CD40、L-的T細胞圍繞,但此T細胞玫瑰花結的意義尚不清楚NLPHL可能與大細胞淋巴瘤共同發生或轉為大B細胞淋巴瘤大量研究表明至少在一些病例中,B-DLCL和NLPHL在克隆上存在相關性。NLPHL也可具有與富組織細胞B細胞淋巴瘤(HRBCL)相似的結節或大塊區域至少某些HRBCL病例起源於NLPHL。富T細胞B細胞淋巴瘤(TCRBCL)也可能存在上述情況。有關NLPHL細胞基因方面的資料很少,且各研究組所報導的細胞基因異常也不一致。
3.細胞因子 霍奇金淋巴瘤的主要組織學特徵為:相當數量的膠原硬化炎症細胞和惡性RS細胞而RS細胞及背景細胞產生的細胞因子導致了各業型上的區別在這些細胞之間有複雜的旁分泌和自分泌作用RS細胞和反應性細胞產生的各種細胞因子既影響RS細胞又影響周圍細胞環境例如,轉化生長因子-β1,(TGF-β1)mRNA在結節型霍奇金淋巴瘤的嗜酸性粒細胞中已被測到。儘管TGF-β1的作用決定於它與其他因子和靶細胞的相互作用,但它可以刺激成纖維細胞增生並產生膠原可能對膠原的形成起著重要的作用後者是結節型霍奇金淋巴瘤的特徵。對本病的發病起重要作用的另一細胞因子是IL-5IL-5是嗜酸性粒細胞的生長因子而嗜酸性粒細胞在一些霍奇金淋巴瘤中是主要的背景細胞在RS細胞中也發現了IL-5mRNA此外RS也分泌IL-1,IL-9腫瘤壞死因子-α粒細胞-巨噬細胞克隆刺激因子和巨嗜細胞刺激因子。IL-6存在於10%~60%的RS細胞中,它可誘導漿細胞增生並能促進淋巴細胞增生和成熟。霍奇金淋巴瘤的不同組織學特徵可能是RS和反應性背景細胞如T淋巴細胞組織細胞和嗜酸性細胞分泌的多種細胞因子網路的結果。
臨床表現
HD為主要侵犯淋巴系統的惡性疾病,由於病變侵犯部位的不同其臨床表現亦各異。
1.初發症狀與腫瘤首侵部位 表1所示具有單一初發症狀的504例患者中(同時有2或3個首發症狀未統計在內)以表淺淋巴結腫大為首發症狀者占絕大部分(75%),其中頸淋巴結腫大占多數;腹部症狀表現為腹痛、腹部腫塊;胸部症狀有胸悶胸痛咳嗽氣短和胸部腫物;頭頸部症狀有咽痛、扁桃體腫大和鼻塞等;周身症狀主要表現為發熱腫瘤的首侵部位見表2,絕大多數為表淺淋巴結,腹腔淋巴結包括腸系膜和腹膜後淋巴結還有縱隔淋巴結。HD首發結外受侵較少主要為小腸、胃和咽淋巴環。
2.周身症狀 包括發熱、盜汗和體重減輕,其次是皮膚瘙癢和乏力就診時伴有周身症狀者較多(55%)出現周身症狀是預後不佳的表現。HD的發熱較常見,並有一定特點約有1/6的HD患者可出現這種周期性發熱。其發熱特點是在數天逐漸上升,體溫在38~40℃持續數天然後逐漸下降至正常。經過10天~6周或更長的時間間歇期,體溫又開始上升如此周而復始,反覆出現並逐漸縮短間歇期。
皮膚瘙癢亦是HD較為常見的一種症狀,由局部可逐漸發展至全身開始輕度皮癢,可使表皮脫落,皮膚增厚,嚴重瘙癢,可抓破皮膚,引起感染和皮膚色素沉著另一特殊症狀為飲酒痛,即飲酒後引起腫瘤部位疼痛,表現在酒後數分鐘至幾小時內發生。
3.淋巴結腫大 是HD最常見的臨床表現其中表淺淋巴結腫大最為常見在首侵腫瘤部位中占86%,如加上腹腔和胸腔淋巴結腫大,則占首侵部位的92%,(表2)。此結果與國外資料相似HD侵犯淋巴結占9l%,結外受侵占9%表淺淋巴結腫大較易發現和診斷,但初期亦易誤診為淋巴結炎或淋巴結結核主要以頸部淋巴結腫大最多,其次為腋下和腹股溝淋巴結,其他還有頜下、耳前、耳後、頦下枕部滑車上和膕窩等淋巴結腫大則較少。
縱隔淋巴結腫大,包括肺門淋巴結腫大。在首侵腫瘤中僅占2%(表2),但在就診時侵犯縱隔較多見常為兩側,多個淋巴結腫大,可以壓迫上腔靜脈,引起上腔靜脈壓迫綜合徵也可壓迫食管和氣管引起吞咽受阻和呼吸困難。引起喉返神經麻痹者少見,但肺癌縱隔淋巴結轉移引起聲帶麻痹則較常見,此點可作鑑別診斷時參考。
腹腔淋巴結腫大包括腸系膜、腹膜後和盆腔淋巴結腫大腫瘤增大時可擠壓胃腸道引起腸梗阻,壓迫輸尿管可引起腎盂積水甚至產生尿毒症。
4.咽淋巴環 包括扁桃體鼻咽部和舌根部在HD首侵部位中占3%(表2)腫物增大時可影響進食和呼吸或出現鼻塞,觸之腫物有一定硬度,並常伴有頸部淋巴結腫大抗炎治療無效時,應儘早作腫物活檢以確定診斷。
5.脾臟腫大 脾大較常見屍檢時發生率更高Rosenberg(1972)報導53例Ⅲ期患者,43例(8l%)有脾臟受侵但原發於脾的HD則少見。臨床表現為巨大脾臟質地較硬可有結節,此時較易診斷。在臨床觸診脾臟腫大時則不能輕易診為脾首侵而檢查脾臟不大,也不能完全排除脾首侵。
6.肝臟腫大 臨床檢查肝受侵者較脾少見因肝受侵病變常為瀰漫性的,肝CT檢查常不易診斷有時可顯示有占位病變,經肝穿刺活檢或剖腹探可確診,但在屍檢中的發生率並不少見臨床表現為肝臟瀰漫性腫大質地中等硬度少數可捫及結節肝功檢查多正常。
7.胃腸道病變 在ML的結外病變中以小腸和胃較常見其他還有食管、結腸、直腸,還可侵犯胰腺,但均罕見原發於胃腸道的HD較NHL少見。
8.胸腔內病變 除縱隔、肺門淋巴結腫大外,還可侵犯胸膜和心包膜,產生胸腔積液和心包積液。肺受侵可出現大片浸潤或肺內結節病變,由於支氣管黏膜病變也可阻塞支氣管,引起肺不張。心臟受侵甚罕見。
9.神經系統病變 多發生在晚期,主要為腦內病變和脊髓侵犯和脊髓受壓表現HD中較少見。
10.泌尿生殖系統病變 HD較NHL少見,HD的腎臟侵犯占13%。腎臟受侵多為雙側浸潤性病變或多發性小結節也可為孤立性較大腫塊,腎廣泛浸潤可引起尿毒症。但臨床甚少見原發於膀胱病變也很少見生殖系統亦可發生於睪丸。
11.骨病變 骨病變骨侵犯常在屍檢時發現,發生率可達45%~60%。Shanks等(1971)收集1525例生存患者中骨侵犯占13.9%骨侵犯的臨床表現首先為固定部位的局部疼痛和壓痛有報導骨侵犯108例中,72例為多發,36例為單發,其中8例由淋巴結直接侵犯主要侵犯的部位為胸椎腰椎肋骨其次為骨盆股骨和頸椎等產生骨膜反應的較多尤其是長骨。骨病變的性質可為溶骨性(75.4%)硬化性(13.6%)或兩者兼有(5.2%)。
12.皮膚病變 局部或全身皮膚瘙癢是HD的常見症狀,一般在瘙癢處皮膚並無明顯病變,有人認為是疾病活動的指征。皮膚和皮下的繼發病變常發生於疾病晚期。非特異性皮膚表現,以帶狀皰疹較常見,這可能與HD患者免疫功能低下,易受病毒感染有關原發性皮膚的ML為蕈樣肉芽腫(mycosis fungoides)。
13.骨髓侵犯 多見於NHL,而HD甚少見。報導HD合併急性白血病有34例包括急性粒單核細胞型原粒細胞型單核細胞型幹細胞型和里-施細胞型白血病。大多數患者的骨髓穿刺塗片檢查結果均在正常範圍少數出現粒細胞系明顯增生,粒/紅比值高,反映中性粒細胞產生增多和(或)紅細胞系產生減少里-施細胞只發現於個別病例。
14.其他病變 可侵犯胸腺、乳腺和甲狀腺等,均甚少見。
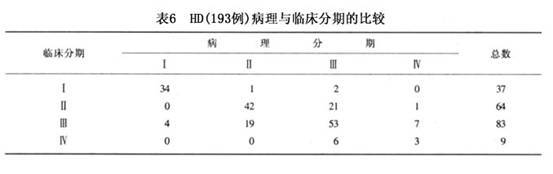
分期標準:Dorothy Reed(1902)將霍奇金病(HD)分為兩期。無全身性症狀為Ⅰ期,出現進行性衰弱、惡病質發熱、貧血等為Ⅱ期。Peters(1950)根據淋巴結區受侵的範圍將HD分為3期,所有結外侵犯均屬於Ⅲ期每期又根據全身症狀的有無分為“B”“A”1965年的Rye會議將HD分為4期,所有結外侵犯均屬於Ⅳ期。表3是HD的Ann Arbor會議(1971)的分期系統至今仍沿用未變。
併發症
最常見的併發症主要見於感染、發熱見於中樞神經系統感染如新型隱球菌感染;也可發生血源性化膿性腦膜炎或腦腫瘤。胸悶、胸痛、咳嗽氣短吞咽受阻、呼吸困難腹痛腸梗阻、腎盂積水尿毒症、黃疸、腹水肝硬化、貧血、神經系統病變、脊髓壓迫症狀腦出血等。這些既是HD的臨床表現,亦是它的併發症。
診斷
1.確診主要依賴病變淋巴結或腫塊的病理活檢檢查 值得注意的是淋巴結或結外淋巴組織的組織學診斷也常有困難有些有經驗的病理學家認為,誤診率可達25%因此對疑難病例有時也要參考臨床表現及發展的經過此時應由臨床醫師與病理學家共同進行討論可能有助於提高確診率。表6
2.分期 對分期方法的完整了解,對於指導完成有效而全面的有關診斷方面的檢查工作至關重要作為分期所進行的各種實驗室檢驗必須因人而異地選用,而不是不加考慮地完成。目前在早期HL常規分期中建議套用的方法概括於下表7中,除了診斷性研究外,還應當測定全血細胞計數、血清生化和紅細胞沉降率(ESR)歐洲和加拿大研究中已將ESR作為早期HL的重要預後指標值得注意的是,骨髓活檢檢出率很低所以在具有正常血細胞計數的無症狀早期病人在一般不行骨髓活檢。
在霍奇金病的每一期中,存在一組根據其病變部位、瘤塊大小和症狀的輕重而具有預後較好或更差的患者。目前常用的霍奇金淋巴瘤分期方法是1971年在Ann Arbor會議上通過的標準(表8)Ann Arbor分類法中規定的這些與預後有關的因素以及分期中的亞類所具有的重要性已越來越多地被人們所認識,因為治療的方法現在是根據每位患者的臨床情況而有針對性地選用在有關E類病損和ⅢA期的患者的預後和治療意義上存在不同意見例如,病理分期屬ⅢA可被進一步分為:①預後良好的腹部病變只限於上腹部淋巴結和(或)脾臟的Ⅲ1組;②預後略差者;其病變已延及下腹部中包括腹主動脈旁、髂窩或腹股溝等處淋巴結的Ⅲ2組。
非常局限的結外淋巴樣細胞惡變,或延及鄰近組織但仍在主要淋巴聚集地附近,用E表示。Ⅳ期病變指結外器官瀰漫受侵,如肝臟。如果有一個或多個淋巴系統以外的器官受侵的病理證據,則用以器官的代表字母並註明(+)表示。S代表脾臟,骨髓(M)肺實質(L)、胸膜(P)肝臟(H)、骨髓(O)、皮膚(D)等,分別以相應字母註明。
1989年Cotswald淋巴細胞消減型會議將Ann Arbor分期予以補充修改,此分期更明確地指出在任何一期中腫瘤負荷與預後的影響。如果治療後有殘餘又不能區分是良性還是惡性則用Cru標記。此分期主要用於HD非霍奇金淋巴瘤也可參考套用1991年建議使用的Cotswald分期系統(表9)與Ann Arbor相同也分為4期。然而Cotswald分期作了許多修改如Ⅲ期中的解剖分期。Cotswald分期中Ⅰ期和Ⅱ期與Ann Arbor相同Ⅲ期病變累及橫膈兩側淋巴結,根據解剖部位進一步分亞組。病變處於Ⅲ期局限於上腹部包括脾臟脾門淋巴結、腹腔淋巴結、肝門淋巴結則定為Ⅲ1期。病變處於Ⅲ期腹腔淋巴結累及包括腹主動脈旁髂部或腹股溝淋巴結為Ⅲ2期。內臟受累為Ⅳ期病變如肺、肝或骨髓侵犯等而非病變淋巴結的直接蔓延來自於病變淋巴結的直接蔓延,如縱隔腫塊直接擴散蔓延至肺定為ⅡE期。A或B症狀定義同Ann Arbor分期。
大腫塊為縱隔腫塊大於胸腔直徑1/3以上,或任何淋巴結腫塊最大直徑>10cm以上以X表示。CS和PS分別指臨床分期和病理分期。美國癌症聯合會1993年對HL進行了臨床分期(表10)。
分期的各項檢查及意義:
(1)常規檢查項目:
①病史與體檢:活體組織標本的檢查與複審
②實驗室檢查:血細胞計數血沉尿素氮尿酸,電解質,肝功能測定;骨髓液抽吸與活檢;血清乳酸脫氫酶(LDH)及β2-微球蛋白水平;腦脊液檢查常規及塗片找惡性細胞;人免疫缺陷病毒(HIV)、EB病毒血清學檢查;如果有胸腔積液腹腔積液、心包腔積液則予穿刺抽液查常規並塗片查腫瘤細胞;分子生物學檢測,如PCR擴增、流式細胞儀檢測以斷定病變是單克隆還是多克隆以及分析DNA的質與量。
③腹部和盆腔B超聲檢查:B超聲檢查的優點與不足與CT掃描類似但其特殊優點是沒有放射線的危害,可經常反覆使用。另外對腔內積液者可以用B超定位尤其包裹性積液定位後能為臨床醫師指示最佳穿刺部位。
④放射學檢查:胸部攝影,胸正側位片仍為一種最基本和常用的檢查方法。可發現較明顯的縱隔、肺門淋巴結腫大和肺部及胸膜病變。側位片對於發現隆突下和內乳淋巴結較有幫助,當縱隔淋巴結病變較大時,側位片亦可對其在前中縱隔的分布有一估計並觀察氣管是否有受壓移位;靜脈尿道造影;CT掃描為淋巴瘤分期的首選影像方法包括頸部胸部腹部與盆腔的CT掃描;磁共振檢查磁共振成像(MRI)的診斷價值與CT類似,其比CT掃描的優點是只需接受放射線,對骨骼及顱腦的影像較CT掃描清晰而對內臟器官的效果則不如CT當患者對碘造影劑過敏時MRI不僅容易鑑別淋巴結與血管還能同時檢出肝脾、腎、胰腺等實質器官的受侵而且在骨髓異常信號區活檢以提高陽性率等方面有套用前景。
⑤必要時檢查項目:剖腹探查淋巴結與肝臟活檢,脾臟切除;骨骼放射攝影,放射性核素骨顯像;正電子發射斷層掃描(C-PET),可全身立體成像,不易遺漏病灶。
(2)淋巴檢查:淋巴造影可以顯示淋巴結的內部結構有利於發現未增大的病變淋巴結並能鑑別腫瘤或良性病變所致淋巴結腫大但顯示範圍局限有些淋巴結不能顯影不能顯示內臟。胸腹部CT掃描顯示病變範圍全面能顯示淋巴造影不能顯示的淋巴結組與內臟但不能觀察內部結構,只能以大小或密度辨別正常或異常。
(3)剖腹探查在分期中的價值:能了解較小病灶與病變性質;增加對病程發展與擴展方式的了解;脾切除便於以後的放療減少左側放療併發症。但手術本身有一定的併發症,甚至導致死亡。脾切除影響機體的免疫功能對Ⅵ期患者的必要性不大但近10多年來由於診斷技術的進展,可以用CT、MRIB超聲等檢查了解深部臟器及淋巴結情況,剖腹探查分期已顯得不那么重要了。剖腹探查分期同時切脾對病人有一定損害手術死亡率約為0.1%也有報導更高的死亡率此外有一些合併症如感染、膈下膿腫、肺栓塞、胃腸道出血潰瘍肺炎等,所以剖腹探查手術應持慎重態度。
(4)肝臟活檢:HD肝侵犯通常見於以下患者:淋巴造影時部位較高的主動脈旁淋巴結陽性,脾腫大的患者病理為淋巴細胞削減型或混合細胞型這些患者應作肝臟活檢經皮肝臟穿刺能發現20%左右患者有肝侵犯肝穿刺陽性再作腹腔鏡檢查可增加10%的陽性率腹腔鏡能在直視下作多次針吸活檢。此外腹腔鏡也能看到胃腸系膜、脾與脾門的病變併發症比剖腹探查術低,對肝侵犯的診斷率不亞於剖腹探查術。
(5)核素67Ga掃描:鎵能被存活的腫瘤細胞攝取,鎵的攝取量取決於組織學上的惡性程度和病變是否活動據報導對於胸部的活動期病變,敏感性特異性和準確性可超過90%。對於腹部病變因為鎵從腸道排泄故可靠性較差對腹膜後淋巴結的敏感性為10%~60%掃描前靜脈注射67Ga 148MBq(4mCi),注射後72h內完成掃描為了清潔腸道掃描前一天晚上與當天清晨口服瀉藥主要用於鑑別治療後纖維變與腫瘤殘存或復發。
鑑別診斷
有兩類淋巴瘤:即富T細胞/組織細胞性大B細胞性淋巴瘤(T/HRL-BCL)和T細胞ALCL被發現與HL有明顯的形態學上的重疊,從而引起鑑別診斷上的困難其次伴有間變性細胞學的DLBCLs可能難以與Ⅱ期LDHI或NSHL相鑑別。
1.富T細胞/組織細胞性大B細胞性淋巴瘤(T/HRLBCL) 在過去幾年中,幾個研究組報導了與瀰漫性LPHL或MCHL形態學特徵相近的一種少見的淋巴瘤以小T淋巴細胞和表達B細胞抗原的分散的大腫瘤細胞為主典型病人表現為進展性病程預後差這些病例現被命名為富組織細胞或富T細胞性大B細胞性淋巴瘤。T/HRLBCL究竟構成一個獨特的疾病或僅僅是NLPHL的一個進展性變異型尚不明確但由於它具有進展性臨床病程所以應與NLPHL或經典HL區分。
T/HRLBCL是一種瀰漫性腫瘤。具有富淋巴細胞性背景,伴有類上皮樣組織細胞小簇和分散的大單核細胞,提示為LP或經典HL這種大細胞可類似於爆米花樣細胞免疫細胞和中心母細胞或三者都相似。
腫瘤細胞表達CD20和其他全B抗原胞質輕鏈可表達也可不表達採用Southern雜交印跡方法或全切片PCR技術可檢測到免疫球蛋白基因重組。但也可能檢測(-)類似NLPHL它們常為EMA+,但CD15-CD30- 和EBV-。背景淋巴細胞為CD57- 的T細胞,缺乏FDC聚集。
在與NLPHL鑑別診斷方面,大細胞的免疫表型的價值是有限的,因為二者的免疫表型很相似;但在T/HRLBCL往往容易檢測到Ig輕鏈。此外.對CD20進行染色可顯示結節形狀和富B細胞背景有利於NLPHL的診斷。濾泡中有FDC聚集(CD21+)和存在大量CD57+ 細胞同樣提示NLPHL在鑑別T/HRLBCL與經典HL時免疫表型的檢測是必要的,有幫助的如果大細胞表達CD20而不表達CD15和CD30,診斷傾向於T/HRLBCL,若表達CD15或CD30則提示經典HL。若診斷為經典HL的病例僅表達CD20則其預後比表達CD15和(或)CD30,CD20+/- 的HL病例明顯不佳(表11)。
2.間變性大細胞性淋巴瘤(ALCL) ALCL是一種以惡性大細胞為特徵的淋巴瘤,具有明顯的核仁和豐富的胞質可類似單核或多核的RS細胞變異型腫瘤細胞呈黏附性生長常侵犯淋巴結竇此外腫瘤細胞通常比RS細胞小核仁較不明顯,常為豆形或馬蹄形,核仁外周無暈輪與單核RS細胞的圓形細胞核相反,ALCL的腫瘤細胞具有一個明顯的核旁核窩ALCL在年齡分布上呈雙峰曲線在兒童和成人各有一個發病高峰雖然ALCL臨床上呈侵襲性,但它典型的具有良好的治療反應。尤其是兒童。由於ALCL的治療和HL不同所以正確的診斷非常重要。
3.慢性淋巴結炎 一般的慢性淋巴結炎多有感染灶,有急性期,如足癬感染可致同側腹股溝淋巴結腫大或伴紅、腫熱痛等急性期症狀,或只有淋巴結腫大伴疼痛。急性期過後,淋巴結縮小疼痛消失而慢性淋巴結炎的淋巴結腫大一般約0.5~1.0cm,質地較軟扁、多活動與之相反HL腫大淋巴結具有大、豐滿、質韌的特點必要時需切除活檢。
4.急性化膿性扁桃體炎 除有不同程度的發熱外扁桃體多為雙側腫大,紅腫、痛,且其上附有膿苔,捫之質地較軟炎症控制後扁桃體可縮小。而HL侵及扁桃體,可雙側也可單側也可不對稱的腫大,捫之質地較硬、韌稍晚則累及周圍組織有可疑時可行扁桃體切除或活檢行病理組織學檢查。
5.淋巴結結核 為特殊慢性淋巴結炎.腫大的淋巴結以頸部多見多伴有肺結核如果伴有結核性全身中毒症狀如低熱盜汗消瘦乏力等則與HL不易區別;淋巴結結核之淋巴結腫大質較硬表面不光滑質地不均勻,或因乾酪樣壞死而呈囊性,或與皮膚粘連活動度差OT試驗呈陽性反應淋巴結穿刺或活檢可找到郎漢斯細胞或上皮樣細胞。
值得注意的是,HL病人可以患有結核病,這可能是由於長期抗瘤治療機體免疫力下降,從而易患結核等疾患因此臨床上應當提高警惕我國醫學科學院腫瘤醫院曾有一例HL患者經抗腫瘤治療後緩解一段時間但後來持續低熱、雙肺門有放射狀陰影經抗炎、抗真菌治療無效而懷疑HL復發,給予化療最後屍檢證實為結核未找到HL證據。
6.結節病 多見於青少年及中年人,多侵及淋巴結可以多處淋巴結腫大常見於肺門淋巴結對稱性腫大,或有氣管旁及鎖骨上淋巴結受累,淋巴結多在2cm直徑內,質地一般較硬也可伴有長期低熱結節病的確診需取活檢,可找到上皮樣結節Kein試驗在結節病90%呈陽性反應,血管緊張素轉換酶在結節病人之淋巴結及血清中均升高。
7.組織細胞性壞死性淋巴結炎 該病在中國多見,多為青壯年臨床表現為持續高熱但周圍血之白細胞數不高用抗生素治療無效,酷似惡性網織細胞增生症組織細胞性壞死性淋巴結炎之淋巴結腫大以頸部多見,直徑在1~2cm質中或較軟,不像HL的淋巴結。確診需行淋巴結活檢本病經過數周后熱退而愈。
8.Castleman病 是一種少見的慢性淋巴結增生性疾病臨床分為局灶性和多中心性。局灶型以單個胸腹腔或淺表淋巴結緩慢性腫大直徑多為3~7cm。以胸腔內特別是縱隔最常見其次為頸部腋下、腹部,亦可見於結外組織。多中心型以多處淋巴結緩慢增大形成巨大腫塊,伴有全身症狀實驗室檢查示:貧血(100%)或同時有白細胞、血小板計數降低多克隆免疫球蛋白增高,ESR增快,類風濕因子及抗核抗體可陽性。淋巴結穿刺見血管顯著增生和透明樣變或伴漿細胞增多。
9.白血病 從血及骨髓象即可作出診斷,但究竟為淋巴細胞白血病還是淋巴瘤累及骨髓需結合病史臨床及實驗室檢查進行鑑別。臨床上一般以淋巴結腫痛為主要症狀者稱為淋巴瘤當出現白血病血象者即認為淋巴瘤合併白血病。
10.淋巴結轉移癌 有原發病灶的表現。淋巴結活檢有助於鑑別。
檢查
實驗室檢查:
1.病理活檢 是確診HL及病理類型的主要依據。HL最常採用的是淋巴結活檢當累及其他組織如皮膚等也可做活檢和印片以助確診肝、脾穿刺塗片及病理檢查如有適應證也可予以適當考慮其他結外侵犯的也儘可能取活檢證實如縱隔淋巴結腫大,特別是無淺表淋巴結腫大的病人也要在全面檢查後行CT下穿刺活檢。
2.外周血 約10%的病人有小細胞低色素性貧血,大多數由胃腸道少量失血引起。晚期常有嚴重貧血白細胞數一般在正常範圍,也可出現白細胞總數和中性粒細胞增多。晚期病人常常有白細胞和淋巴細胞的減少嗜酸性細胞的增加尤其是伴有皮膚特異性損害時血小板早期多為正常疾病晚期或伴有脾亢或放療化療後減少,也可因伴發ITP而減少甚至發生出血傾向血液中RS細胞極罕見並發白血病時可有白血病的血象特點。
3.
骨髓象 早期正常,約有3%病例骨髓塗片可找到RS細胞,對診斷有特殊價值但呈RS細胞白血病者極為罕見,骨髓活檢發現RS細胞及其單核細胞變異型陽性率高於塗片,可達9%~22%HL骨髓受侵常伴廣泛纖維化LD或MC易合併骨髓受侵而NS和NLP很少見。並發ANLL時可顯示白血病骨髓象的特點。
4.血沉 血沉在活動期增快,緩解期正常為測定緩解期和活動期較為簡便的方法。
5.血清β2-微球蛋白 Hagberg等對189例未經治療腎功能正常的惡性淋巴瘤患者檢測血清β2-MG,ⅠⅡ期HL患者有11%升高,ⅢⅣ期有83%升高。
6.可溶性白介素-2受體(SIL-2R) HL患者的HL細胞和RS細胞大多數表達IL-2R,IL-2R水平與疾病的嚴重程度有關具有較明顯的臨床症狀或復發的病人SIL-2R常升高。
7.血清鐵蛋白(SF)測定 活動期患者SF增高,緩解期病人SF下降復發時又增高提示對HL病人進行SF測定有助於了解腫瘤擴散範圍有助於了解疾病的活動情況。
8.外周血鐵蛋白測定 鐵蛋白的測定對病情評估和預後判斷有一定意義。
9.血清生化檢查 如中性粒細胞鹼性磷酸酶(NAP)、血清鹼性磷酸酶(AKP)及血清乳酸脫氫酶(LDH)隨病情進展而增高;血漿蛋白電泳測定約半數晚期病例顯示γ球蛋白含量減少血清α2-球蛋白升高。早期有40%病人IgGIgA稍升高,而IgM降低CRP、C3及Fg也可升高上述檢查雖不能肯定診斷,但對病情及預後的判定可能有所幫助。
其它輔助檢查:
1.X線檢查 各類型淋巴瘤累及縱隔的X線征大體相似典型HL胸部病變常表現為前縱隔雙側不對稱的淋巴結腫大影,輪廓清楚邊緣可呈直線狀或波浪狀,密度均勻無鈣化;側位胸片見腫瘤位於中縱隔的中上部。支氣管受侵可致狹窄阻塞表現為肺不張的X線特徵。約有30%侵及胸膜表現為胸腔積液有的可見病理性骨折胃腸道淋巴瘤通過鋇劑造影可見腔內不規則充盈缺損,局部不規則的狹窄或擴張;有些可出現龕影,局部僵直,蠕動減弱或消失,較難與消化道腫瘤相鑑別。
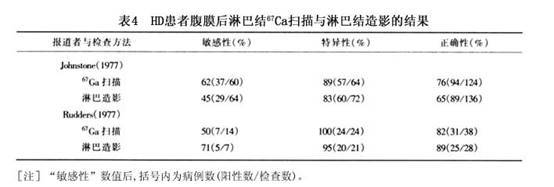
2.淋巴造影術 淋巴造影術目的是診斷和治療HL對膈上受侵的Ⅰ~Ⅱ期HL當腹部和盆腔CT陰性尤其是要進行根治性放療時才考慮做淋巴造影術淋巴造影術在提供正常大小淋巴結精細結構方面具有優勢是HL患者腹膜後和盆腔淋巴結相當精確的方法其敏感性和特異性在90%以上通過分期剖腹術對CT和淋巴管造影進行比較,結果證明淋巴管造影檢查HL患者後腹膜淋巴結比CT的敏感性高10%,且更特異和精確在某些方面淋巴造影術能夠彌補腹部CT掃描的不足。表4。
3.CT CT對於HL的診斷性評估是必不可少的,為淋巴瘤分期首選影像方法。與胸部X線相比CT能更精確的識別縱隔心包胸膜、肺和胸壁疾病,並且CT能識別上腹部淋巴結和腫大的肝、脾病變胸片陰性者CT可檢出5%~30%病變,對於胸片異常者,可多發現25%~42%胸片漏診的病變腹部、盆腔CT能準確發現增大的淋巴結,但只能以大小確定異常(≥1.5cm為異常),無法觀察淋巴結內部結構的改變;對於實質器官應常規做增強掃描有助於發現病變和做出鑑別診斷但是如果上腹部淋巴結大小正常或脾淋巴結病變則CT無法檢測到這些隱伏病變,而這些病變的發生率為20%~25%。表5
4.B超 B超為淋巴瘤分期常用的第2種手段可多軸面掃查能發現腹部、盆腔淋巴結腫大和器官受侵。
5.MRI MRI易於顯示胸腔腫大淋巴結,採用專門的脈衝頻率可增強淋巴瘤的顯示。MRI的作用在於鑑別治療後纖維化與腫瘤復發或殘存;當患者對碘造影劑過敏時MRI不僅容易鑑別淋巴結與血管還能同時檢出肝、脾腎、胰腺等實質器官的受侵。最近Dohner等研究了30例淋巴瘤病人MRI與骨髓活檢的關係除4例不符外,其餘MRI與骨髓活檢結果一致。認為MRI是確定淋巴瘤骨髓侵犯的一個敏感方法MRI可確定HL及高度惡性NHL的骨髓侵犯,從而對骨髓形態學評估作一個補充。
6.淋巴結掃描 據報導對未經治療的HL陽性診斷率為88%並能發現普通X線無法顯示的病灶。目前常用的是核素(Ga)掃描Ga-67掃描有助於識別隱伏的HL,尤其可證實具有殘餘X線攝影異常的病人的持續病變但是鎵掃描偶有假陽性或假陰性結果可高至30%~50%。PET成像技術目前處於初步階段,但具有套用前景(表4)。
7.99mTc全身骨掃描 其原理是將放射性核素99mTc標記在PL上作為示蹤劑,利用PL高度聚集於肝脾、淋巴骨髓等網狀內皮系統的特點用γ相機進行體外顯像。由於骨髓網狀內皮細胞吞噬膠體的活性與骨髓造血組織總活性水平相平行,故骨髓攝取99mTc-PL的量能夠間接反應各部分骨髓造血組織的活性水平患者全身性骨髓的異常和其功能狀態可由骨髓γ顯像片直接顯示故骨髓顯像對於了解惡性淋巴瘤患者骨髓功能活性水平尋找骨髓受侵病灶選擇穿刺定位和合理治療間隔,並隨訪觀察,均有重要臨床價值。
治療
1.治療常規 HD一般按臨床分期採用化療和放射治療。
(1)ⅠA和ⅡA期首選放射治療(次全淋巴結照射或區域照射)。
(2)ⅠBⅡB和ⅢA期首選全淋巴結照射。
(3)ⅢB期和LD亞型首選化療,以後可酌情進行放射治療
(4)縱隔大腫塊(橫徑>1/3胸腔橫徑)應先作化療2周期腫物縮小後再放療。
(5)Ⅳ期病人以化療為主,目前為多數學者接受的治療方案(圖1)
①劑量:每4~6周40~44Gy
②照射野:次全淋巴結(STLI)照射膈上病變採用斗篷野和全肋形野照射,膈下病變採用倒丫野和斗篷野。全淋巴結(TLI)照射即斗篷野加倒丫野。
③兒童患者由於處於發育期:為了防止放射引起的發育障礙,放療劑量應適當降低,照射野也適當限制,如改為局部擴大野。
根據不同年齡劑量調整如下:<5歲 20Gy5~10歲 25Gy,11~15歲 30Gy早期HD通過照射可取得良好根治性效果美國Stanford大學的結果如表12。近年來對於早期霍奇金病由於治癒率高和減少第2原發癌的發生治療趨向保守。適當病例可以進行區域性照射加化療遠期結果和全淋巴結照射相同。
2.化學治療 隨著新藥的增多特別是近20年來聯合化療的發展和經驗的積累HD的化療效果已有明顯提高常用化療方案如表13。
約75%~80%的HD病人通過MOPP治療可達完全緩解約60%~65%的病人可得治癒ABVD作為與MOPP不交叉耐藥的補充治療,可在一定程度上提高MOPP的療效(表1415)。
經多年的臨床研究ABVD方案對男性生殖細胞的抑制較MOPP輕為暫時性;第2原發尤其是急性白血病很少。進一步