端粒學說由Olovnikov提出,認為細胞在每次分裂過程中都會由於DNA聚合酶功能障礙而不能完全複製它們的染色體,因此最後複製DNA序列可能會丟失,最終造成細胞衰老死亡。端粒是真核生物染色體末端由許多簡單重複序列和相關蛋白組成的複合結構,具有維持染色體結構完整性和解決其末端複製難題的作用。大量實驗說明端粒、端粒酶活性與細胞衰老及永生有著一定的聯繫。但是隨著時間的推移,有些問題用端粒學說尚有疑問。2009年,諾貝爾瑞典卡羅林斯卡醫學院將諾貝爾獎生理學或醫學獎授予美國加利福尼亞舊金山大學的伊莉莎白·布萊克本(ElizabethBlackburn)、美國巴爾的摩約翰·霍普金斯醫學院的卡羅爾-格雷德(CarolGreider)、美國哈佛醫學院的傑克·紹斯塔克(JackSzostak)以及霍華德休斯醫學研究所,以表彰他們發現了端粒和端粒酶保護染色體的機理。
基本介紹
- 中文名:端粒學說
- 外文名:telomerase
端粒學說由Olovnikov提出,認為細胞在每次分裂過程中都會由於DNA聚合酶功能障礙而不能完全複製它們的染色體,因此最後複製DNA序列可能會丟失,最終造成細胞衰老死亡。
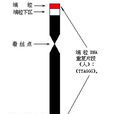
端粒是真核生物染色體末端由許多簡單重複序列和相關蛋白組成的複合結構,具有維持染色體結構完整性和解決其末端複製難題的作用。端粒酶是一種逆轉錄酶,由RNA和蛋白質組成,是以自身RNA為模板,合成端粒重複序列,加到新合成DNA鏈末端。在人體內端粒酶出現在大多數的胚胎組織、生殖細胞、炎性細胞、更新組織的增生細胞以及腫瘤細胞中。正因如此,細胞每有絲分裂一次,就有一段端粒序列丟失,當端粒長度縮短到一定程度,會使細胞停止分裂,導致衰老與死亡。
大量實驗說明端粒、端粒酶活性與細胞衰老及永生有著一定的聯繫。第一個提供衰老細胞中端粒縮短的直接證據是來自對體外培養成纖維細胞的觀察,通過對不同年齡供體成纖維細胞端粒長度與年齡及有絲分裂能力的關係觀察到隨著增齡,端粒的長度逐漸變短,有絲分裂的能力明顯漸漸變弱;Hastie發現結腸端粒限制性片段的長度隨供體年齡增加逐漸縮短,平均每年丟失33bp的重複序列;植物中不完整的染色體在受精作用中得以修復,而不能在已經分化的組織中修復,這在較為高等的真核生物中也證實了體細胞中端粒酶的活性受抑制;精子的端粒要比體細胞長,體細胞缺失端粒酶活性就會逐漸衰老,而生殖細胞系的端粒卻可以維持其長度;轉化細胞能夠通過端粒酶的活性完全複製端粒以得永生。
但是有些問題用端粒學說尚有疑問。體細胞端粒長度與有絲分裂能力呈正比,這一點實驗已經證實了,而不同的體細胞其有絲分裂能力是不盡相同的,胃腸黏膜細胞的分裂增殖速度就比較快,神經細胞分裂的速度就比較慢。曾有人就不同年齡供體角膜內皮細胞的端粒長度進行研究發現角膜內皮細胞內端粒長度長期維持在一個較高的水平,而端粒酶卻不表達。另外,Kippling發現,鼠的端粒比人類長近5-10倍,壽命卻比人類短的多。這些都提示體細胞端粒長度與個體的壽命及不同組織器官的預期壽命並非一致。生殖細胞的端粒酶活性長期維持較高的水平卻不會象腫瘤那樣無限制分裂繁殖;端粒長度由端粒酶控制,那何種因素控制端粒酶呢?生殖細胞內端粒酶活性較高,為什麼體細胞中沒有較高的端粒酶活性。看來端粒的長度縮短是衰老的原因還是結果尚需進一步研究。
2009年,諾貝爾瑞典卡羅林斯卡醫學院將諾貝爾獎生理學或醫學獎授予美國加利福尼亞舊金山大學的伊莉莎白·布萊克本(ElizabethBlackburn)、美國巴爾的摩約翰·霍普金斯醫學院的卡羅爾-格雷德(CarolGreider)、美國哈佛醫學院的傑克·紹斯塔克(JackSzostak)以及霍華德休斯醫學研究所,以表彰他們發現了端粒和端粒酶保護染色體的機理。