碳酸氫根(HCO3-)的原子排布為平面結構,碳位於中心,與三個氧原子鍵連(一個C=O,一個C-OH,一個C-O-)。它是碳酸的共軛鹼,也是碳酸根離子的共軛酸。水溶液中存在下列平衡,碳酸氫根既可發生電離生成碳酸根離子(CO32-)和氫離子(H+),也會水解生成氫氧根離子(OH-)和碳酸(H2CO3),由於碳酸氫根的水解(產生OH-)程度大於電離(產生H+)程度,因此其水溶液呈弱鹼性。
基本介紹
- 中文名:碳酸氫根
- 符號:HCO3-
- 化合價:-1價
- 酸鹼性:碳酸氫根顯鹼性
基本信息
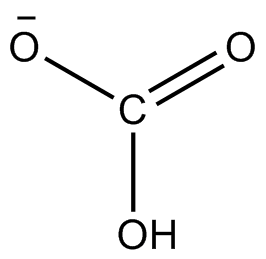
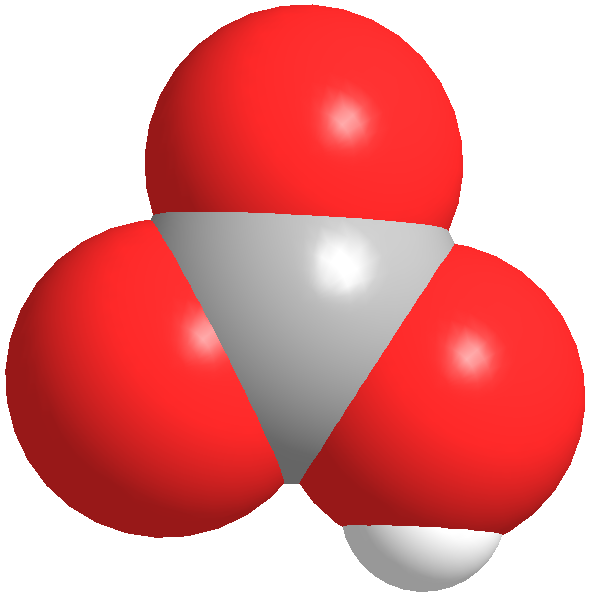
碳酸氫根(HCO3-)的原子排布為平面結構,碳位於中心,與三個氧原子鍵連(一個C=O,一個C-OH,一個C-O-)。它是碳酸的共軛鹼,也是碳酸根離子的共軛酸。水溶液中存在下列平衡,碳酸氫根既可發生電離生成碳酸根離子(CO32-)和氫離子(H+),也會水解生成氫氧根離子(OH-)和碳酸(H2CO3),由於碳酸氫根的水解(產生OH-)程度大於電離(產生H+)程度,因此其水溶液呈弱鹼性。

碳酸氫根(HCO3-)的原子排布為平面結構,碳位於中心,與三個氧原子鍵連(一個C=O,一個C-OH,一個C-O-)。它是碳酸的共軛鹼,也是碳酸根離子的共軛酸。水溶液中...
實際碳酸氫根(AB)是指在隔絕空氣的條件下,取血分離血漿測得的HCO3實際含量。...... 實際碳酸氫根(AB)是指在隔絕空氣的條件下,取血分離血漿測得的HCO3實際含量。...
碳酸根的化學式為CO3(離子CO32-),相對分子質量60。雖然含碳,但含碳酸根的物質卻多是無機物。碳酸根是一種弱酸根,在水中很容易水解產生碳酸氫根離子和氫氧根離子,...
碳酸氫鹽是碳酸形成的酸式鹽,含有碳酸氫根離子。大多數碳酸氫鹽對熱不穩定,會分解為碳酸鹽、二氧化碳和水。鹼金屬碳酸氫鹽溶於水,水溶液呈鹼性,與酸迅速反應放出...
指動脈血液標本在溫度37℃和血紅蛋白完全氧合(SaO2達100%)的條件下,用PCO2為5.33kPa的氣體平衡後所測得的血漿碳酸氫根(HCO3-)濃度。...
由於碳酸根可以結合水中的質子(即氫離子)生成碳酸氫根和碳酸,並且能結合酸中的質子釋放二氧化碳。所以碳酸鈉在酸鹼質子理論中屬於布朗斯特鹼。...
2、碳酸氫鎂過量時候要考慮到碳酸氫根二級電離:HCO3- 可逆生成 H+ + CO32-電離出來的氫離子跟氫氧根結合 因此過量時候電離為Mg2+ + 2HCO3- + 2Ca2+ + 4OH-...
二碳酸氫根四氨合鉑(II)是化學物質,CSA號是123439-82-7。...... 二碳酸氫根四氨合鉑(II)是化學物質,CSA號是123439-82-7。CAS號 123439-82-7 分子式 C2H1...
靜脈用藥還應注意下列問題:(1)靜脈套用的濃度範圍為1.5%(等滲)至8.4%;(2)應從小劑量開始,根據血中pH值、碳酸氫根濃度變化決定追加劑量;(3)短時期大量靜脈輸注...
指未經氣體平衡處理的人體血漿中的碳酸氫根(HCO3-)的真實含量,故又稱真實重碳酸鹽。是指隔絕空氣的血標本在實際條件下測得的碳酸氫鹽含量。...
實際碳酸氫鹽指未經氣體平衡處理的人體血漿(即隔絕空氣的血液標本)中的碳酸氫根的真實含量,它是反映酸鹼平衡代謝因素的指標;實際碳酸氫鹽與標準碳酸氫鹽相比,它受...
標準碳酸氫鹽是全血在37℃時,二氧化碳分壓在在5.32千帕(40mmHg),血紅蛋白在100%氧飽和的條件下測出的血漿碳酸氫根濃度。其不受呼吸的影響,故是判斷代謝改變的...
2.鹼化尿液,套用本品時,由於尿中碳酸氫根濃度升高,尿液 PH升高,使尿酸,磺胺類藥及血紅蛋白等不易在尿中形成結晶或聚集. 3.制酸,口服能迅速中和或緩衝胃酸,而...
AB,中文名稱為實際碳酸氫根,是體內代謝性酸鹼失衡重要指標,參考值為21.4~27.3mmol/L。
HCO3-重吸收試驗是一項用於檢查腎小管酸化功能是否正常的一項輔助檢查方法。正常人經腎小球濾出的碳酸氫根大部分(85%-90%)由近端腎小管重吸收入血,另外的10%-...
10.329 [6] 碳酸氫根 HCO3- 10.5 [6] 次碘酸 HOI 10.62 [6] 甲胺* MeNH3+ 10.63 [6] 乙胺* EtNH3+ 10.77 [6] 二甲胺* Me2NH2+ 10.80 [6...
此外腎臟的泌氫離子和碳酸氫根離子重吸收功能受動脈血的二氧化碳分壓、血鉀濃度等多種因素的影響。原發性代謝性酸中毒或鹼中毒的形成,主要與呼吸運動和腎臟活動有關...
