甲烷化反應是在催化劑存在下,用氫氣還原一氧化碳和二氧化碳生成甲烷和水的反應。
基本介紹
- 中文名:甲烷化反應
- 特點:體積縮小、強放熱過程
- 使用:催化劑
- 生成:甲烷和水
反應原理
影響因素
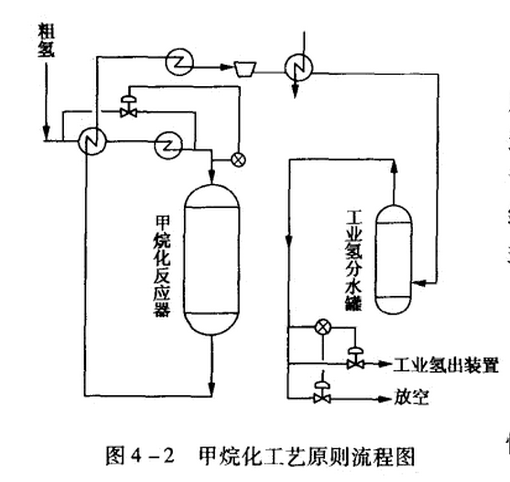 甲烷化工藝流原則程圖
甲烷化工藝流原則程圖甲烷化催化劑
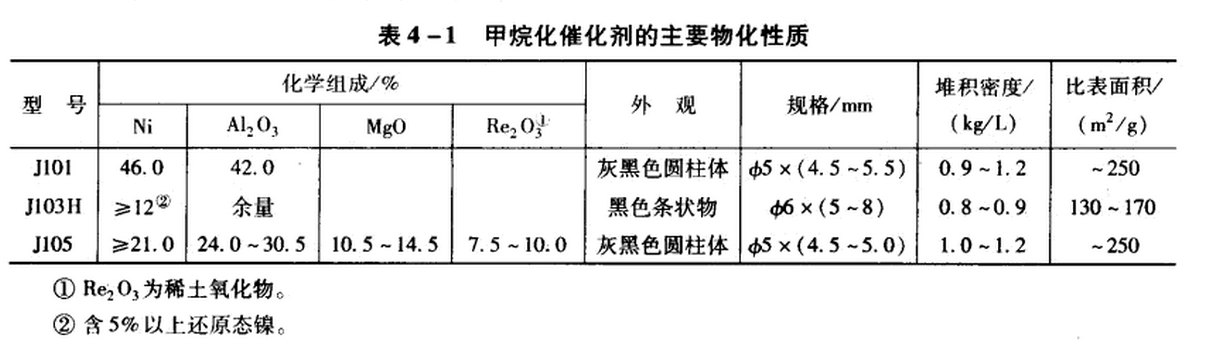 甲烷化催化劑主要性質
甲烷化催化劑主要性質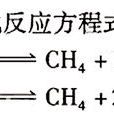
甲烷化反應是在催化劑存在下,用氫氣還原一氧化碳和二氧化碳生成甲烷和水的反應。
 甲烷化工藝流原則程圖
甲烷化工藝流原則程圖 甲烷化催化劑主要性質
甲烷化催化劑主要性質甲烷化反應是在催化劑存在下,用氫氣還原一氧化碳和二氧化碳生成甲烷和水的反應。...... 甲烷化反應是在催化劑存在下,用氫氣還原一氧化碳和二氧化碳生成甲烷和水的反...
屬於此類反應的有,烴類加氫裂解反應、積炭反應、合成氨反應、費托合成反應、CO甲烷化反應等。而結構不敏感反應(facile reaction)則是指催化劑活性組分固定後,催化劑...
甲烷化反應141氨合成基本原理145氨合成動力學1467催化劑148氨的利用與生產150合成氣制甲醇152甲醇的物理和化學性質155甲醇原料氣的製造157甲醇合成熱力學163...
合成天然氣是一種根據甲烷化反應原理利用相應的設備將含碳資源轉化為甲烷的技術。我國的能源資源特點是少油、貧氣、富煤。煤炭資源相對豐富,充分利用廉價的煤炭資源...
電轉氫氣僅進行電解水反應,反應效率約為56%~73%,避免了甲烷化反應的能量損失,同時削減了甲烷化反應相關的基礎建設費用。但氫氣注人到現有天然氣管道會引起管材...
這些研究幾乎不可能在系統自身上完成,因為從技術上很難保持過程處於穩態,而且生物甲烷化反應的起動過程很慢,需要幾周的時間。但如果利用(仿真)模型在計算機上仿真,...
甲烷化法是在催化劑存在下使少量CO、CO2與H2反應生成CH4和H2O的一種淨化工藝,要求入口原料氣中碳的氧化物含量(體積分數)一般應小於0.7甲烷化法可以將氣體中碳的...
但如果利用(仿真)模型在計算機上仿真,則甲烷化反應的起動過程只需要幾分鐘的時間。數字模型又稱數字沙盤,多媒體沙盤、數字沙盤系統等,它是以三維的手法進行建模,...
53. 朱秋軍,王海洋,李振花. Ni基催化劑上CO甲烷化反應性能研究. 天然氣化工,2012,37(2),17~2054. Haiyang Wang, Zhenhua Li, Xinbin Ma. Effect of ...
①選擇反應器直徑5.0m,高度12.0m,數量2座,鋼製結構。 ②設備選用時最好採用兩台串聯使用,第一台設備為第一段酸化反應,第二台設備為第二段甲烷化反應,原污水...
5、甲烷化反應CO+2H2=CH4+74KJ/mol6、Boudouard反應C+CO2=2CO-172KJ/mol煤炭氣化技術煤氣化工藝 編輯 煤炭氣化技術雖有很多種不同的分類方法,但一般常用按生產...
能源導入量的擴大,利用風力發電、太陽能發電等的剩餘電力電解水生成氫,然後提供給現有的燃氣管道網路;或者利用電力、水及大氣中的CO2,通過甲烷化反應製造甲烷,提供...
3、部分氧化反應C+0.5 O2=CO+111KJ/mol4、完全氧化(燃燒)反應C+O2=CO2+394KJ/mol5、甲烷化反應CO+2H2=CH4+74KJ/mol6、Boudouard反應...
5、甲烷化反應CO+2H2=CH4+74KJ/mol6、Boudouard反應C+CO2=2CO-172KJ/mol煤炭氣化技術煤氣化工藝 編輯 煤炭氣化技術雖有很多種不同的分類方法,但一般常用按生產...
但甲烷化反應中需消耗氫氣,且生成對合成氨無用的惰性組分──甲烷。合成氨原料氣水分乾燥 水蒸氣對氨合成催化劑有害,故被水蒸氣所飽和的新鮮氮氫混合氣在進入...
實驗6 42熱導式自動量熱計的標定和化學反應熱的測定203 實驗6 43CO2加氫甲烷化反應207 實驗6 44氣態小分子熱力學函式的理論計算211 實驗6 45振盪反應的系統動力...
3、氣體裝置設計與最佳化;4、汽油穩定、石腦油分離和氣提、反應精餾、變換和甲烷化反應器、酸水分離器、硫和 HF 酸烷基化、脫異丁烷塔等設計與最佳化; [3] ...
將其導入膜分離裝置, 在膜的非滲透側得到富甲烷氣體, 然後把來自PSA 裝置的H2與之混合, 再將該混合氣進行甲烷化反應, 使CO2 轉變為CH4 , 由此得到高熱值城市...
6 3 4活性炭甲烷化反應353 參考文獻364 第7章催化劑的性能評價與表征369 7 1催化劑的性能評價370 7 1 1基本概念371 7 1 2催化劑的性能評價374 7 2催化劑...
