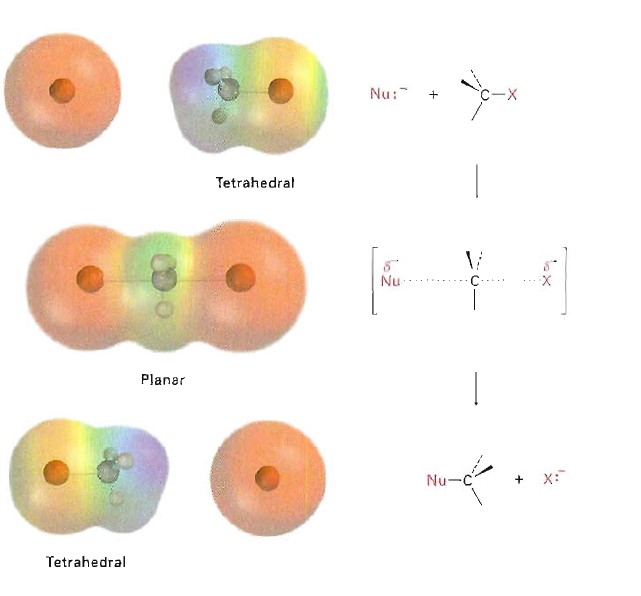
雙分子親核取代反應
相關詞條
- 雙分子親核取代反應
雙分子親核取代反應反應(SN2)是親核取代反應的一類,其中S代表取代(Substitution),N代表親核(Nucleophilic),2代表反應的決速步涉及兩種分子。與SN1反應相對應,SN2反應...
- 親核取代反應
親核取代反應是指有機分子中與碳相連的某原子或基團被作為親核試劑的某原子或基團取代的反應。在反應過程中,取代基團提供形成新鍵的一對電子,而被取代的基團則帶...
- 親核取代
親核取代反應簡稱SN。飽和碳上的親核取代反應很多。例如,鹵代烷能分別與氫氧化鈉、醇鈉或酚鈉、硫脲、硫醇鈉、羧酸鹽和氨或胺等發生親核取代反應,生成醇、醚、...
- 分子內親核取代
分子內親核取代反應(internal nucleophilic substitution)用SNi表示,其中S代表取代,N代表親核,i代表分子內。...
- 取代反應
取代反應(substitution reaction)是指化合物或有機物分子中任何一個原子或原子團被試劑中同類型的其它原子或原子團所替代的反應,用通式表示為:R-L(反應基質)+A-...
- 雙分子反應
雙分子反應,元反應類型之一,其特點是在決定反應速率的步驟中,涉及兩個反應物分子間的變化。...
- 威廉姆遜合成反應
威廉姆遜合成(Williamson合成)是製備混合醚的一種方法。是由鹵代烴與醇鈉或酚鈉作用而得。是一種雙分子親核取代反應(SN2)。最早由亞歷山大·威廉·威廉姆遜發表於英國...
- Menschutkin反應
叔胺與鹵代烴作用生成季銨鹽的反應,稱為Menschutkin反應。Menschutkin反應是研究得較多的親核取代反應之一,對溶劑的動力學效應也進行了廣泛和深入的研究,並獲得了巨大...
- 雙分子共軛鹼消除
雙分子共軛鹼消除:即E2反應,反應體系中若有鹼存在,則隨著鹼濃度的提高,消除產物增多。這說明反應速度不僅與鹵代烷的濃度有關,而且還與鹼的濃度有關,在動力學上...
- 取代反應機理
取代反應機理me}hanistn of displa}enient reaction;練Jmechanism又稱}NZ機理·反應ML}+Y}MLn -,Y+l}M為金屬離子,L為配位體,Y為親核試劑,n配位體黝目)...
- 親核反應
由親核試劑進攻反應物而引起的反應稱為親核反應。親核反應又可以進一步分為親核加成反應,親核取代反應。親核取代反應又包括單分子親核取代和雙分子親核取代。...
- 疊氮反應
疊氮反應是在有機分子中引入疊氮基是用含N-3的親核試劑中N-3取代鹵素、磺酸酯基、硝胺酯基、硝酸酯基等可離去基團,反應機理為親核取代反應(SN)。...
- 單分子反應
整個反應速率只決定於第一個慢的步驟。由於在決定反應速率的慢步驟中只有一個反應物(RL)分子參加,所以一般把按這種過程進行的反應叫做單分子親核取代反應SN1(S代表...
- 取代(漢字詞語)
取代是指有機分子里的某些原子或原子團通過化學反應被其他原子或原子團所替代。包括親核取代和親電取代。...
- 取代基效應
同一族(或同一組)反應物中各種不同取代基對其熱力學性質(如平衡常數等)和動力學參數(如反應速率常數等)的影響。反應物分子中的一個基團被另一基團所取代的反應...
- 光延反應
光延反應是一種雙分子親核取代反應(SN2反應)。由日本化學家光延旺洋(Mitsunobu, O) 等人於1967年發現,是現代有機合成中常用的反應。...
- 雙分子鹼催化烷氧斷裂
某些酯如2, 4, 6— 三叔丁基苯甲酸甲酯在甲醇水溶液中是按雙分子鹼催化烷...按BAL2機理的水解,是飽和碳原子上的親核取代反應,因此,當R′的體積較大時, ...
- 威廉姆遜合成
威廉姆遜合成(Williamson合成)是製備混合醚的一種方法。是由鹵代烴與醇鈉或酚鈉作用而得。是一種雙分子親核取代反應(SN2)。最早由A. W. Williamson發表於英國化學...
- 鄰位效應
由於反應物結構和反應條件的差異,SN有兩種機理,即單分子親核取代反應SN1和雙分子親核取代反應SN2。2、SN1的過程分為兩步:第一步,反應物發生鍵裂(電離),生成...
- 有機化學(第2版)(李毅群、王濤、郭書好主編書籍)
8.4鹵代烷的性質8.4.1鹵烷的物理性質8.4.2鹵烷的化學性質8.5飽和碳原子上的親核取代反應歷程8.5.1單分子親核取代反應(SN1)歷程8.5.2雙分子親核取代反應(SN2)...
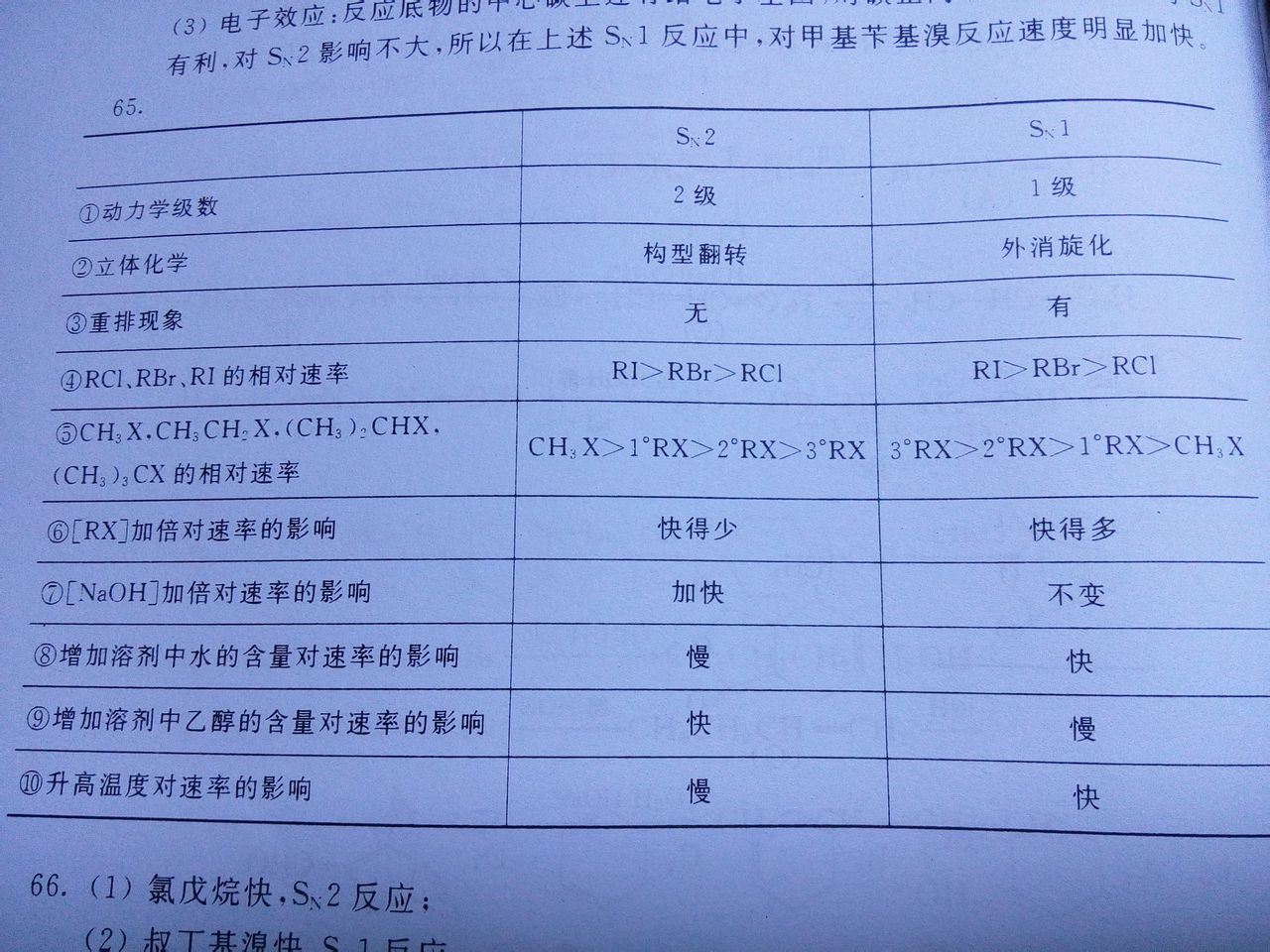 SN2與SN1的對比
SN2與SN1的對比