化學電池中,能使電解質發生氧化反應的電極稱為陽極。此外,在電子管中用來接收或加速從陰極發射的電子的電極也叫陽極。
基本介紹
- 中文名:陽極
- 外文名:anode
- 套用範圍:電化學,電學等
- 反義詞:陰極
基本概念
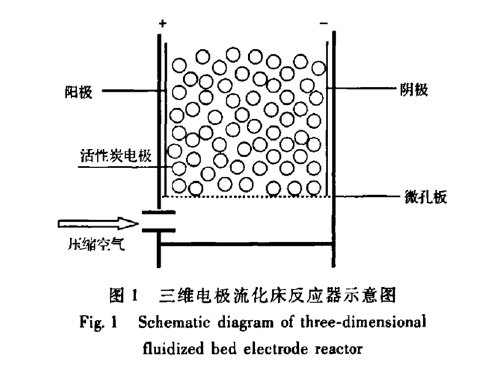
化學電池中,能使電解質發生氧化反應的電極稱為陽極。此外,在電子管中用來接收或加速從陰極發射的電子的電極也叫陽極。

化學電池中,能使電解質發生氧化反應的電極稱為陽極。此外,在電子管中用來接收或加速從陰極發射的電子的電極也叫陽極。...
陽極氧化(anodic oxidation),金屬或合金的電化學氧化。鋁及其合金在相應的電解液和特定的工藝條件下,由於外加電流的作用下,在鋁製品(陽極)上形成一層氧化膜的過程...
陽極化處理,是一種金屬表面處理工藝。是指金屬材料在電解質溶液中,通過外施陽極電流使其表面形成氧化膜的一種材料保護技術,又稱表面陽極氧化。...
在電池中,電子從此處流入電解質中的一極叫做陽極。在腐蝕過程中,陽極是溶解趨勢較大的一方。在陽極發生的陽極反應是氧化反應,即一種元素或原子團由低價氧化成高價...
陽極區是指電弧焊接時,電弧緊靠正電極的區域。陽極的導電機理比陰極簡單得多。陽極帶正電,可以吸收電弧柱來的電子,電子不斷從弧柱補充進來,這樣,陽極附近總保持...
金屬陽極又稱形穩性陽極,是在金屬鈦的基質上用熱分解法被覆一層鉑族金屬(如釕)氧化物和閥金屬(如鈦)氧化物混晶結構的塗層。這塗層比貴金屬鈍化膜具有耐還原...
由陽極極化引起的金屬鈍化現象,叫陽極鈍化或電化學鈍化。陽極鈍化是作為陽極的金屬或化合物在電流作用下,不同程度地失去轉入溶液的能力。一般認為陽極鈍化是陽極表面...
由於預焙陽極技術要求將炭塊經1100~1200攝氏度高溫下焙燒,去除揮發分,使瀝青焦化,提高製品的機械強度和導電性,所以成型後未經焙燒的陽極稱為生陽極。...
廢陽極即生陽極廢品。振動成型後的生製品,需按生陽極外觀檢測標準逐塊進行檢查,對不符合生陽極外觀檢測標準的成型塊挑檢出來,其中類型有裂紋,麻面、彎面、彎曲,...
犧牲陽極是指電解池理論金屬做陽極情況下,陽極(金屬)隨著流出的電流而逐漸消耗。犧牲陽極通常僅經濟地套用在保護電流需要量小的構築物上和低土壤電阻率環境中。...
以鋁或鋁合金製品為陽極,置於電解質溶液中進行通電處理, 利用電解作用使其表面形成氧化鋁薄膜的過程, 稱為鋁及鋁合金的陽極氧化處理。經過陽極氧化處理,鋁表面能...
電流通過時,自身不溶解,只發生氧化反應的陽極。電鍍中不溶性陽極的材料有鉛、碳、鉑、石墨、鎳、不鏽鋼、鍍鉑的鈦、鉛合金和鑄造的磁性氧化鐵等。...
陽極防腐——一種電解法,可使有色金屬進行陽極氧化,以達到防腐蝕和防磨損的作用。陽極防護是指通過對處於酸性介質中的鋼質材料通以適當的陽極電流使金屬表面陽極...
陽極地床又稱為輔助陽極,是外加電流陰極保護系統中,將保護電流從電源引入土壤中的導電體。通過輔助陽極把保護電流送入土壤,經土壤流入被保護的管道,使管道表面進行...
犧牲陽極陰極保護是將活性不同的兩種金屬連線後,處於同一電解質中,活性強的金屬失去電子,受到腐蝕,活性差的金屬得到電子受到保護。由於在這一過程中,活性強的金屬...
預焙陽極是以石油焦、瀝青焦為骨料,煤瀝青為黏結劑製造而成,用作預焙鋁電解槽作陽極材料。這種炭塊已經過焙燒,具有穩定的幾何形狀,所以也稱預焙陽極炭塊,習慣上...
鎂是電化學陰極保護工程中常用的一種犧牲陽極材料,具有較高的化學活性,它的電極電位較負,驅動電壓高。同時,鎂表面難以形成有效的保護膜。因此,在水介質中,鎂表面...
陽極炭塊(anode carbon block)是指以石油焦、瀝青焦為骨料,煤瀝青為黏結劑生產的炭塊,用作預焙鋁電解槽做陽極材料。這種炭塊已經過焙燒,具有穩定的幾何形狀,...
陽極銅俗稱“粗銅”。是以銅精礦為原料熔煉的銅中間產品,一般含銅量98%~99%,為電解法生產陰極銅的原料。世界上有陽極銅冶煉廠約100座,生產能力約1000萬噸,...
在酸性溶液中,鋁陽極在外電流作用下氧化時,同時發生兩個過程:氧化膜的生成和氧化膜的溶解,當成膜的速度超過膜溶解的速度時,鋁表面才有氧化膜的實際存在,這就...
陽極保護是指將被保護金屬作為陽極,進行陽極氧化而使金屬鈍化的保護方法。陽極保護的關鍵是建立和保持鈍態,因此不是陽極極化曲線具有明顯的鈍化特徵的腐蝕體系都一定...
陽極化處理是利用氧化原理使用電解氧化處理生成氧化鋁,本身自發生成帶色的陽極氧化膜,具有抗腐蝕,抗氧化的功能。鋁陽極氧化膜可分為阻擋型和多孔型兩類,在接近中性...
硬質陽極化是一種厚層鋁陽極氧化工藝。...... 獲得硬質陽極氧化膜的溶液很多,其中以直流、低溫硫酸電解液套用最J’一。[1] 參考資料 1. 化學化工大辭典 詞條標...
陽極氧化鋁是指在鋁及鋁合金表面鍍一層緻密氧化鋁為了防止進一步氧化,其化學性質與氧化鋁相同。但是與一般的氧化膜不同,陽極氧化鋁可以用電解著色加以染色。...
銷售和服務為一體,電鍍是一種電化學過程,也是一種氧化還原過程.電鍍的基本過程是將零件浸在金屬鹽的溶液中作為陰極,金屬板作為陽極,接直流電源後,在零件上沉積出...
