過渡金屬促進的C-C鍵活化反應近年來引起了較大的興趣。醇是一類很常用的反應底物,可以通過β-C消除來實現C-C鍵活化,繼而發生後續的轉變。但醇類的C-C活化仍然較為困難,條件較為苛刻。如果能在醇類底物中引入額外的合適基團與過渡金屬進行配位,則有望穩定反應中的關鍵C-C活化過渡態/中間體,從而實現較為溫和的反應。
基本介紹
- 中文名:逆羥醛縮合
- 對應:羥醛縮合
- 套用1:C-C鍵活化
- 套用2:α-芳基化反應
- 領域:有機合成
逆羥醛縮合實現C-C鍵活化及在α-芳基化反應
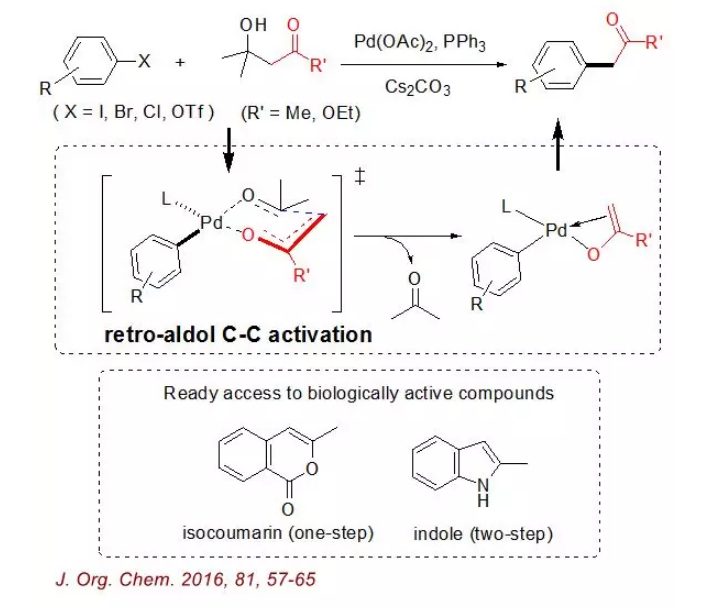 實例
實例
過渡金屬促進的C-C鍵活化反應近年來引起了較大的興趣。醇是一類很常用的反應底物,可以通過β-C消除來實現C-C鍵活化,繼而發生後續的轉變。但醇類的C-C活化仍然較為困難,條件較為苛刻。如果能在醇類底物中引入額外的合適基團與過渡金屬進行配位,則有望穩定反應中的關鍵C-C活化過渡態/中間體,從而實現較為溫和的反應。
 實例
實例最後,DFT理論計算支持該反應包含一個關鍵的逆羥醛縮合C-C活化步生成鈀烯醇鹽中間體,它是整個催化循環的決速步。該逆羥醛縮合策略有望在其它基本的有機反應中...
羥醛反應(英語:Aldol reaction)是有機化學中形成碳-碳鍵的重要反應之一。它是指:具有α氫原子的醛或酮在一定條件下形成烯醇負離子,再與另一分子羰基化合物發生...
五、定向羥醛縮合21 六、類羥醛縮合反應28 七、不對稱羥醛縮合反應30 第二節芳醛的α-羥烷基化反應 (安息香縮合反應)33 第三節有機金屬化合物的α-羥烷基...
桂醛在鹼催化下的水解反應為逆羥醛縮合反應。在反應中, 桂油中存在的天然肉桂醛在鹼催化下水解生成苯甲醛和沸點較低的乙醛,因此隨著乙醛的逸出,可使反應向有...
新高效甲醛阻聚劑中含有乙烯醇基與甲醛進行羥醛縮合,該反應是一個可逆反應,可降低甲醛分子間自聚,同時形成的乙烯醇縮醛基是一個六元環狀結構,有較大的空間位阻...
當按逆羥醛縮合和逆Claisen縮合類型進行裂解時,形成 α,β-烯酸。遷移過程為氫氧根離子先奪取雙鍵烯丙位的氫原子,然後再在另一個烯丙位進行質子化。α,β-烯酸...
(1)羥醛縮合在稀鹼或稀酸的作用下,兩分子的醛或酮可以互相作用,其中一個醛(或酮)分子中的α-氫加到另一個醛(或酮)分子的羰基氧原子上,其餘部分加到羰基...
化學合成法有:逆羥醛縮合法、仿生合成法、以噁唑衍生物為前體合成法。 天然提取法有:聚醯胺法、超臨界二氧化碳萃取分子精餾法等。 還有一種新型的提取法:分子...
它是Meerwein-Ponndorf-Verley還原反應的逆反應,屬於可逆反應,也是一個由二級醇...一級醇可以不受破壞,雖也可以氧化為相應的醛,但存在副反應羥醛縮合反應,效果...
11 36Friedel Crafts烷基化的逆反應34811 37芳醛的脫羰34911 38芳酸的脫羧...16 38羥醛縮合反應58416 39Mukaiyama羥醛反應及相關反應58616 40羧酸酯或醯胺...
第5章 縮合與聚合反應5.1 概述5.2 羥醛縮合反應5.3 羧酸及其衍生物的縮合5.4 加成聚合方法5.5 縮合聚合方法5.6 縮合與聚合反應套用第6章 逆合成反應...
