基本介紹
- 中文名:螯合反應
- 外文名:Chelate reaction
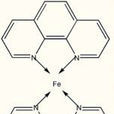
對同一種原子,若形成螯合物比單基配位體形成的絡合物(非螯合物)要更加穩定,這種反應稱作螯合反應。螯合物一般以五元環、六元環為最穩定,且一個絡合劑與中心...
螯合物是具有環狀結構的配合物,是通過兩個或多個配位體與同一金屬離子形成螯合環的螯合作用而得到。...
螯合反應就是生成螯合物的化學反應。螯合物是配合物的一種,在螯合物的結構中,一定有一個或多個多齒配體提供多對電子與中心體形成配位鍵。“螯”指螃蟹的大鉗,...
金屬原子或離子與含有兩個或兩個以上配位原子的配位體作用,生成具有環狀結構的絡合物,該絡合物叫做螯合物。能生成螯合物的這種配體物質叫螯合劑,也稱為絡合劑。...
螯合酵素催化劑樣的催化作用催動著機體的生化反應,催動著生命現象的進行。若沒有酵素,生化反應將無法進行,五大營養素都將變的對機體毫無用處,生命現象將會停止。它...
螯合分散劑是一種高效多用途的有機螯合物,它可以軟化水質,對Ca2+、Mg2+、Fe3+等金屬離子有很強的螯合力及浮渣分散力,防止染整加工過程中沉澱物的生成及其它污物...
又稱螯合微量元素肥料(chelate micro fertilizers),簡稱螯合微肥。用螯合劑與植物必需的微量元素(硼和鉬除外)製成的肥料,如螯合鋅、螯合鐵、螯合錳、螯合銅等。...
螯合樹脂(chelate resins ),是一類能與金屬離子形成多配位絡合物的交聯功能高分子材料。螯合樹脂吸附金屬離子的機理是樹脂上的功能原子與金屬離子發生配位反應,形成...
重金屬螯合劑,通常也被叫做重金屬離子析出劑,重金屬捕集劑等。...... 環聚合等方法製取;另一種是利用合成的或天然的高分,通過高分子化學反應引入具有螯合功能的鏈...
食品螯合劑chelGting agent= for focal一類能夠鰲合食uni,中不希望有的金屬離子(如},ll` } , }'' P3 .等)的食品添加劑因為一些金屬離子會催化和參與一些...
對同一種原子,若形成螯合物比單基配位體形成的絡合物(非螯合物)要更加穩定,這種效應稱作螯合效應。螯合物一般以五元環、六元環為最穩定,且一個絡合劑與中心...
金屬螯合蛋白是所有含有金屬離子的蛋白質,甚至包括在蛋白質基因表達時,為便於分離而引入His6-標籤(易與鎳結合)的蛋白質。金屬離子是某種物質溶於水後的金屬元素的...
螯合劑驅鉛試驗是挑撥試驗或鉛代謝試驗,主要通過觀察機體對鰲合劑CaNa2EDTA的驅鉛反應,判斷機體的鉛負荷。...
又稱螯合聚合物,螯型聚合物。螯合物是一種特殊絡合物,指在絡合物中一個分子可以提供多配位基團,形成螯型結構的絡合物。如果提供多配位的分子是聚合物大分子時稱...
微量元素胺基酸螯合物是第三代微量元素添加劑,屬於有機微量元素範疇。...... 螯合物是指1個或多個配位基團與金屬離子之間的配位反應所形成的環狀結構產物,金屬氨基...
谷氨酸螯合銅又稱谷氨酸銅,為藍色粉末,緩慢溶於水,乙醇等,高濃度溶液為深藍色。...... 谷氨酸螯合銅又稱谷氨酸銅,為藍色粉末,緩慢溶於水,乙醇等,高濃度溶液為深...
金屬螯合親和層析(MCAC)是近30年來出現的一種親和層析技術,也稱固相化金屬離子親和層析。它於1975年首先被Porath和他的合作者們成功用於分離純化人血清蛋白。並...
