定義,編號系統,物理性質,分子結構及化學性質,用途,生態學數據,生態學數據,分子結構數據,計算化學數據,性質與穩定性,健康危害,侵入途徑,健康危害,急性中毒,慢性中毒,生產方法,簡介,製備、衍生物,毒理資料,毒性,急性毒性,慢性毒性,致突變性,生殖毒性,致癌性,生物降解,危險特性,燃燒產物,應急處理,泄漏處理,防護措施,急救措施,安全術語,
定義
工業上最重要的稠環
芳香烴。純品為具有香樟木氣味的白色晶體,熔點80.5℃。主要用於生產
鄰苯二甲酸酐、
染料中間體、
橡膠助劑和殺蟲劑等。1958年以來,代替
滴滴涕等氯化產品的
甲萘威投產後,用作殺蟲劑原料的比例有所增加。萘的用途分配,各國有所不同,大致用於生產鄰苯二甲酸酐約占70%,染料中間體(如
β-
萘酚)和橡膠加工助劑約占15%,殺蟲劑約占6%,鞣革劑約占4%,染料生產較少的國家,如美國則用於生產殺蟲劑的比例較大。
英文別名naphthalene, pure; Melting point standard naphthalene;
'LGC' (2402); 'LGC' (2603); 1-NAPHTHALENE;
 萘晶體顯微結構
萘晶體顯微結構TAR CAMPHOR; NAPTHALENE; NAPTHALIN; NAPHTHENE
分子式:C10H8
CAS登錄號91-20-3
EINECS號202-049-5
國標編號41511
分子量128.18
InChI編碼InChI=1/C10H8/c1-2-6-10-8-4-3-7-9(10)5-1/h1-8H
編號系統
CAS號:91-20-3
MDL號:MFCD00001742
EINECS號:202-049-5
RTECS號:QJ0525000
BRN號:1421310
物理性質
密度1.162
熔點80.5℃,沸點217.9℃,凝固點,80.5℃,
閃點78.89℃,折射率1.58212(100℃)恆容燃燒熱:5148.9KJ/mol(標準大氣壓,298.15K) 恆壓燃燒熱:-5153.9KJ/mol(標準大氣壓,298.15K)。
易揮發,易升華
溶於乙醇後,將其滴入水中,會出現白色渾濁。
分子結構及化學性質
(1)萘的氧化反應
溫和氧化劑得醌,強烈氧化劑得酸酐。萘環比側鏈更易氧化,所以不能用側鏈氧化法制萘甲酸。
電子云密度高的環易被氧化。例如α-硝基萘氧化得3-硝基鄰苯二甲酸酐,α-萘胺氧化得鄰苯二甲酸酐(氨基所在的環被氧化)。
(2) 萘的還原反應(加成反應)
萘可與5個氫氣加成生成十氫化萘。
萘的α-位比β-位更易發生親電取代反應。α-位取代兩個共振式都有完整的苯環。β-位取代只有一個共振式有完整的苯環。
在萘環上主要發生親電取代,同苯環一樣(易取代,難加成),但活性比苯環強。
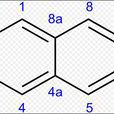
從中間對稱的兩個C旁邊的C開始標(中間的兩個碳不編號),其中1,4,5,8號碳活性完全一樣(稱為α碳),2,3,6,7號碳性質完全一樣(稱為β碳)。
一般情況下,α碳活性大於β碳,取代基在α位上,這是由動力學控制,溫度較高時,α碳上取代基會轉移到β碳上。
但在萘的弗瑞德-克來福特醯基化反應,不加熱卻生成了α位和β位的混合物。如用硝基甲烷為溶劑,則主要生成β醯化產物 。
用途
廣泛用作製備染料、樹脂、溶劑等的原料,也用作驅蟲劑(俗稱
衛生球或
樟腦丸)。易取代,難加成。
生態學數據
1.生態毒性 LC50:1.37~3.8mg/L(96h)(魚類)
2.生物降解性
好氧生物降解(h):12~480
厭氧生物降解(h):600~6192
3.非生物降解性
水相光解半衰期(h):1704~13200
光解最大光吸收波長範圍(nm):310.5~220.5
水中光氧化半衰期(h):1704~13200
空氣中光氧化半衰期(h):2.96~29.6
4.生物富集性 BCF:36.5~168(鯉魚,接觸濃度0.15ppm,接觸時間8周);23~146(鯉魚,接觸濃度0.015ppm,接觸時間8周)
生態學數據
1.生態毒性 LC50:1.37~3.8mg/L(96h)(魚類)
2.生物降解性
好氧生物降解(h):12~480
厭氧生物降解(h):600~6192
3.非生物降解性
水相光解半衰期(h):1704~13200
光解最大光吸收波長範圍(nm):310.5~220.5
水中光氧化半衰期(h):1704~13200
空氣中光氧化半衰期(h):2.96~29.6
4.生物富集性 BCF:36.5~168(鯉魚,接觸濃度0.15ppm,接觸時間8周);23~146(鯉魚,接觸濃度0.015ppm,接觸時間8周)。
分子結構數據
1、摩爾折射率:44.09
2、摩爾體積:123.5
3、等張比容(90.2K):311.1
4、表面張力(dyne/cm):40.2
5、介電常數(F/m):2.82
6、極化率:17.48
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:0
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積0
7.重原子數量:10
8.表面電荷:0
9.複雜度:80.6
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.用五氧化二釩和硫酸鉀作催化劑,矽膠作載體,於385-390℃用空氣氧化得到鄰苯二甲酸酐。在乙酸溶液中用氧化鉻進行氧化,生成α-萘醌。加氫生成四氫化萘,進一步加氫則生成十氫化萘。在氯化鐵催化下,將氯氣通入萘的苯溶液中,主要得到α-氯萘。光照下與氯作用則生成四氯化萘。萘的硝化比苯容易,常溫下即可進行,主要產物是α-硝基萘。萘的磺化產物和溫度有關,低溫得到α-萘磺酸,較高的溫度下,主要得到β-萘磺酸。
2.萘的水溶性較小,而且不易被吸收,故其毒性不太強。吸入濃的萘蒸氣或萘粉末時,能促使人嘔吐,不適,頭痛。特別是損害眼角膜,引起小水泡及點狀渾濁,還能使皮膚發炎,有時還能引起肺的病理改變,還可損害腎臟,引起血尿,但沒有致癌性。工作場所萘的最大容許濃度為
。生產設備及容器應密閉,防止蒸氣粉末外逸,操作現場強制通風。若發生中毒現象,要立即移至新鮮空氣處,多飲熱水,使之嘔吐,進行人工呼吸,嚴重者送醫院治療。
3.穩定性 穩定
4.禁配物 強氧化劑(如鉻酸酐、氯酸鹽和高錳酸鉀等)
5.聚合危害 不聚合
健康危害
侵入途徑
吸入、食入、經皮吸收。
健康危害
具有刺激作用,高濃度致溶血性貧血及肝、腎損害。會導致貧血或紅細胞數、血色素和血細胞數顯著減少。對皮膚敏感者,萘會引起一些嚴重的皮膚病。
急性中毒
吸入高濃度萘蒸氣或粉塵時,出現眼及呼吸道刺激、角膜混濁、頭痛、噁心、嘔吐、食慾減退、腰痛、尿頻、尿中出現蛋白及紅
白細胞。亦可發生視神經炎和視網膜炎。重者可發生中毒性腦病和肝損害。口服中毒主要引起溶血和肝、腎損害,甚至發生
急性腎功能衰竭和肝壞死。
慢性中毒
反覆接觸萘蒸氣,可引起頭痛、乏力、噁心、嘔吐和
血液系統損害。可引起白內障、視神經炎和視網膜病變。皮膚接觸可引起皮炎。
生產方法
簡介
1.由石油烴製得:催化重質重整油,催化裂化輕循環油,裂解制乙烯的副產焦油等;
2.由煤焦油分離,高溫煤焦油中萘約占8%-12%,將煤焦油蒸餾,切取煤油,經脫酚,脫喹啉,蒸餾得成品萘。每噸萘消耗10t煤焦油;
3.粗萘經白土精製而得精萘;
4.降膜分步結晶法 結晶法生產過程由產品生產工藝系統、能源系統、氮氣密封系統和計算機控制系統等組成。生產工藝系統以大循環為生產周期,每個大循環包含4個小循環,每個小循環又包含4~6個段,每個段由結晶、部分熔融和全部熔融3個步驟組成;
(降膜結晶法操作工藝實例:由工業萘裝置送來的液態工業萘送入餾分槽中,當進行第四段結晶操作時,用泵將槽中的原料液送入動態結晶器收集槽中。未結晶萘油與發汗液放入純度低一級的餾分槽中,全熔液可作為第五段的原料。按預定程式進行六段結晶精製後即可得到產品精萘。為提高萘的提取率,可將富含硫茚的餾分送往靜態結晶器中處理,靜態結晶器所得的產品返回動態結晶系統的相應餾分槽,殘液可作為減水劑出售。由於該裝置同時採用動態和靜態結晶器,既可保證較高的萘回收率,又能降低能耗。)
5.靜態分步結晶法 將原料工業萘裝入結晶箱後進行快速降溫,降至82℃後轉為均勻降溫,以2℃/h的降溫速度冷卻至60℃,排放富含硫茚的第一次晶析萘油,作為中間餾分待後處理。然後結晶箱內的物料以4℃/h的速度升溫,間隔0.5h取樣一次,測定其結晶點,根據結晶點的不同,分別排入對應餾分槽,如此進行3~4次分步結晶,可得到較高純度的精萘。
製備、衍生物
可由
煤焦油的中油部分和石炭酸部分分出(焦油萘);也可從裂解焦油碳十
餾分分出(石油萘);此外,還可從
甲基萘經脫甲基製得。
毒理資料
毒性
屬低毒類。
急性毒性
LD50: 490mg/kg(大鼠經口);人經口5g,白內障及腎損害;人經口5~15g,致死;兒童經口2.0g/2日,致死。
慢性毒性
兔經口1g/(kg·天),3天,見晶狀體渾濁,20天后形成白內障。兔吸入
飽和蒸氣2小時/天,2~3個月,紅細胞先增多後減少;400~500mg/m3,4小時/天,5個月,見晶狀體渾濁。小鼠吸入60~500mg/m3,5個月,條件反射紊亂,屍檢見呼吸系統損害。
致突變性
細胞遺傳學分析:倉鼠卵巢30mg/L。
姊妹染色單體交換:倉鼠卵巢15mg/L。
生殖毒性
小鼠經口最低中毒劑量(TDL0):2400mg/kg(孕7~14天),影響活產指數,影響存活指數(如活產在第4天時的存活數)。
致癌性
大鼠皮下最低中毒劑量(TDL0):3500mg/kg(12周,間歇),疑致腫瘤劑,致淋巴瘤,包括何杰金氏病,致子宮腫瘤。小鼠吸入最低中毒濃度(TCL0):30ppm(6小時)(2處,間歇),致腫瘤,致肺腫瘤。
生物降解
在環境中的遷移幾個實驗證明了
多環芳烴(PAHs)的
可生物降解性。低分子量的多環
芳香烴(PAHs)如萘、苊、
苊烯在實驗研究中均能快速地被降解。初始濃度為5~10mg/L的液體,在7天之內有90%以上的多環芳香(PAHs)被生物降解。高分子量的
多環芳香烴(PAHs)如
熒蒽、苯並(a)蒽、屈、
苯並(a)芘和和蒽等很難被 生物降解。
危險特性
遇明火、高熱可燃。燃燒時放出有毒的刺激性煙霧。與
強氧化劑如鉻酸酐、
氯酸鹽和高錳酸鉀等接觸,能發生強烈反應,引起燃燒或爆炸。粉體與空氣可形成
爆炸性混合物,當達到一定的濃度時,遇火星會發生爆炸。
燃燒產物
一氧化碳,二氧化碳,水
應急處理
泄漏處理
隔離泄漏污染區,限制出入。切斷火源。建議應急處理人員戴自給式呼吸器,穿一般作業工作服。不要直接接觸泄漏物。小量泄漏:避免揚塵,使用無火花工具收集於乾燥、潔淨、有蓋的容器中。運至空曠處引爆。或在保證安全情況下,就地焚燒。大量泄漏:用塑膠布、帆布覆蓋,減少飛散。使用無火花工具收集回收或運至廢物處理場所處置。
防護措施
呼吸系統防護:高濃度蒸氣接觸可應該佩戴過濾式防毒面具(半面罩);可能接觸其粉塵時,建議佩戴自吸過濾式防塵口罩。
身體防護:穿防毒物滲透工作服。
手防護:戴防化學品手套。
其它:工作現場禁止吸菸、進食和飲水。工作畢,淋浴更衣。
急救措施
皮膚接觸:脫去被污染的衣著,用肥皂水和清水徹底沖洗皮膚。
眼睛接觸:提起眼瞼,用流動清水或生理鹽水沖洗。就醫。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸,就醫。
食入:飲足量溫水,催吐,就醫。
安全術語
安全標識:S16S22S39S46S60S61S36/S37
危險標識:R11R22R40R43R50/53
 萘晶體顯微結構
萘晶體顯微結構