義齒加工,範圍,引用檔案,分類與型號,要求,基本要求,材料,外觀,色澤,表面光澤度,強度,咬合,試驗方法,基本要求檢查,材料檢查,外觀檢查,色澤,表面光澤度,強度試驗,咬合試驗,檢驗規格,交付條件,檢驗分類,出廠檢驗,型式檢驗,其他信息,標誌,包裝,驗配記錄卡,使用說明書,運輸,貯存,
義齒加工
:
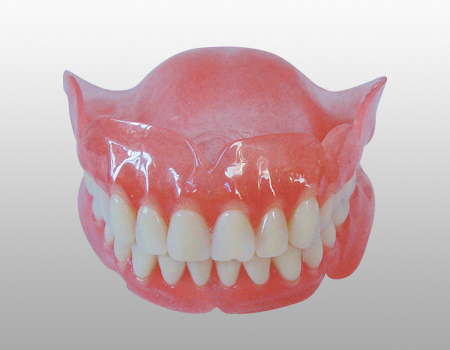
定製式全口義齒
定製式固定義齒
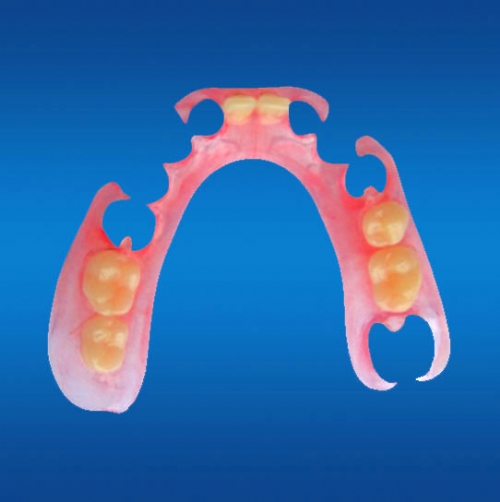
定製式可摘局部義齒
範圍
以下內容包含義齒加工的分類、要求、試驗方法、標誌、包裝、運輸和貯存。
該產品套用於口腔修復。
引用檔案
GB/T 191 包裝儲運圖示標誌
GB/T 6387-1998 齒科材料名詞術語
GB/T 9937-1988 齒科材料、器械、設備、測試和操作中的名詞術語
GB/T 9938-1988 牙位和口腔區域的標示法
GB/T 9969.1 工業產品使用說明書 總則
YY 0270-2003 牙科學 義齒基托聚合物
YY 0300 牙科學 修復用人工牙
YY 0466.1 醫療器械 用於醫療器械標籤、標記和提供信息的符號 第1部分:通用要求
YY 0620 牙科學 鑄造金合金
YY 0621 牙科金屬 烤瓷修復體系
YY 0626 貴金屬含量25%~75% 的牙科鑄造合金
YY 0716 牙科陶瓷
《定製式義齒註冊暫行規定》(國食藥監械〔2003〕365號)
《醫療器械說明書、標籤和包裝表示管理規定》(國家食品藥品監督管理局令第10號)
分類與型號
定製式全口義齒
(1)按照產品組成及用途不同,可分為以下兩種:
a) 金屬支架全口義齒;
b) 膠托全口義齒
(2)組成:該產品由基托和樹脂組成,基托分為金屬基托和樹脂托。材料為已取得醫療器械註冊證的樹脂、金屬、樹脂牙。
(3)適用範圍:本產品按口腔醫生定製要求製作,適用於牙列缺失的修復。
(4)產品禁忌症:口腔組織創口未愈或有炎症者禁用;對塑膠、金屬等義齒材料過敏者禁用;對精神病、癲癇或生活不能自理者需慎用
(5)基準
產品以完整的石膏模型為基準製作,但修復體完成後模型即被破壞,不能以模型為基準進行檢驗。
(6)型號
產品的型號用下列方式表示:
Z D Q — ×
其中,Z L —— 生產企業標識號:Zhi Mei (致美齒科技術發展有限公司);
D —— 產品名稱碼: Denture (義齒);
Q —— 產品特徵碼: Quankou (全口);
×× —— 產品分類碼:1,2 (詳見表1)。
注 : ZDQ-3 表示西安致美齒科技術發展有限公司生產的定製式膠托全口義齒。
表1
定製式固定義齒
分類
(1)按照產品組成及用途不同,可分為以下四種:
c) 冠:包括烤瓷熔附金屬牙冠、鑄造金屬牙冠、全瓷牙冠;
d) 橋:包括烤瓷熔附金屬橋、鑄造金屬橋、全瓷橋;
(2) 產品性能結構及組成:該產品由固位體、橋體、連線體和牙冠組成。由烤瓷合金材料和烤瓷粉製成。材料為已取得醫療器械註冊證的考瓷粉和烤瓷合金。
(3) 產品適用範圍: 該產品按口腔醫生定製要求加工製作,主要適用於:1、牙齒顏色異常或形態異常,及不宜用其他方法修復的。2、齲洞或牙體缺損交大無法填充治療者。3、前牙位置異常,影響美觀,不能做正畸治療者。4、牙列缺損(牙缺失)且缺牙區兩端都有餘留牙,餘留牙條件較好的。
(4) 產品禁忌症:1、青少年恆牙尚未發育完全者禁用。2、牙體過小無法取得足夠的固位形和抗力形者禁用。3、嚴重的深覆頜、咬頜緊無法預備出足夠的間隙者禁用。4、牙齒連續缺失超過3個或牙鬆動者禁用。5、對金屬有過敏史者禁用。
(5) 基準:產品以完整的石膏模型為基準製作並檢驗。
(6) 型號
產品的型號用下列方式表示:
Z D G — ××
其中,Z L —— 生產企業標識號:Zhi Mei (致美齒科技術發展有限公司);
D —— 產品名稱碼: Denture (義齒);
×× —— 產品分類碼:11,12,13,21,……(詳見表1);
注 : ZDG-23 表示西安致美齒科技術發展有限公司生產的定製式全瓷橋固定義齒。
表2
分類碼 | 1 | 2 | 3 |
1 | 烤瓷熔附金屬牙冠 | 鑄造金屬牙冠 | 全瓷牙冠 |
2 | 烤瓷熔附金屬橋 | 鑄造金屬橋 | 全瓷橋 |
定製式可摘局部義齒
(1)分類
按照產品組成及用途不同,可分為以下四種:
e) 冠:包括烤瓷熔附金屬牙冠、鑄造金屬牙冠、全瓷牙冠;
f) 橋:包括烤瓷熔附金屬橋、鑄造金屬橋、全瓷橋;
(2)產品性能結構及組成:該產品主要由樹脂牙、基托、卡環等結構構成,材料為已取得醫療器械註冊證的樹脂、金屬、樹脂牙。
(3)產品適用範圍:該產品按口腔醫生定製要求製作,適用於牙列缺損修復
(4)產品禁忌症:
1、口腔組織創口未癒合或有炎症者禁用。
2、對塑膠、金屬等義齒材料過敏者禁用。
3、對精神病、癲癇或生活不能自理者需慎用
1.1 (5)基準:產品以完整的石膏模型為基準製作,但修復體完成後模型即被破壞,不能以模型為基準進行檢驗。
(6)產品的型號用下列方式表示:
Z D Q — ×
其中,Z L —— 生產企業標識號:Zhi Mei (致美齒科技術發展有限公司);
D —— 產品名稱碼: Denture (義齒);
Q —— 產品特徵碼: Quankou (全口);
×× —— 產品分類碼:1,2 (詳見表1)。
注 : ZDQ-3 表示西安致美齒科技術發展有限公司生產的定製式膠托可摘局部義齒。
表3
分類碼 | 1 | 2 |
產品類別 | 金屬支架可摘局部義齒 | 膠托可摘局部義齒 |
要求
基本要求
1. 產品應根據臨床口腔醫生提供的患者牙模及按規定程式批准的圖樣、設計檔案製造。
2. 產品的製作應符合口腔臨床醫生的設計要求。
材料
製作產品的所用材料必須是經國家批准註冊的齒科材料產品或醫用產品。其所用基底金屬應採用符合YY 0620、YY 0621、YY 0626的牙科專用金屬及合金,陶瓷應符合YY 0716的要求。
組成產品的基托或牙體的材料應符合YY 0270、YY 0300或其它相關標準的規定。
外觀
1. 產品的外部形態應具有人體生理學中牙體正常解剖學的基本特徵,基本符合個性修復與仿生修復原則。
2. 產品的外形及大小應與同名牙相匹配,即與醫療機構提供的牙模和模型設計單位所示要求的外形相一致。
3. 產品的鄰面與相鄰牙之間的接觸部位應與同名正常牙的接觸部位相一致。
4. 產品的咬合面應有接觸點,不應存在咬合障礙。
5. 產品用肉眼觀察應無裂紋、無氣泡,內部應無氣孔、雜質。。
6. 產品表面(固位部分除外)應光滑、有光澤,無氣孔、裂紋、縮坑、麻點與毛刺,組織面不得存在殘餘石膏。
7. 產品不得有刺激異味,樹脂基托不得有肉眼可見的氣孔和裂紋,鑄造的基托、連線體和卡環內部應無氣孔、雜質,且不得有白色斑點。。
色澤
產品的表面色澤應與臨床口腔醫生所指定的標準色片色澤相一致(為模仿充填的邊緣或天然牙的釉質缺陷所特殊設計的分界線除外)。
表面光澤度
義齒中除組織面外,假牙、基托、卡環及連線體均應高度拋光,表面粗糙度應達到R≤0.025。
強度
產品應能經受100N壓力持續2min而不應出現裂紋、破損、斷裂等現象。
咬合
(不包含固定義齒)
產品的上、下頜修復體對合後,4~7牙位均應有接觸,且上下頜修復體之間應無翹動現象。
試驗方法
基本要求檢查
通過檢查與驗證,其結果應符合4.1的規定。
材料檢查
通過逐批驗證(是否具有有效的醫療器械產品註冊證或符合國標、行標的出廠檢驗報告)或檢驗進行評價,證明製造產品的主要材料能符合4.2的規定。
外觀檢查
正常目力(必要時藉助通用器具如牙科探針)檢查,其結果應符合4.3的規定。
色澤
在距離40瓦日光燈不超過1.5米直射光線下,用通用比色板比對,產品的色澤應符合4.4條的規定。
表面光澤度
在帶光源的5倍放大鏡下,用正常目力觀察和用粗糙度樣板比對檢查,產品的表面光潔度應符合4.5條的規定。
強度試驗
1. 試驗設備
萬能試驗機或其它施力裝置。誤差不超過±1%。
2. 試樣製備
同樣類型和色澤的3副產品。
3. 試驗步驟
將義齒兩端通過模型固定,從咬合面中間向下平穩施加100N壓力,並使恆力保持2min,卸載並取下試樣。
用正常目力觀察,試樣應符合4.6條的規定。
咬合試驗
手動操作試驗,應符合4.7條的規定
檢驗規格
交付條件
產品由生產企業質量檢驗部門驗收,檢驗合格後,方可交付。
檢驗分類
檢驗分為出廠檢驗和型式檢驗(周期檢驗)。
出廠檢驗
出廠檢驗依照4.3、4.4、4.5條的規定逐件進行檢驗。
型式檢驗
(周期檢驗)
其他信息
標誌
產品包裝上應有下列標誌:
a) 製造企業名稱、地址、電話;
b) 產品名稱、適用牙位;
c) 數量、編號(或批號);
d) 生產日期;
e) 醫療器械產品註冊證號。
f) 醫療器械生產企業許可證號;
g) 採用標準;
h) 產品使用說明;
i) “易碎物品”等字樣或符號,其標誌應符合GB/T 191及YY/T 0466.1的規定。
包裝
1.2.1 包裝
產品用中性泡泡塑膠膜纏裹包裝,再裝入自封式或其他結構的塑膠袋中,塑膠袋應密封。應保證在正常搬運和貯存期間產品不受損壞。
註: 允許契約規定的其它包裝方式。
1.2.2 合格證
每一包裝上應附有檢驗合格證。
檢驗合格證上應有下列內容:
a) 產品名稱、編號(或批號);
b) 製造企業名稱;
c) 檢驗日期;
d) 檢驗員姓名或代號。
驗配記錄卡
每批產品應附相應的驗配記錄卡,其內容應包括:
a) 患者基本資料(至少應包括姓名、牙位等);
b) 產品基本資料(至少應包括牙位、材料等);
c) 醫療機構基本情況(至少應包括名稱、地址、電話、醫生姓名等);
d) 生產企業基本情況(至少應包括名稱、地址、服務電話等)。
使用說明書
使用說明書的術語應符合GB/T 6387-1998、GB/T 9937-1998、GB/T 9938-1998等的規定。
使用說明書的內容應符合GB/T 9969.1及《醫療器械說明書的管理規定》等的要求。
運輸
常規運輸條件或按契約規定。
貯存
產品應存放在常溫、乾燥(相對濕度不大於85% RH)、通風、潔淨的場所。