分子中含有氨基(一NH3)和羧基(一COOH)的絡合劑。試劑分子中含有多個配位原子(O與N),能與大多數金屬離子形成穩定的螫合物(chelate),常用於絡合滴定,最常用的氨羧絡合劑是乙二胺四乙酸(EDTA)。
基本介紹
- 中文名:氨羧絡合劑
- 外文名:complexonetrilon
- 套用學科:分析化學
- 本質:氨氮和羧氧配位原子的配位多元酸
- 常用試劑:乙二胺四乙酸
基本性質
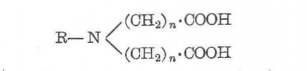 化學通式
化學通式製備方法
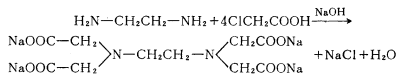 製備EDTA反應方程式
製備EDTA反應方程式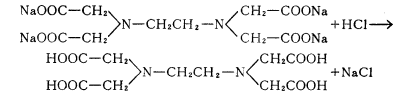 沉澱析出方程式
沉澱析出方程式性 質
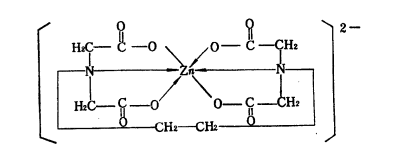 螯合物結構
螯合物結構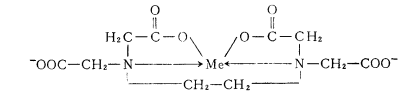 螯合物結構
螯合物結構分子中含有氨基(一NH3)和羧基(一COOH)的絡合劑。試劑分子中含有多個配位原子(O與N),能與大多數金屬離子形成穩定的螫合物(chelate),常用於絡合滴定,最常用的氨羧絡合劑是乙二胺四乙酸(EDTA)。
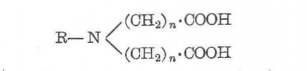 化學通式
化學通式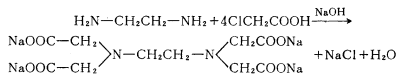 製備EDTA反應方程式
製備EDTA反應方程式 沉澱析出方程式
沉澱析出方程式 螯合物結構
螯合物結構 螯合物結構
螯合物結構有機絡合劑分子中氨氮和羧氧配位原子的配位多元酸,統稱為氨羧絡合劑。...... 有機絡合劑分子中氨氮和羧氧配位原子的配位多元酸,統稱為氨羧絡合劑。...
百里酚酞氨羧絡合劑是一種化學物質,分子式為C38H42N2O12。...... 百里酚酞氨羧絡合劑是一種化學物質,分子式為C38H42N2O12。中文名 百里酚酞氨羧絡合劑 C...
絡合滴定法是以絡合反應為基礎的滴定分析方法稱。它主要以氨羧絡合劑為滴定劑,這些氨羧絡合劑對許多金屬有很強的絡合能力。...
氨三乙酸外觀為白色棱形結晶或粉末,與強氧化劑、鋁、銅、銅合金和鎳不能共存。氨三乙酸能為金屬離子提供四個配位鍵,而且它的分子又較小,因而它具有非常強的絡...
另一種電負性配位體最好為多合配位體的絡合劑:如乙二胺四乙酸二鈉(縮寫為EDTA)、二甲酚橙、氮三乙酸、茜素氨羧絡合劑、1-(2-吡啶偶氮)—間苯二酚(縮寫...
氨羧絡合劑,大多數具有與EDTA相類似的性質,即能與許多金屬離子形成絡合物,只是不同試劑與金屬離子的絡合能力不相同,這便為我們提供了選擇使用這類試劑作為某些金屬...
螯合物常見的螯合劑 編輯 具有多基配位體能與金屬離子起螯合作用,生成螯合物的試劑。在用水廢水化學中,常用的有有機螯合劑,如氨羧絡合劑 (包括氨基三乙酸即NTA...
CyDTA(環己二胺四乙酸)和EDTA一樣,是重要的氨羧絡合劑 。...... CyDTA(環己二胺四乙酸)和EDTA一樣,是重要的氨羧絡合劑 。中文名 CyDTA 外文名 trans-1,...
螯合滴定法:又稱絡合滴定法。是以絡合反應為基礎的容量分析方法,它主要以氨羧絡合劑為滴定劑,較常用氨羧絡合劑有氨三乙酸(NTA)、乙二胺四乙酸(EDTA)、環...
乙二胺四乙酸二鈉二水合物是一種化學物質,分子式是C10H20N2Na2O10。...產品用途:用作氨羧絡合劑,還用於製藥工業、彩色顯影V百科往期回顧 詞條統計 ...
此外,還套用疏代硫酸鹽電鍍銀,氨羧絡合劑-銨鹽電鍍鎘,焦磷酸鹽電鍍銅錫合金等以及其他一些無氰電鍍工藝。無氰電鍍可避免工人受氰化物毒害和污染環境。 [1] ...
外觀呈紅紫色結晶狀,易溶於水,是一種氨羧絡合劑。醫學中用作氫氰酸的解毒劑。...... 外觀呈紅紫色結晶狀,易溶於水,是一種氨羧絡合劑。醫學中用作氫氰酸的...
氟離子與鑭、氟試劑(茜素氨羧絡合劑)在適宜pH下生成藍色三元絡合物,顏色隨氟離子濃度的增加而加深,用或不用含胺類有機溶劑提取,與標準系列比較定量。用含胺類有...
1、用作分析試劑,如非水滴定的溶劑。還用作環氧樹脂固化劑,並用於有機合成及高分子聚合。2.用於非水溶液滴定。氨羧絡合劑。測定銻、鉍、鎘、鈷、銅、汞、銀...
由於稀土離子與氨羧絡合劑具有很強的絡合作用,水相中的氨羧絡合劑能對稀土的萃取分離性能產生較大影響,當水相中加入氨羧絡合劑可顯著提高萃取體系分離稀土的...
枯草桿菌蛋白酶與茜素氨羧絡合劑作用研究,光譜學與光譜分析(SCI收錄),2005,25 (9): 1471-1474.張歡,王興明*,王清成,石榮銘,丁立生. 鹼性介質中茜素黃R與牛...
