基本信息,理論數據,毒理學數據,生態學數據,分子結構數據,計算化學數據,性質與穩定性,主要性質,物理性質,化學性質,危險說明,管制信息,儲存及運輸注意事項,儲存,運輸注意事項,化學特性,氨基磺酸工業化,製法,用途,危險性概述,
基本信息
基本信息
中文名稱:氨基磺酸,AR
中文別名:磺醯胺酸;氨磺酸;磺酸胺;磺酸氨;胺磺酸;氨基磺酸SULFAMIC ACID;亞胺磺酸;氨基磺酸, 98+%;氨基磺酸, 99.99% (METALS BASIS);氨基磺酸, ACS, 99.3-100.3% (ASSAY DRIED BASIS)
英文名稱:Sulfamic acid
英文別名:ACETO ACID; AMIDOSULFONIC ACID; AMIDOSULFURIC ACID; AMINOSULFONIC ACID; BETZ 0254; SULFAMIDIC ACID; SULFAMINIC ACID; SULPHAMIC ACID; aminosulfuricacid; Imidosulfonic acid; Jumbo; Kyselina amidosulfonova; Kyselina sulfaminova; kyselinaamidosulfonova; kyselinaamidosulfonova(czech); kyselinasulfaminova; kyselinasulfaminova(czech); sulfamic; sulphamidic acid
等級:AR
CAS號:5329-14-6
分子式:NH2SO3H
分子量:97.09
 氨基磺酸
氨基磺酸MDL號: MFCD00011603
EC號: 226-218-8
理論數據
毒理學數據
1.急性毒性
LD50:3160mg/kg(大鼠經口);1312mg/kg(小鼠經口)
2.刺激性
家兔經皮:500mg(24h),重度刺激。
家兔經眼:250μg(24h),重度刺激。
生態學數據
1.生態毒性 LC50:70mg/L(96h)(黑頭呆魚)
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
分子結構數據
1、摩爾折射率:16.01
2、摩爾體積(cm3/mol):50.7
3、等張比容(90.2K):161.1
4、表面張力(dyne/cm):101.5
5、極化率(10-24cm3):6.34
計算化學數據
1.疏水參數計算參考值(XlogP):-1.6
2.氫鍵供體數量:2
3.氫鍵受體數量:4
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積88.8
7.重原子數量:5
8.表面電荷:0
9.複雜度:92.6
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.在常溫乾燥的環境中,氨基磺酸比較穩定,只要保持不與水接觸,固體的不吸濕。在高溫時分解,放出氮、硫的氧化物等毒性氣體。氨基磺酸及其鹽類與多種金屬化合物都能生成可溶性鹽類。260℃時分解。溶於水、液氨,微溶於甲醇,不溶於乙醇、乙醚有機溶劑及二硫化碳、液體亞硫酸。水溶液是高電離物。強酸。對有機物的反應性弱,其鹽類易溶於水(除鹼性汞鹽外)。其水溶液煮沸時水解為硫酸銨。有毒!不揮發也不吸濕,在常溫下很穩定。能溶於水,水溶液呈酸性。在沸水中水解生成NH+4和HSO-4。
2.氨基磺酸在空氣中不吸濕,在室溫和乾燥環境下能長期保存。化學性質穩定,其水溶液有較強酸性,對金屬有腐蝕作用。
3.溶解性:溶於水、液氨,微溶於乙醇和甲醇,微溶於丙酮不溶於醚。不溶於有機溶劑。易溶於含氮鹼液和液氮;也可溶於含氮的有機試劑如吡啶等;難溶於乙醇和甲醇。在水中能中等程度溶解,與常見非極性溶劑如THF或甲苯等很難混合。
4.穩定性: 穩定
5.禁配物: 強氧化劑、強鹼
6.避免接觸的條件: 受熱
7.聚合危害: 不聚合
8.分解產物: 硫氧化物、氮氧化物
主要性質
物理性質
熔點:215-225°C (dec.)
水溶性:146.8 g/L (20°C)
外觀:H3NSO3白色斜方晶體。無味無臭,不揮發,不吸濕
相對密度:2.126
熔點:205℃(209℃開始分解,260℃分解放出SO2、SO3、N2和水及其它微量產物)
折射率:α型1.553,β型1.563,γ型1.568
折射係數(25±3℃):1.553~1.568
離解常數:1.10×10-2
生成熱:685.9kJ/mol
溶解性:易溶於水和液氨,在水溶液中呈中等酸性,微溶於甲醇,不溶於乙醇和乙醚。
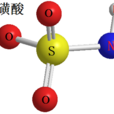
氨基磺酸是偶極體,紅外光譜顯示3個H的化學環境完全相同,3個O的化學環境也完全相同,所以其結構簡式不是H2NSO2OH,而是H3NSO3,即發生了分子內的酸鹼反應。
化學性質
無色斜方晶繫結晶或白色結晶。無臭。溶於水、液氨,微溶於甲醇,不溶於乙醇、乙醚有機溶劑及二硫化碳、液體亞硫酸。水溶液是高電離物。強酸。對有機物的反應性弱,其鹽類易溶於水(除鹼性汞鹽外)。其水溶液煮沸時水解為硫酸銨。
危險說明
危險代碼:Xi
危險等級:R36/38- R52/53
安全等級:S26- S28- S61
管制信息
屬於危險化學品中的酸性腐蝕品。
儲存及運輸注意事項
儲存
密封乾燥保存。密閉包裝,並貯於乾燥通風處。與氧化劑、鹼類等分儲分運。注意個體防護,嚴禁身體直接接觸。誤食,用水漱口,飲牛奶或蛋清。
運輸注意事項
鐵路運輸時應嚴格按照鐵道部《危險貨物運輸規則》中的危險貨物配裝表進行配裝。起運時包裝要完整,裝載應穩妥。運輸過程中要確保容器不泄漏、不倒塌、不墜落、不損壞。嚴禁與氧化劑、鹼類、食用化學品等混裝混運。運輸時運輸車輛應配備泄漏應急處理設備。運輸途中應防曝曬、雨淋,防高溫。
化學特性
氨基磺酸是重要的精細化工產品,廣泛套用於金屬和陶瓷製造的多種工業設備和民用清洗劑、石油並處理劑和清洗劑、電鍍工業用劑電化學拋光用劑、瀝青乳化劑、蝕刻劑、染料醫藥及顏料工業用磺化劑、染色用劑、高效漂白劑、纖維、紙張用阻燃劑、柔軟劑、樹脂交聯促進劑、除草劑、防枯劑以及標準分析試劑等各個領域中。
氨基磺酸可以製成極純的
常溫時穩定的結晶體,其水溶液具有與鹽酸、硫酸同等的強酸性,別名固體硫酸。不揮發,不吸濕,對人身毒性極小,但皮膚不能長時間與氨基磺酸接觸,更不能進入眼睛。氨基磺酸生產工藝過程簡單,反應較容易控制,原料及設備都較容易解決,廢水也容易處理,副產物可以有效利用。該產品可以代替硫酸,其包裝、貯存、運輸都很方便。
氨基磺酸是具有氨基和磺酸基的雙官能團物質,能進行與之有關的許多
化學反應.
1、
分解反應:氨基磺酸在常溫度下很穩定,加熱到209度時開始分解。
2HSO3NH2=SO2+SO3+N2+2H2+H2O
2、與金屬反應 氨基磺酸能與金屬反應,生成鹽和氫氣,但與較活潑金屬反應,氨基的一個氫可被取代,生成雙金屬鹽。
2HSO3NH2+Zn=Zn(SO3NH2)2+H2
HSO3NH2+2Na=NaSO3NHNa+H2
3、與金屬氧化物、氫氧化物和鹽反應。
2HSO3NH2+FeO=Fe(SO3NH2)2+H2O
4、與亞硝酸鹽和硝酸鹽反應。氨基磺酸能被亞硝酸鹽和硝酸鹽迅速氧化。
HNO3+HSO3NH2=H2SO4+N2O+H2O2
HNO2+HSO3NH2=H2SO4+N2+H2O
5、與氧化劑反應。氨基磺酸能被次氯酸氧化,但不能被鉻酸、高錳酸鉀和三氯化鐵氧化。
KClO3+2HSO3NH2=2H2SO4+KCl+N2+H2O
2HOCl+HSO3NH2=HSO3NCl2+2H2O
6、與醇和酚反應
HSO3NH2+ROH→ROSO2ONH4
HSO3NH2+C6H5OH→C6H5OSO2ONH4
7、與胺和醯胺反應
HSO3NH2+RNH2→ RNH3SO3NH2
HSO3NH2+C6H5CONH2→C6H5CONHSO3NH4
8、生成
絡合物氨基磺酸與硫酸鈉反應,生成氨基磺酸絡合物。
6HSO3NH2+5Na2SO4=6HSO3NH2+5Na2SO4+15H2O
9、
水解反應氨基磺酸水溶液加熱至60度以上時,將水解成硫酸鹽
HSO3NH2+H2O=NH4HSO4
氨基磺酸工業化
自從氨基磺酸工業化生產以來,由於套用範圍不斷擴大,產品產量也相應增長。日本在1965年年產量為1.4萬噸,1980年售價每公斤為140~160日元。日本生產廠有富士的日產化學公司,年產7.2千噸;大阪的大喜產業公司,年產3千噸。美國年產量為5萬噸,在1984年每100磅售價為38~41美元。
製法
合成法:將尿素與發煙硫酸在40~70℃進行磺化生成氨基磺酸粗品,然後加水結晶、分離,製得氨基磺酸
用途
氨基磺酸作為清洗劑,因為它是固體,具有貯存、運輸方便,容易配製等很多優點,特別適用遠途使用。
氨基磺酸清洗劑使用範圍很廣,可用於清洗鍋爐、冷凝器、換熱器、夾套及化工管道。在啤酒廠用它清除玻璃襯裡貯罐、鍋、開口啤酒冷卻器,啤酒桶上的垢層;清洗搪瓷廠的蒸發器,以及造紙廠的設備等;在空調方面可除去冷卻系統、蒸發冷凝器的鐵鏽、水垢;海輪用它可清除海水蒸發器(蒸餾設備)、換熱器和鹽水加熱器內的海藻、水垢;可以清洗銅壺、散熱器、餐具洗滌機理、銀器、抽水馬桶、瓷磚、食品和奶酷加工設備的水垢;可以清除沉積在蒸煮器上的蛋白質以及鮮肉、蔬菜、乳酪加工廠中使用的消毒
呂上的沉積物。
美國農業部準許將氨基磺酸用在鮮肉、家禽、兔、蛋加工企業上作酸性清洗劑。
將氨基磺酸溶液注入
碳酸鹽岩產油層。因為氨基磺酸容易和油層岩石起反應,能避免反應生成鹽的沉積,處理費用比用鹽酸略高些,但石油產量倍增。美國用
羥基乙酸鉀48.5%,氨基磺酸3.4%。潤濕劑0.1—3%的水溶液清洗油井套管中的石膏垢層,處理時間約30小時
汽車外殼先電鍍錫-鋅合金,然後上漆,漆膜的粘接力就會增加。
鍍金或合金時普遍採用氨基磺酸,鍍金、銀、金-銀合金的電鍍液是每立升水中含氨基磺酸60~170克。鍍銀女服飾針的典型電鍍液是每立升水中含氨基磺酸125克,可獲得表面非常光亮的鍍銀。在新的含水鍍金電鍍液中鹼金屬氨基磺酸鹽、
氨基磺酸銨或氨基磺酸可作為導電、緩衝作用的化合物使用。
從鍍鎳廢液中回收時是用
陽離子交換樹脂吸附處理而後用氨基磺酸清洗樹脂,使被吸附的解吸出來,樹脂獲得再生。例如處理400ppmNi的電鍍廢液,用150克/升的氨基磺酸50ml,回收的(NH2SO3)2112克/升,NiSO4148克/升。在鍍鎳部件修復時需要鎳上鍍鎳,在其陽極處理時可用100克/升的氨基磺酸處理。在鍍鎳前的鍍鎳表面要用0.003~0.1克分子的氨基磺酸溶液清洗。
鍍銅液的氨基磺酸含量為3~20升,氨基磺酸的作用是使鍍層細密而富有延展性,其粘度力高。
鍍銥時NH2SO3H/Ir≥7,獲得的銥鍍層無裂紋,銥層厚15微米,粘接力大,該產品有自動抗污染設備中顯示出良好的活性。
在銀器、電器元件上鍍銠-錸合金時,電渡液中含氨基磺酸為100克/升,當鍍層厚為≤5微米時就有很高硬度和很強的耐腐蝕性,而且電鍍層非常光亮,美觀。
在黃銅上光潔美觀的銠-錸電渡層硬度高,耐腐蝕,電鍍液含氨基磺酸100克/升,
濃硫酸50克/升,銠(如
硫酸鹽)2克/升,錸〔如K3N(RuCl4H2O2)2〕0.05克/升,在65℃和1~2安/分米2的條件,沉積速度3~4毫克/安分。
義大利已使用氨基磺酸鉛浴代替氟矽酸浴,可減少污染。在防蝕鋁工業上有多種用途。產品光澤好,加工性能優良。
氨基磺酸是價廉易得和穩定性好的固體酸,對有機酸的酯化反應具有很好的催化效果,且不腐蝕設備
危險性概述
毒性防護:該品低毒。對皮膚和眼睛有一定的刺激作用。生產設備應密閉,操作人員應穿戴好防護用具
安全:粉塵或溶液對眼及皮膚有刺激性,能造成灼傷。最高容許濃度10mg/m3。眼受刺激時須用水沖洗,重者應就醫診治。皮膚接觸時也套用水沖洗,再用肥皂徹底洗滌。入口時,應立即漱口,速送醫院診治。用內襯聚乙烯塑膠袋的木箱包裝,每箱淨重25kg。貯存在陰涼、通風、乾燥處。包裝應密封,注意防潮。運輸過程中要防雨淋和日光曝曬。對逸出物料處置時須戴好防毒面具與手套,用砂土混合掃起或用水沖洗。失火時,可用水、砂土和滅火器撲救。
 氨基磺酸
氨基磺酸