NKK氨法
NKK氨法是日本鋼管公司開發的工藝,該工藝流程主要分三部分,即SO2的吸收、 (NH4)2SO3氧化、(NH4)2SO4結晶。
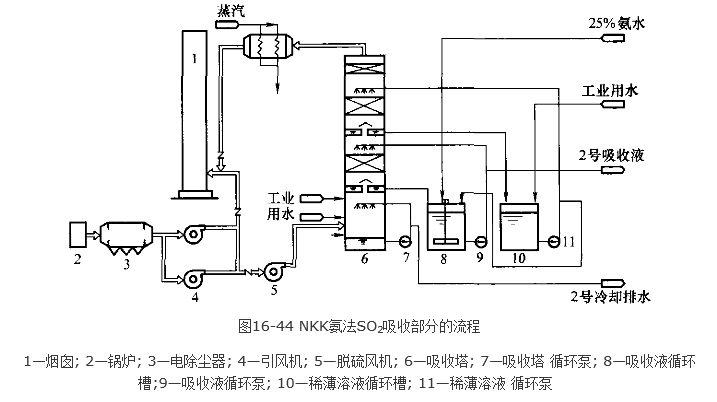
NKK氨法套用塔型為填料塔,填料為聚丙稀格柵式。該塔有一定的特點,按其功能可 分三段。下段(從塔底開始) 是預洗滌段,主要作用是除塵和降溫,在這階段不加吸收劑 NH3; 中段是第一吸收段,加有吸收劑NH3; 上段為第二吸收段,沒有NH3加入,僅用工 業水來洗滌。
NKK氨法對 (NH4)2SO3的氧化在單設一台氧化在反應器中進行。其氧化用氧由壓縮 空氣補充,氧化後的餘氣 (含有SO2和NH3) 排入系統中,。壓縮空氣壓力為 0.5~1.0MPa。
GE公司氨法
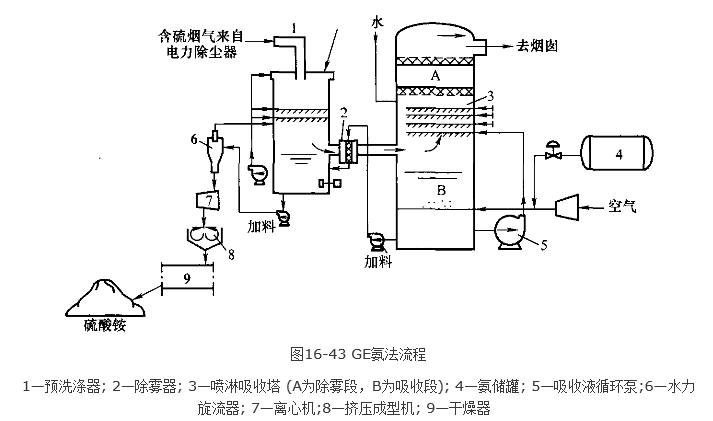
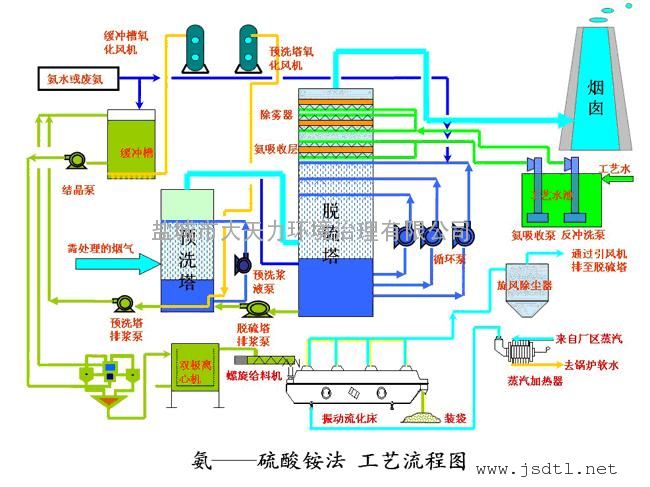
GE公司氨法的工藝流程如圖所示,主要由預洗滌、SO2吸收、亞硫酸銨氧化和 結晶四個工序構成所需工藝系統。
(1) 煙氣系統。煙氣經過靜電除塵器除塵後,進入煙氣預洗滌段,由於預洗滌段也具有 對SO2的吸收作用,所以該技術也可視為兩段吸收或稱雙循環吸收。煙氣在預洗滌器中能 起脫除SO2的作用,但其吸收量較小,這是由預洗滌器尚未通入氨氣,其pH值小於2所 致。煙氣經過預冷卻器冷卻飽和後進入吸收塔,經氨水洗滌脫硫,淨化後煙氣經除霧器除去水滴,由煙囪排出。
(2) SO2吸收系統。氨法SO2吸收反應在SO2吸收塔中進行。來自預洗滌器的已被冷 卻飽和的煙氣進入SO2吸收塔,煙氣與噴淋的氨液逆向流動接觸,SO2與稀硫酸銨液反應, 生成 (NH4)2SO3或硫化氫。稀硫酸液靠漿液循環泵進行循環。對於 (NH4)2SO3的氧化工 序,是在吸收塔底部進行的,生成(NH4)2SO4。液氨是通過減壓蒸發後同空氣同時送入塔 底,以維持吸收液的pH值。
根據GE公司提供的試驗數據,吸收液中 (NH4)2SO4的濃度是熱煙氣溫度和SO2含量 的函式,即使煙氣中SO2濃度高達6 100mg SO2/kg煙氣,吸收液中 (NH4)2SO4的濃度也 不會超過30% (質量)。為排出已產生的 (NH4)2SO4,從吸收塔底部排出適量的吸收液,但同時必需以自動補 水方式來維持恆定的液位。
(3) 硫酸銨回收系統。預洗滌段硫酸銨結晶液和吸收段硫酸銨結晶液先經旋流器濃縮, 經離心機脫水,使含水量小於2%,回收。
NADS脫硫淨化技術
NADS (Novel Ammonia De—Sulphurization,氨—肥法) 是由中國華東理工大學開發成功的一種新的脫硫方法,它是採用氨來吸收煙氣中的SO2,可根據不同情況生成 NH4HSO3、(NH4)2SO3,結合化肥生產,將脫SO2產物生成硫氨、磷銨或硝銨等化肥,並 生產工業用高濃度硫酸。
相關化學反應:
SO2+xNH3+H2O⇌ (NH4)xH2-xSO3
上式中x值現有氨法中x=2,而NADS法的x=1.2~1.4。
NADS除能生產 (NH4)2SO4,同時也可與磷銨化肥廠或硝銨化肥廠聯合生產 (NH4)3PO4、NH4NO3及工業高濃度硫酸,其反應如下
2(NH4)xH2-xSO3+xH2SO4⇌x(NH4)2SO4+2SO2↑+2H2O
(NH4)xH2-xSO3+xH3PO4⇌xNH4H2PO4+SO2↑+H2O
(NH4)xH2-xSO3+xHNO3⇌xNH4NO3+SO2↑+H2O
SO2+1/2O2+H2O⇌H2SO4+熱量
工藝流程
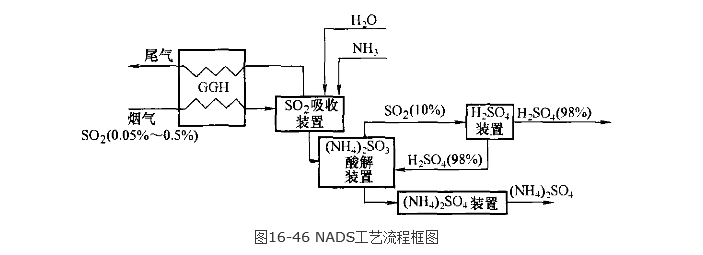
以硫酸銨—硫酸為例, NADS的工藝流程如圖16-46 所示。由靜電除塵器來的煙先 經GGH,冷段降溫 (由140~ 160℃) 冷卻到小於80℃進入 SO2吸收塔,吸收塔內吸收溫 度約45~60℃之間,SO2的吸 收率大於95%。
吸收塔內煙氣中SO2與NH3和H2O的吸收結合生成含有 (NH4)2SO3,NH4HSO3和 少量Na2SO4的過程與其他氨法一樣,在NADS技術中NH3和H2O是分別進入吸收塔,這 樣做有三大好處:
(1) 吸收塔出口NH3含量低,氨損耗小。
(2) 吸收液循環量小,氣液比大,能耗低。
(3) 生成 (NH4)2SO3濃度高,有利於硫銨化肥生產,節約成本。
混合液中,總鹽含量約為30%~50%,具體值與煙氣中的SO2濃度有關,淨化後煙氣 中含SO2量約為10~100mL/m。
NADS法中吸收系統阻力通常在1.96~2.9kPa之間,引風機富餘壓頭難以滿足,需裝 增壓風機。
吸收SO2後產生的亞硫酸銨漿液用其酸解裝置,硫酸生產裝置和硫酸銨生產裝置來完 成後續工序。
(1) 亞硫酸銨溶液酸解裝置。該裝置是將 (NH4)2SO3(包括NH4HSO3) 與H2SO4 (或者H3PO4、HNO3) 反應,生成 (NH4)2SO4(或NH4H2PO4、NH4NO3) 溶液和SO2 氣體,同時酸解過程送入空氣,使得SO2在空氣混合物中濃度達10%~20% (質量)。酸解 中硫酸原料的濃度為98% (質量),酸解是放熱反應,溫度可達70~80℃,所以SO2解析 不需外部熱源。最後,用氨調節pH值,中和富餘的硫酸。
(2) 硫酸生產裝置。包括SO2催化氧化 (催化劑為V2O5/SiO2) 為SO2的轉化器和換 熱器,SO2氣體乾燥塔和SO2氣體吸收塔及酸循環槽等設備。
(3) 硫酸銨生產裝置。硫酸銨溶液經蒸發、分離、乾燥,包裝出廠。
篩板塔
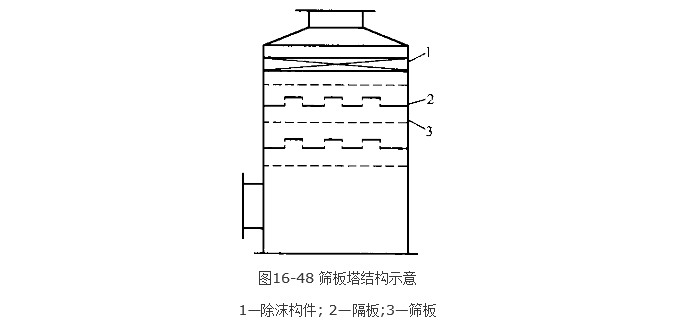
NADS技術採用的是篩板塔。它用的是一種大孔徑、高開孔率篩板做傳質元件,具有 阻力小 (0.15~0.3kPa) 的特點,是傳統板式塔的50%; 空塔氣速可達4m/s,是傳統板式 塔兩倍。塔體可由耐熱玻璃鋼製造。
NADS技術氣液接觸方式是噴霧方式,且可一塔多級吸收,圖16-48為二層隔板,三層 篩分段吸收。段層數視系統需要而增減。
氨—亞銨法
氨—亞銨法是直接吸收SO2後的母液加工成產品——亞硫酸銨 (簡稱亞銨)。亞銨可替 代燒鹼用於製漿造紙工業。該法工藝流程簡單,它可用氣氨、氨水及碳酸氫銨作氨源,取材靈活。
反應原理
用碳酸氫銨溶液吸收SO2,主要反應為:
2NH4HCO3+SO2→ (NH4)2SO3+H2O+2CO2
(NH4)2SO3+SO2+H2O→2NH4HSO3
煙氣中一般含一定量的氧,在溶液中還會發生副反應:
(NH4)2SO3+1/2O2→ (NH4)2SO4
對於硫酸尾氣,含有少量SO3,會發生如下反應:
2 (NH4)2SO3+SO3+H2O→ (NH4)2SO4+2NH4HSO3
吸收SO2後,母液主要含NH4HSO3,加固體NH4HCO3中和,可析出亞銨晶體,反應如下:
NH4HSO3+NH4HCO3→ (NH4)2SO3+CO2+H2O
此反應為吸熱反應,溶液不經 冷卻即可降至0℃左右。
工藝流程
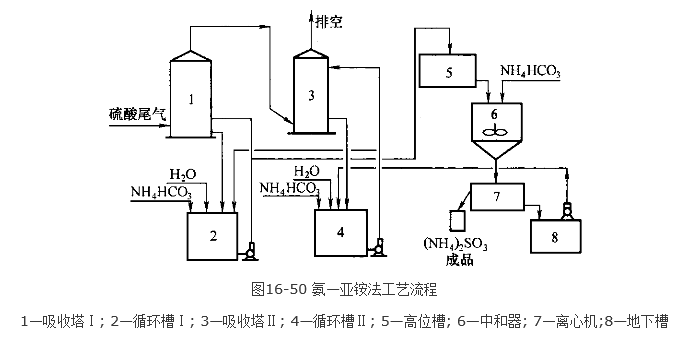
氨—亞銨工藝 流程見圖16-50,全部工藝可分為吸 收、中和、分離、氧化四個階段。
1) 吸收。含SO2的氣體依次進 入串連的吸收塔Ⅰ和Ⅱ,在塔內SO2 被循環噴淋的吸收液吸收後排放。 在第Ⅰ塔中吸收液儘量保持較高的 濃度,以便生成較多的NH4HCO3, 並不斷抽取部分溶液送至中和工序, 以便製取固體 (NH4)2SO3產品。在 第Ⅱ塔中,吸收液濃度可降低些,保持高鹼度,使(NH4)2SO3含量高些。為保持各塔循環液鹼度和液位不變,要不斷地補充 固體NH4HCO3。
2) 中和。由於NH4HSO3比 (NH4)2SO3 在水中溶解度大,第Ⅰ塔引出高濃 度NH4HSO3溶液,在中和器內加入NH3HSO3 進行反應,反應後NH4HSO3轉化成 (NH4)2SO3,而(NH4)2SO3的溶解度小,大量 晶體析出。
3) 分離。由中和器底部引出含有 NH4HSO3·H2O晶體的懸浮液通過離心機分 離,分離出白色固體NH4HSO3·H2O產品,濾 液送回第Ⅱ塔繼續吸收。
4) 氧化。煙氣中存在氧對NH4HSO3氧化率可達5%~14%,而晶體亞銨氧化成為硫 銨氧化率一般為0.3%~7%,最高可達50%。