預防及治療免疫功能缺陷病人的巨細胞病毒感染,如愛滋病患者,接受化療的腫瘤患者,使用免疫抑制劑的器官移植病人。
基本介紹
- 中文名:更昔洛韋
- 外文名:ganciclovir
- 製劑規格:每小瓶含有540 mg凍乾
- 藥物別名:賽美維、麗科偉 Cymevene
化合物簡介
基本信息
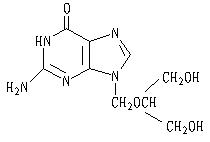
預防及治療免疫功能缺陷病人的巨細胞病毒感染,如愛滋病患者,接受化療的腫瘤患者,使用免疫抑制劑的器官移植病人。

方法名稱: 更昔洛韋原料藥—更昔洛韋的測定—非水滴定法套用範圍: 本方法採用滴定法測定更昔洛韋原料藥中更昔洛韋的含量。本方法適用於更昔洛韋原料藥。...
更昔洛韋片,更昔洛韋片用於免疫功能損傷引起巨細胞病毒感染的患者。1、用於免疫功能損傷(包括愛滋病患者)發生的巨細胞病毒性視網膜炎的維持治療。2、預防可能發生於器官...
注射用更昔洛韋,用於預防和治療危及生命或視覺的受巨細胞病毒感染的免疫缺陷病人,以及預防與巨細胞病毒感染有關的器官移植病人。...
更昔洛韋注射液,適應症為僅用於:1、免疫功能缺陷者(包括愛滋病患者)發生的巨細胞病毒性視網膜炎。2、預防可能發生於接受器官移植者的巨細胞病毒感染。...
更昔洛韋分散片,適應症為本品用於免疫損傷引起巨細胞病毒感染的患者。1、用於免疫功能損傷(包括愛滋病患者)發生的巨細胞病毒性視網膜炎的維持治療。2、預防可能發生乾...
更昔洛韋膠囊,適應症為本品用於免疫損傷引起巨細胞病毒感染的患者。 1、於免疫功能損傷(包括愛滋病患者)發生的巨細胞病毒性視網膜炎的維持治療。 2、預防可能發生於...
注射用更昔洛韋鈉,適應症為僅用於:1.免疫功能缺陷者(包括愛滋病患者)發生的巨細胞病毒性視網膜炎。2.預防可能發生於接受器官移植者的巨細胞病毒感染。...
更昔洛韋滴眼液,適應症為廣譜抗皰疹病毒藥。用於治療單純皰疹性角膜炎。...... 因未進行專項研究,尚不清楚滴眼液與其它滴眼液的相互作用;但文獻報導更昔洛韋靜脈給藥與...
更昔洛韋鈉,化學藥品,分子式:C9H112N5NaO4。...... 中文名稱:更昔洛韋鈉 [1] 中文別名:9-(1,3-二羥基-2-丙氧甲基)-鳥嘌呤鈉英文名稱:Ganciclovir sodium...
三乙醯更昔洛韋InChI編碼 編輯 1S/C15H19N5O7/c1-8(21)17-15-18-13-12(14(24)19-15)16-6-20(13)7-27-11(4-25-9(2)22)5-26-10(3)23/h6,...
纈更昔洛韋為合成的2-脫氧鳥苷類似物,是抗病毒藥更昔洛韋(ganciclovir)的前體藥物,可大大減少更昔洛韋的毒性。它的藥效學特點與更昔洛韋相同。...
更昔洛韋眼膏,適應症為廣譜抗皰疹病毒藥。用於治療單純皰疹性角膜炎。...... 更昔洛韋眼膏,適應症為廣譜抗皰疹病毒藥。用於治療單純皰疹性角膜炎。 藥品名稱 更昔洛韋...
鹽酸纈更昔洛韋片,適用於治療獲得性免疫缺陷綜合症(AIDS)患者的巨細胞病毒(CMV)視網膜炎。適用於預防高危實體器官移植患者的CMV感染。...
更昔洛韋葡萄糖注射液,適應症為本品僅用於:1、預防可能發生於有巨細胞病毒感染風險的器官移植受者的巨細胞病毒病。2、治療免疫功能缺陷患者(包括愛滋病患者)發生的...
更昔洛韋鈉氯化鈉注射液,本品僅用於:1、預防可能發生於有巨細胞病毒病風險的器官移植受者的巨細胞病毒病。2、治療免疫功能缺陷者(包括愛滋病患者)發生的巨細胞病毒...
Cbz-纈更昔洛韋是一種化學品,化學式是C22H28N6O7。...... Cbz-纈更昔洛韋是一種化學品,化學式是C22H28N6O7。中文名 Cbz-纈更昔洛韋 英文名 Cbz-Valine ...
更昔洛韋氯化鈉注射液,適應症為僅用於1、免疫功能缺陷者(包括愛滋病患者)發生的巨細胞病毒性視網膜炎。 2、預防可能發生於接受器官移植者的巨細胞病毒感染。...
2.交叉過敏:對其他鳥嘌呤類抗病毒藥(如阿昔洛韋、更昔洛韋、泛昔洛韋)過敏者也可對本藥過敏。3.藥物對妊娠的影響:本藥對動物無致畸性,但疾病控制和預防中心不...
更昔洛韋眼用凝膠,用於治療單純皰疹病毒性角膜炎。...... 更昔洛韋眼用凝膠孕婦及哺乳期婦女用藥 動物實驗表明,更昔洛韋口服和靜脈給藥有致畸和生殖毒性,故孕婦應權衡...
存活的原因是該例患者在肝移植後使用了更昔洛韋/泛昔洛韋治療,HBV DNA陰轉。泛昔洛韋治療已達26個月,再次肝移植3年後,患者仍正常。作者認為,肝移植後長期使用...
Cbz-單甲醯纈更昔洛韋是一種化學物質,分子式是C23H28N6O8。...... Cbz-單甲醯纈更昔洛韋是一種化學物質,分子式是C23H28N6O8。中文名 Cbz-單甲醯纈更昔洛韋 ...
更昔洛韋鈉注射液,1.免疫功能缺陷者包括愛滋病患者發生的巨細胞病毒性視網膜炎。 2.預防可能發生於接受器官移植者的巨細胞病毒感染。...
編輯 1.對更昔洛韋過敏者也可能對本品過敏。2.脫水或已有肝、腎功能不全者慎用。腎功能不全者在接受本品治療時,需根據肌酐清除率來校正劑量。3...
1.對更昔洛韋過敏者也可能對本品過敏。 2.脫水或已有肝、腎功能不全者需慎用。 3.嚴重免疫功能缺陷者長期或多次套用本品治療後可能引起單純皰疹病毒和帶狀皰疹...
賽美維(注射用更昔洛韋),用於預防和治療危及生命或視覺的受巨細胞病毒感染的免疫缺陷病人,以及預防與巨細胞病毒感染有關的器官移植病人。...
萬賽維(鹽酸纈更昔洛韋片),適應症為鹽酸纈更昔洛韋片適用於治療獲得性免疫缺陷綜合症(AIDS)患者的巨細胞病毒(CMV)視網膜炎。鹽酸纈更昔洛韋片適用於預防高危實體器官...
林可宏™(注射用更昔洛韋鈉),適應症為僅用於:1.免疫功能缺陷者(包括愛滋病患者)發生的巨細胞病毒性視網膜炎。2.預防可能發生於接受器官移植者的巨細胞病毒感染。...
麗科明(更昔洛韋眼用凝膠),適應症為單純皰疹病毒性角膜炎。...... 麗科明(更昔洛韋眼用凝膠),適應症為單純皰疹病毒性角膜炎。 藥品名稱 麗科明 藥品類型 處方藥、...
麗科樂(更昔洛韋膠囊),適應症為本品用於免疫損傷引起巨細胞病毒感染的患者。 1、於免疫功能損傷(包括愛滋病患者)發生的巨細胞病毒性視網膜炎的維持治療。 2、預防...
