利用氧化還原反應在非水溶液中進行容量分析的方法,1935年由K.費歇爾提出,主要用於微量水分的測定。
基本介紹
- 中文名:卡爾·費歇爾滴定
- 化學式:I2+SO2+H2O─→2HI+SO3
- 原理:二氧化硫、碘與水反應
- 干擾物質:氧化劑和還原劑
- 運用:用於多種物質中水分的測定
原理,卡爾·費歇爾試劑,干擾物質,套用,展望,
原理
(圖1)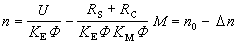 (圖1)
(圖1)
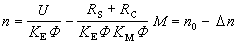 (圖1)
(圖1)在吡啶和甲醇存在下,二氧化硫、碘與水發生反應:
I2+SO2+H2O─→2HI+SO3
吡啶和甲醇參與的反應為:(圖1)
總的反應為:(圖2)
吡啶的作用是使反應產物與之結合成鹽,使反應能夠順利進行,甲醇則與吡啶-三氧化硫結合物反應,生成穩定的甲基硫酸氫吡啶。
卡爾·費歇爾試劑
一般的配製方法為將碘溶於吡啶中,做為儲備液,此溶液穩定,於套用前,將此溶液用甲醇稀釋,並加入二氧化硫,使三者的摩爾比為:
碘:二氧化硫:吡啶=1:3:10
並使每毫升試劑相當於2~5毫克水。常用的配方是84.7克(0.33摩爾)碘溶於269毫升(3.3摩爾)無水吡啶中,加667毫升無水甲醇,將此溶液置於冰浴中,緩緩通入二氧化硫氣體或加入液態二氧化硫,至重量增加64克(1摩爾)為止。甲醇是配製此試劑的最常用溶劑,因它對一般樣品和反應產物的溶解度均較好;其他醇類如乙二醇等也可套用。配好的溶液不穩定,放置時會分解,開始分解較快,過幾十小時後逐漸變慢,即可套用。用時應同時以水標定,常用的標準是水的甲醇溶液,也可用含已知結晶水量的有機酸鹽類(如二水合酒石酸鈉)做為標準。因系用於水的測定,所以所用的試劑、溶劑等均須預先經脫水處理,容器也必須乾燥,儲存與使用過程均應採取防潮措施,不使空氣中水分進入試劑,並應對所用溶劑進行空白滴定,以求得其含水量。
滴定時,一般將樣品溶於甲醇中,以此試劑滴定至水全部反應完畢,溶液出現終點,其中以死停終點法(見庫侖滴定法)最為常用。以兩根鉑絲為電極,外加幾十毫伏的電壓,終點前溶液中只有I-存在,電極間無電流通過,終點後由於有過量的碘存在,I2-I-偶對在電極反應,產生電流,可用微安表檢出。也可用回滴法,即加入過量試劑,而以標準水溶液滴定,至兩電極間無電流通過為止。
此試劑中每摩爾碘所能滴定的水的量總是小於按上述反應式的計算值,因為配製的溶液不穩定,放置時不斷分解,一般在一個月即損失一半左右,其分解反應為: SO2+I2+2CH3OH─→2HI+CH3SO4CH3或:(圖3)
因此試劑配製後放置時間較長即會失去效用。為克服此缺點,可將此試劑分開配製成兩種溶液,分別存放,均較穩定。第一種溶液中含吡啶、二氧化硫和甲醇,第二種溶液為碘的甲醇溶液。使用時,或事先將二液混合,放置過夜後用作滴定劑;或將樣品溶於第一種溶液中,以第二種溶液進行滴定。存放與使用時,仍須注意防止甲醇吸收空氣中的水分及溶液中碘的揮發。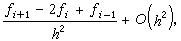 (圖3)
(圖3)
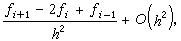 (圖3)
(圖3)干擾物質
氧化劑和還原劑 由於試劑含有碘和二氧化硫,所以如果樣品中含有能與此二者反應的還原劑或氧化劑時,會發生干擾而引起誤差。如果幹擾物質與碘的反應遵循化學計量比例,則可另取一份樣品溶於甲醇-吡啶溶液中,以碘的甲醇溶液滴定,從而可以求出干擾物消耗的碘量而加以校正。
鹼性氧化物與氫氧化物 這些化合物均能與試劑中的碘、二氧化硫和甲醇發生反應,其反應與水的反應相似,如:
MO+I2+SO2+CH3OH─→MI2+CH3HSO4
如果存在著Ag2O、MgO、CaO、ZnO、HgO等,則它們與碘和二氧化硫的反應也是化學計量的,因此可以求出消耗試劑的量而加以校正。
一些易分解的弱酸鹽 例如碳酸鈉、碳酸氫鈉、亞硫酸鈉等,也可與試劑反應,引起誤差。
醛、酮、甲酸 這些化合物均可緩慢與甲醇反應,生成縮醛和水。為去除干擾,可以使用含有少量甲醇及大量吡啶的特製試劑,或使羰基與氫氰酸反應。
有一種常用的去除干擾物質的方法是將水蒸餾出來,如與苯或甲苯共同蒸餾,則水與苯或甲苯形成共沸物,有最低沸點,從而可與其他化合物分離。收集蒸餾液進行滴定,即可測得水分含量。
套用
測定物質中的水分含量 包括有機溶劑、各類化合物、有機酸鹽和無機化合物中的結晶水等。樣品如不溶於甲醇,有時也可將其粉碎後懸浮於甲醇中進行滴定。強吸附劑如矽膠、氧化鋁中的水分也可如此測定。
測定反應產生的水分或反應中消耗的水分 可用來間接測定某些化合物的含量,例如:
①醇類 伯、仲、叔醇均可與乙酸反應產生酯和水:
ROH+CH3COOH─→CH3COOR+H2O
式中R為烷基。此反應在65℃和三氟化硼催化下,於2小時內完成。加入吡啶,與三氟化硼結合後,即可用卡爾·費歇爾試劑滴定生成的水分,從而求出醇量。
②脂肪酸類 使脂肪酸與甲醇在三氟化硼催化下反應,然後滴定生成的水分。芳香酸反應不完全,不能用此法測定。
③酸酐類 可加入略為過量的水,與酸酐反應,並以三氟化硼或碘化鈉催化,在60℃,1~2小時可反應完全,然後加入吡啶,使它與三氟化硼結合而失去催化能力,過量的水用卡爾·費歇爾試劑滴定,可求出酸酐含量。
④胺類 伯胺、仲胺可與乙酸酐反應,過量酸酐再按上述方法測定,伯胺也可與苯甲醛反應生成水分:過量的苯甲醛用氰化鈉及氫氰酸的吡啶溶液反應去除,生成的水用卡爾·費歇爾試劑滴定。 (圖4)
(圖4)
 (圖4)
(圖4)⑤醛類和酮類 利用羥胺與羰基的反應:
過量的羥胺加二氧化硫的吡啶溶液進行反應除去後,用卡爾·費歇爾試劑滴定生成的水分。
(圖5)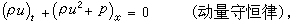 (圖5)
(圖5)
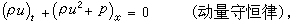 (圖5)
(圖5)⑥腈類 利用水解反應,加入過量水,使發生以下反應:
RCN+H2O─→RCONH2
以三氟化硼的乙酸溶液催化,在80℃反應2小時後,加入吡啶,滴定剩餘的水,由消耗的水量求出腈的含量。
