概述,發展歷史,分類,結構和功能,IL-1,IL-2,IL-3,IL-4,IL-5,IL-6,IL-7,IL-8,IL-9,IL-10,IL-11,IL-12,IL-13,IL-14,IL-15,IL-16,IL-17,IL-18,IL-19,IL-20,IL-21,IL-22/IL-TIF,IL-23,IL-24/MDA-7,IL-25(IL-17E),IL-26,IL-27(IL-30),IL-28,IL-29,IL-31,IL-32,IL-33(IL-1F11),IL-34,IL-35,IL-37,IL-38,種內同源分子和種屬間差異,白細胞介素2,白細胞介素3,白細胞介素4/5,白細胞介素6,白細胞介素13,白細胞介素16,白細胞介素21,白細胞介素34,白細胞介素38,白細胞介素-1家族,白細胞介素-17家族,研究意義,白細胞介素1,白細胞介素12,套用,白細胞介素2,白細胞介素3,
概述
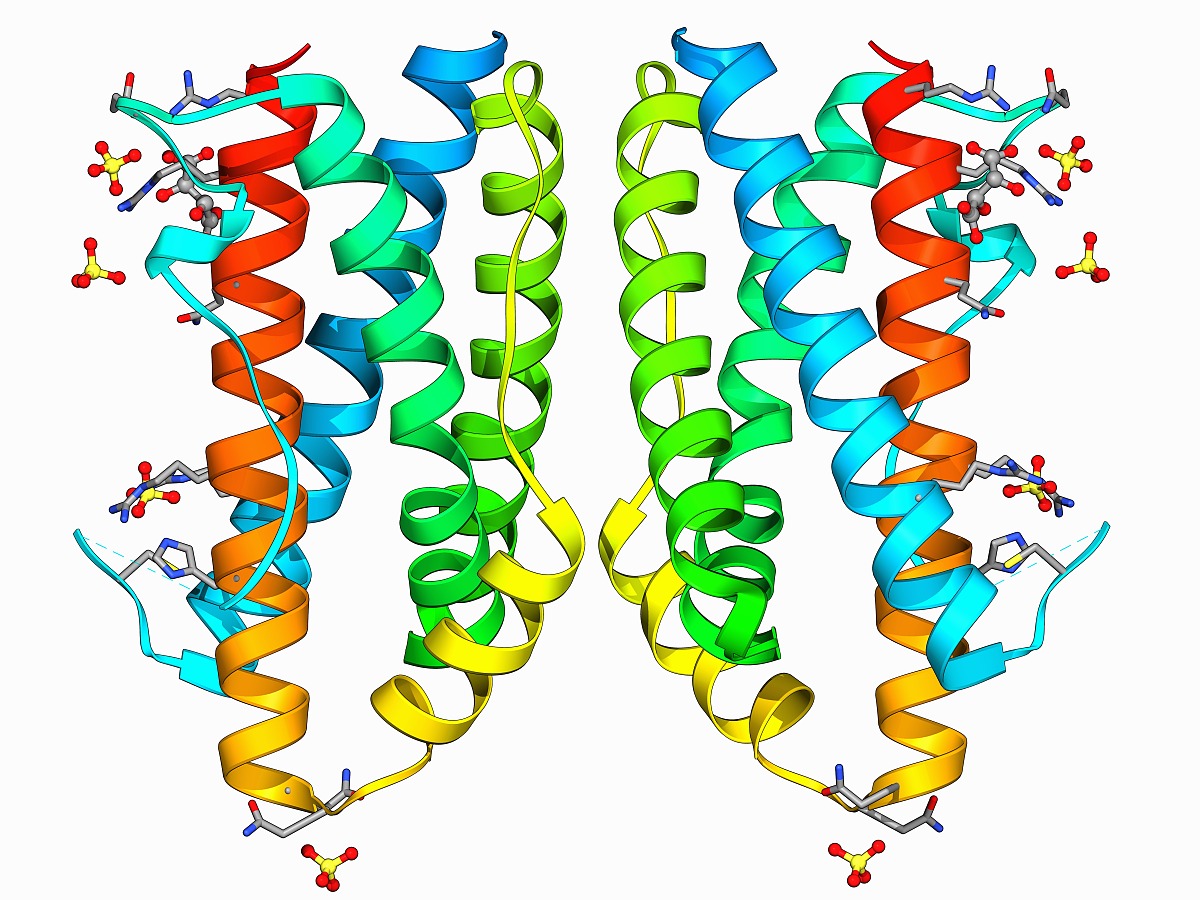
白細胞介素是由多種細胞產生並作用於多種細胞的一類
細胞因子。由於最初是由白細胞產生又在白細胞間發揮作用,所以由此得名,現仍一直
沿用。最初指由白細胞產生又在白細胞間起調節作用的
細胞因子,現指一類分子結構和生物學功能已基本明確,具有重要調節作用而統一命名的細胞因子,它和血細胞生長因子同屬細胞因子。兩者相互協調,相互作用,共同完成造血和免疫調節功能。白細胞介素在傳遞信息,激活與調節免疫細胞,介導T、B細胞活化、增殖與分化及在炎症反應中起重要作用。
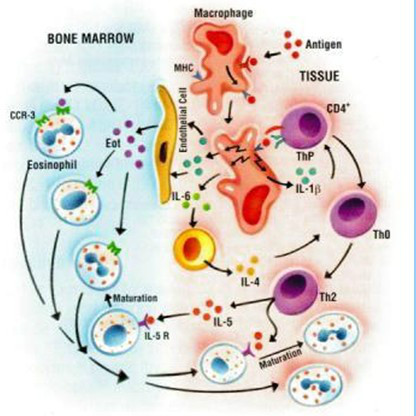 信號傳遞
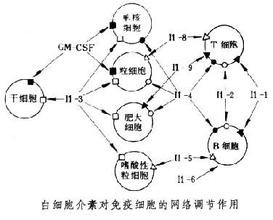
信號傳遞白細胞介素interleukin 縮寫為IL,功能關係
免疫反應的表達和調節,這種調節有來源於淋巴細胞或巨噬細胞等的許多因子參與。來源於淋巴細胞的有淋巴細胞活素,來源於巨噬細胞的總稱為monokine,其中的各個因子的生物活性各有不同(例如巨噬細胞活化,促進T細胞繁殖等),因子自身的物理化學性質多不清楚。
在對
免疫應答的研究過程中,在
絲裂原刺激的細胞培養上清中發現了許多具有生物活性的分子,研究者各以自己測得的活性進行命名,十幾年報導了近百種因子。後來藉助
分子生物學技術進行比較研究發現,以往許多以生物活性命名的因子實際上是具有多效性的同一物質。
發展歷史
1979年,為了避免命名的混亂,第二屆國際
淋巴因子專題會議將免疫應答過程中白細胞間相互作用的細胞因子統一命名為白細胞介素(interleukin,IL),在名稱後加阿拉伯數字編號以示區別,例如IL-1、IL-2……,新確定的因子依次命名。只有取行克隆化的基因、明確產物的性質和活性才能得到國際會議的認可。這些物質在
淋巴細胞活素及
巨噬細胞因子(monoki-ne)中,已作為一種分子提純並弄清了性質。最初測定的物質為 IL1和IL2。IL1屬於monokine,以前曾以淋巴細胞活化因子(lymphocyte activating factor)命名。細胞促進蛋白質(mitogenic protein)以及
B細胞活化因子(B cell-activating factor)等七種名稱稱之。而IL2屬於淋巴細胞活素,以前曾以
胸腺細胞刺激因子(thymocyte stimulating factor)、
T細胞生長因子(T cell growth factor)等六種名稱稱之。
1987年人
IL-3克隆成功,並產生重組IL-3。
1995年國際免疫學學會聯合會根據IL-16基本結構和基因順序,將IL-16正式命名。
2001年,Lee等首先報導了IL-17E的cDNA和胺基酸序列。
截至2013年12月,得到承認的成員至少達38個。
分類
分類 | 簡介 | 成員 |
白細胞介素-1家族 | 白細胞介素-1家族(interleukin-1 family, IL-1F)有11個成員,可稱作IL-1F1~IL-1F11;其中絕大多數是促炎性細胞因子,主要通過刺激炎症和自身免疫病相關基因的表達,誘導環氧化酶2、磷脂酶A2、一氧化氮合酶、干擾素γ、黏附分子等效應蛋白的表達,在免疫調節及炎症進程中扮演著重要的角色;多數經典家族成員的受體、信號傳導和功能已經得到了廣泛而深入的研究 | IL-1α、IL-1β、IL-1受體拮抗劑(IL-1 receptorantagonist, IL-1Ra)、IL-18、IL-36Ra、IL-36α、IL-37、IL-36β、IL-36γ、IL-38和IL-33 |
白細胞介素-2家族(γc家族) | 有5個成員,是信號傳導都依賴於γc鏈 (commonγ chain)的一組細胞因子 | IL-2,IL-4,IL-13,IL-15和IL-21 |
趨化因子家族 | IL3和一些不屬於白細胞介素的細胞因子歸類為趨化因子家族 | IL-3 |
趨化因子家族C-X-C/α亞族 | IL8和一些不屬於白細胞介素的細胞因子歸類為趨化因子家族此亞族 | IL-8 |
白細胞介素-12/白細胞介素-6家族 | 白細胞介素12家族/白細胞介素6家族包含5個成員 | IL6,IL12,IL23,IL27(即IL30),IL35 |
白細胞介素-10家族 | IL-10家族是Ⅱ類細胞因子的一個亞家族,對免疫系統發揮著多種多樣的調節作用 | IL-10,IL-19,IL-20,IL-22/IL-TIF和IL-24/MDA-7、IL-26等 |
白細胞介素-17家族 | 白細胞介素17家族有兩個白介素成員 | IL17,和IL25即(IL17E) |
其他 | 其餘的白細胞介素不明確屬於任何一個家族 | IL5,IL7,IL9,IL11,IL14,IL16,IL31,IL32 |
結構和功能
IL-1
IL-1(
白細胞介素-1)又名淋巴細胞刺激因子。主要由活化的單核-巨噬細胞產生。
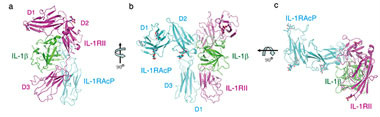 白細胞介素1(IL-1)結合併激活其受體
白細胞介素1(IL-1)結合併激活其受體結構:有IL-1α和IL-1β兩種存在形式。
功能:局部低濃度時協同刺激
抗原呈遞細胞(Antigen-presenting cells, APC)和T細胞活化,促進B細胞增殖和分泌抗體,進行免疫調節。大量產生時有內分泌效應:誘導肝臟
急性期蛋白合成,引起發熱和
惡病質。
生物學活性:1.局部作用局部低濃度的IL-1主要發揮免疫調節作用。①與抗原協同作用,可使CD4+T細胞活化,IL-2R表達;②促進B
細胞生長和分化,可使脾細胞的溶血空斑數(PFC)增加100倍,這說明IL-1也促進抗體的形成;③促進單核-巨噬細胞等APC的
抗原遞呈能力;④與IL-2或
干擾素協同可以增強NK細胞活性;⑤吸引中性粒細胞,引起
炎症介質釋放;⑥可刺激多種不同的
間質細胞釋放蛋白分解酶並產生一些效應;例如
類風濕關節炎的滑膜病變(膠原破壞、骨質重吸收等)就是由於
關節囊內Mφ受刺激後活化並分泌IL-1,使局部組織間質細胞分泌大量的前列腺素和膠原酶,分解破壞滑膜所致;⑦IL-1對軟骨細胞、成纖維細胞和骨代謝也均有一定影響。2.全身性作用動物實驗證明,IL-1的大量分泌或注射可以通過血循環引起全身反應。①作用於
下丘腦可引起發熱,具有較強的致熱作用。這種作用與細菌內毒素明顯不同:IL-1致熱曲線為單向、潛伏期200 min左右,而
內毒素致熱曲線為雙向,潛伏期至少為1H;IL-1對熱敏感、易破壞,而內毒素耐熱;給家兔反覆注射內毒素可出現耐受,但對IL-1不會耐受。②刺激下丘腦釋放促腎上腺皮質素釋放激素,使垂體釋放促腎上腺素,促進腎上腺素釋放糖皮質激素,對IL-1有
反饋調節作用。③作用於
肝細胞使其攝取胺基酸的能力增強,進而合成和分泌大量
急性期蛋白,如α2球蛋白、
纖維蛋白原、C-反應蛋白等。④使骨髓細胞庫的中性粒細胞釋放到血液,並使之活化;增強其殺傷病原微生物的能力和遊走能力。⑤與CSF協同可促進骨髓造血
祖細胞增殖能力,使之形成巨大的集落;還可誘導
骨髓基質細胞產生多種CSF並表達相應受體,從而促使
造血細胞定向分化。
一般性質:1.IL-1的產生細胞IL-1主要由
巨噬細胞產生;此外幾乎所有的有核細胞,如B細胞、NK細胞、體外培養的T細胞、角質細胞、
樹突狀細胞、星形細胞、
成纖維細胞、
中性粒細胞、內皮細胞以及
平滑肌細胞均可產生IL-1。正常情況下只有皮膚、汗液和尿液中含有一定量的IL-1,絕大多數細胞在受到外來抗原或絲裂原刺激後才能合成和分泌IL-1。2.IL-1分子IL-1有兩種不同的分子形式,一種稱IL-1α,由159個胺基酸組成;另一種稱為IL-1β,含153個胺基酸;兩者由不同的基因分別編碼。雖其胺基酸順序僅有26%的同源性,然而IL-1α和IL-1β以同樣的親和力結合於相同的
細胞表面受體,發揮相同的生物學作用。3.IL-1受體(IL-1R)IL-1R幾乎存在於所有有核細胞表面,每個細胞的IL-1R數目不等,少則幾十個(如T細胞),多則數千個(如成纖維細胞)。IL-1R主要有兩種類型:一種為IL-1R1,其分子伸入胞漿內的肽鏈部分較長,起著傳遞活化信號的作用;另一種為IL-1R2,胞內部分的肽段較短,不能有效地傳遞信號,而是將胞外部分的肽鏈釋放到
細胞外液中,以游離形式與IL-1結合,發揮反饋抑制作用。GM-CSF、G-CSF及IL-1自身均可提高細胞IL-1R的表達水平,而TGF及皮質類固醇能降低IL-1R的表達。
IL-2
結構:IL-2分子量為15KD,是含有113個胺基酸殘基的
糖蛋白。
功能:主要由T細胞產生,以自分泌和
旁分泌方式發揮效應。能夠活化T細胞,促進細胞因子產生;刺激
NK細胞增殖,增強NK殺傷活性及產生細胞因子,誘導
LAK細胞產生;促進B細胞增殖和分泌抗體;激活巨噬細胞。
生物學活性:1.刺激T細胞生長。IL-2生物學功能很廣泛,能夠對多種細胞類型如T細胞、B細胞、NK細胞、巨噬細胞和少突神經膠質細胞等產生作用,其中最顯著的作用是影響T淋巴細胞的生長。各種刺激物活化的T細胞一般不能在體外培養中長期存活,加入IL-2則能其長期持續增殖,因此IL-2曾被命名為T
細胞生長因子(T cell growth factor,TCGF)。靜止的T細胞表面不表達IL-2R,對IL-2沒有反應;受
絲裂原或其它刺激活化後T細胞才能表達IL-2R,成為IL-2的靶細胞;而IL-2又可誘導靶細胞增加IL-2R的表達。在活體內,IL-2對CD4+T細胞的作用是通過自分泌途徑實現的,因為活化的CD4+T細胞能夠產生大量的IL-2;而CD8+T細胞則通過
旁分泌途徑來維持細胞的生長。IL-2R在T細胞上的表達是一過性的,一般在活化後2~3天達到高峰,6~10天左右消失。隨著IL-2R的消失,T細胞即失去對IL-2的反應能力。因此若要維持正常T細胞在體外長期生長,必須不斷地用
絲裂原或其它刺激物去刺激T細胞,以維持IL-2R的表達。2.誘導細胞毒作用。①接受了預刺激信號的CD8+T細胞可以受IL-2的作用活化為CTL,發揮細胞毒作用;在一定條件下,CD4+T細胞也可受IL-2的誘導而具有殺傷作用。②NK細胞是唯一正常情況下表達IL-2R的淋巴樣細胞,因此始終對IL-2保持反應性。然而靜止的NK細胞上只表達IL-2R的β鏈和γ鏈,對IL-2的親和力低,只能對高濃度的IL-2發生反應。一旦NK細胞活化,就表達IL-2R的α鏈,成為高親和力的受體;大劑量的IL-2誘導的LAK活性主要NK細胞。③使T細胞作NK細胞產生IFNγ、TNFβ和TGFβ等因子,促進非特異性細胞毒素;還可誘導產生某些B細胞生長因子以及
造血生長因子等,從而發揮相應的生物學作用。3.對B細胞的作用。IL-2對B細胞的生長及分化均有一定的促進作用。活化的或惡變的B細胞表面表達高親和力IL-2R,但是密度較低;較高密度的IL-2可誘導B細胞生長繁殖,促進抗體分泌,並誘使B細胞由分泌IGM向著分泌IGG2轉換。4.對
巨噬細胞作用。人類單核-巨噬細胞表面在正常時興有少量IL-2Rβ鏈的表達,但是受到IL-2、IFNγ或其它活化因子作用後,可表達高親和力IL-2R。單核-巨噬細胞受到IL-2的持續作用後,其
抗原遞呈能力、殺菌力、
細胞毒性均明顯增強,分泌某些細胞因子的能力也得到加強。
產生:IL-2的產生細胞IL-2主要由T細胞(特別是CD4+T細胞)有受抗原或
絲裂原刺激後合成;B細胞、NK細胞及單核-巨噬細胞亦能產生IL-2。
IL-2受體(IL-2R):IL-2的靶細胞包括T細胞、NK細胞、B細胞及單核-巨噬細胞等。這些細胞表面均可表達IL-2R。IL-2R包含3條多肽鏈:1條為α鏈,分子量55KD;1條為β鏈,分子量75KD;另1條為γ鏈,分子量64KD。α鏈的胞內區較短,不能向細胞內傳遞信號,而β鏈和γ鏈的胞內區較長,具有傳遞信號的能力。3種肽鏈單獨與IL-2結合親和力較低,只有同時表達才能產生高度親和力。
IL-3
結構:IL-3分子量約為15KD,其化學本質為糖蛋白。
 白細胞介素3
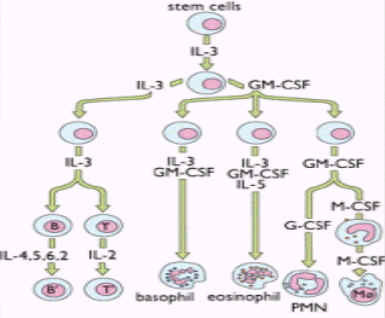
白細胞介素3功能:其主要作用為促進骨髓中
多能造血幹細胞的定向分化與增殖,產生各種類型的血細胞。此外IL-3還可調節多種成熟細胞的生長、分化及相關的基因表達,如C-MYC、IL-2RA基因等。
IL-4
結構:人和小鼠的IL-4CDna均已克隆成功,並獲得了相應的重組產品。成熟IL-4分子量為18~19KD的糖蛋白。
功能:主要由
Th2細胞、肥大細胞及嗜鹼性粒細胞產生(IL-4由
抗原或
絲裂原刺激的CD4+T細胞產生,活化的肥大細胞亦可產生
IL-4。)。能夠促B
細胞增殖、分化;誘導IgG1 和IgE產生;促進
Th0細胞向Th2細胞分化;抑制
Th1細胞活化及分泌細胞因子;協同IL-3刺激肥大細胞增殖等。
IL-4的生物學活性包括以下幾個方面:①促使
抗原或
絲裂原活化的B細胞分裂增殖,但其作用遠弱於IL-2;然而IL-4能促使靜止的B細胞表達MHCⅡ類分子,增強B細胞的
抗原遞呈能力,因此曾稱為B細胞刺激因子。IL-4是Ig重鏈基因類轉換的主要調節因子,能促使B細胞表達和分泌IgE。此外,IL-4還能誘導B細胞表達低親和力fc受體。②象IL-2一樣,IL-4也是CD4+T細胞的自分泌性生長因子;此外,IL-4還能促進tc細胞的活性。③IL-4不能刺激
巨噬細胞增殖,但可增強巨噬細胞的功能;巨噬細胞受刺激後Ⅱ類
抗原和fcγr的表達量均明顯增加;同時巨噬細胞遞呈抗原的能力及對腫瘤細胞的細胞毒素作用也顯著增強。④IL-4與IL-3協同可維持和促進肥大細胞的增殖,在某些起敏反應性疾病發生中具有一定的意義;可與CSF協同作用,促進骨髓造血前體細胞的增殖,誘導髓樣細胞定向分化;誘導內皮細胞表達血管
細胞粘附分子-1(VCAM-1),對淋巴細胞的遷移具有一定意義。
IL-5
結構:與IL-4一樣,IL-5(
白細胞介素-5)也由
抗原活化的CD4+T細胞產生;肥大細胞也能產生IL-5。天然IL-5的分子量為40~50KD,是由二硫鍵連線的二聚體糖蛋白,但是單體IL-5也有IL-5活性。
功能:IL-5曾補稱為T細胞替代因子(T cell replacing factor,TRF),後來發現人類的IL-5對B細胞沒有明顯的刺激作用;其主要功能是刺激
嗜酸性粒細胞增殖、分化及活化。IL-5不僅使嗜酸性粒細胞的數量增加,而且能增強其功能。在
蠕蟲感染和過敏性疾病時出現的嗜酸性粒細胞增多主要是由IL-5引起的。人類IL-5還能促進
嗜鹼性粒細胞釋放組胺和
白三烯等
炎症介質,從而提高嗜鹼性粒細胞的活性。
IL-6
結構:人類IL-6基因位於第7號染色體上;IL-6分子量在21~30KD之間。
功能:主要由
單核巨噬細胞、Th2細胞、血管
內皮細胞、成纖維細胞產生。能夠刺激活化B細胞增殖,分泌抗體;刺激
T細胞增殖及CTL活化;刺激肝細胞合成急性期蛋白,參與
炎症反應;促進血細胞發育。
IL-6可由多種細胞合成,包括活化的T細胞和B細胞、單核-
巨噬細胞、內皮細胞、上皮細胞以及成纖維細胞等。
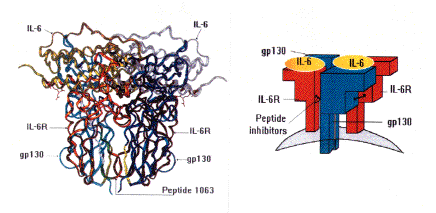 白細胞介素6
白細胞介素6IL-6作用的靶細胞很多,包括巨噬細胞、
肝細胞、靜止的T細胞、活化的B細胞和漿細胞等;其生物效應也十分複雜,曾稱為B細胞刺激因子2(bsf-2)、26KD蛋白、B細胞
分化因子(bCDf)、肝細胞刺激因子(hsf)等。①促進T細胞表面IL-2r的表達,增強IL-1和TNF對TH細胞的致有絲分裂作用。②作為肝細胞刺激因子,在感染或外傷引起的急性炎症反應中誘導
急性期反應中誘導
急性期反應蛋白的合成,其中以澱粉狀蛋白a和c-反應蛋白增加尤為明顯。③促進B細胞增殖、分化並產生抗體;
多發性骨髓瘤的惡變B細胞既能產生IL-6,又能對IL-6發生應答,提示IL-6可能作為這些細胞的自分泌性生長因子。④IL-6還能有效地促進TNF和IL-1誘導的惡病質;促進糖皮質激素合成;刺激破
骨細胞活性和角質細胞生長;還能促進骨髓造血的功能。IL-6不能刺激相應
細胞分泌其它細胞因子,在生理濃度下對免疫細胞的自分泌作用亦比較弱,提示其主要免疫學功能是加強其它細胞因子的效果。
IL-7
結構:IL-7是由骨髓基質細胞分泌的糖蛋白,分子量為25KD;其基因位於第8號染色體。現多採用基因工程手段,從轉染含IL-7CDna表達性質粒的哺乳類細胞培養上清中獲取IL-7。功能:IL-7的靶細胞主要為淋巴細胞,對來自人或小鼠骨髓的B祖細胞、胸腺細胞及外周成熟的T細胞等均有促生長活性。①與
幹細胞生長因子(SCF)協同能夠刺激b前體發生有絲分裂,這一效應可被tgf和所抑制;但對B祖細胞(pro-b)的生長沒有明顯作用。②促進雙陰性胸腺細胞的成熟,提供胚胎胸腺細胞發育過程中tcr基因重組的始動信號;但對成熟T細胞無明顯作用。③誘導胸腺細胞或
外周血淋巴細胞產生LAK細胞活性,其
效應細胞主要為CD8+亞群;但IL-7誘導的LAK細胞不具有NK活性。④IL-7能刺激髓樣前體細胞和
巨核細胞產生
集落形成單位和血小板,使機體從環磷醯胺的
免疫抑制作用中恢復過來;在較高濃度時,IL-7還能增強巨噬細胞的細胞毒活性,誘導
單核細胞分泌細胞因子。

IL-8
結構:主要由單核-巨噬細胞產生;其他如成纖維細胞、
上皮細胞、
內皮細胞、肝細胞等亦可在適宜的刺激條件下產生IL-8。IL-8的分子量約8KD,主要活性形式為72個胺基酸。IL-8的胺基酸順序與許多炎症因子有較高的同源性,屬於同一個家族;現初步證實IL-8家族(亦稱pf4家族)至少有12個成員。IL-8可以分成α和β亞群,α亞群的基因位於第4號染色體上,β亞群的基因位於第17號染色體上。IL-8的受體也有兩型:一種只能與IL-8結合,而另一種還能結合其它的
趨化因子;中性粒細胞和嗜鹼性粒細胞表面均表達豐富的IL-8受體。
功能:主要的生物學活性是吸引和激活中性粒細胞,曾被命名為中性粒細胞激活肽(NAF)、粒細胞趨化肽(GCP)、中性粒細胞激活因子(NAF)等。中性粒細胞與IL-8接觸後發生形態變化,定向遊走到反應部位並釋放一系列活性產物;這些作用可導致機體局部的
炎症反應,達到殺菌和細胞損傷的目的。此外IL-8對嗜酸性粒細胞、嗜鹼性粒細胞和淋巴細胞也有一定作用。
IL-9
結構:IL-9主要是由TH細胞產生,成熟分子含126個胺基酸,包括10個
半胱氨酸;由於糖基化不同,分子量為30~40KD;經過n-聚糖酶處理後,分子量降到15KD。
2-巰基乙醇可使IL-9失活,表明分子間二硫鍵在維持分子生物學活性方面十分重要。
功能:IL-9可在無IL-2和IL-4的情況下維持TH細胞長期生長;IL-9還可促進某些骨髓樣
白血病細胞系(如MOTE)的生長,提示其可能還參與造血過程的調控。IL-9與其它白細胞介素的關係尚不清楚,但與IL-2明顯的不同是不能誘導CTL和LAK等細胞毒活性,但能維持非抗原依賴性TH細胞的長期生長。此外,IL-9還促進肥大細胞的生長及活性。
IL-10
結構:IL-10的分子量為35~40KD,通常為二聚體;主要由TH2細胞產生,也可由
單核細胞、角質細胞及活化的B細胞產生。
 白細胞介素10
白細胞介素10功能:主要Th2細胞和單核巨噬細胞產生。能夠抑制前
炎症細胞因子產生;抑制MHC -II類分子和B-7分子的表達;抑制T細胞合成IL-2、IFN-等細胞因子;可促進B細胞分化增殖。
IL-10能夠抑制活化的T細胞產生細胞因子,因此曾稱為細胞因子合成抑制因子(csif),特別是抑制TH1細胞產生IL-2、IFN-γ和lt等細胞因子,從而抑制細胞免疫應答。IL-10可降低單核-巨噬細胞表面MHCⅡ類分子的表達水平,損害了APC的
抗原遞呈能力,實際上這可能是其抑制
細胞介導免疫的原因。此外,IL-10還能抑制NK細胞活性,干擾NK細胞和巨噬細胞產生細胞因子;但可刺激B細胞分化增殖,促進抗體生成。
IL-11
結構:IL-11由骨髓基質細胞產生,分子量約為23KD,是造血微環境中一個多功能的調節因子。
功能:IL-11可刺激漿細胞增殖及T細胞依賴的B細胞發育;促進巨核細胞的形成及成熟,提高外周血血小板數目;與IL-3和IL-4協同作用刺激休止期
造血幹細胞的增殖;影響紅細胞的生成及分化;調節肝細胞血漿蛋白基因的表達,誘導急性期蛋白生成。
IL-12
結構:IL-12主要由B細胞和
巨噬細胞產生;其分子是一種異型二聚體,40KD(p40)和35KD(p35)的2個亞基通過二硫鍵相連線。
功能:IL-12主要作用於T細胞和NK細胞,曾被命名為細胞毒性淋巴細胞成熟因子(CLMF)和NK細胞刺激因子(NKsf)。IL-12可刺激活化型T細胞增殖,促進TH0細胞細胞向TH1細胞分化;誘導ctl和NK細胞的細胞毒活性並促進其分泌IFN-γ、TNF-α、GM-CSF等細胞因子;促進NK細胞和IL-2rα、TNF受體及CD56分子的表達,增強對腫瘤細胞的adcc效應。
IL-13
結構:IL-13由TH2細胞產生,分子量約10KD。
功能:IL-13可誘導單核細胞分化,增強其MHCⅡ類分子的表達;抑制lps誘導的
單核因子分泌,控制
炎症反應;誘導B細胞增殖及合成IgE類抗體,增強B細胞表面MHCⅡ類分子、CD23及CD72的表達;協同IL-2刺激NK細胞產生IFN,從而促進單核-巨噬細胞活化和TH1型
細胞免疫反應。最近還發現,IL-13還具有抑制HIV-1在
巨噬細胞內複製,誘導中性粒細胞中IL-1RA基因表達和蛋白質合成等多種功能。
IL-14
結構:IL-14由T細胞分泌,其成熟形式含468個胺基酸殘基。
功能:可刺激活化的B細胞增殖,抑制
絲裂原誘導的B細胞分泌免疫球蛋白。
IL-15
功能:IL-15是新近發現的一種因子,可由活化的單核-
巨噬細胞、表皮細胞和
成纖維細胞等多種細胞產生。IL-15的分子結構與IL-2有許多相似之處,因此可以利用IL-2受體的β鏈和γ鏈與靶細胞結合,發揮類似IL-2的生物學活性。屬於IL-2家族成員,通過改變Bcl-1家族成員(如Bcl-2和Bcl-XL)的表達來調節T和NK細胞的激活和增殖。
可誘導B細胞增殖和分化,是唯一能部分取代IL-2誘導初期抗體產生的細胞因子;IL-15能夠刺激T細胞和NK細胞增殖,誘導LAK細胞活性,還能與IL-12協同刺激NK細胞產生IFN-γ。
IL-16
白細胞介素-16是由激活的細胞分泌的一種細胞因子。首先被發現可誘導人和大鼠CD4T淋巴細胞的遊走應答,因此最初被命名為淋巴細胞趨化因子(LCF)。
結構:人白細胞介素-16由第15號染色體上基因15q26.1編碼,其mRNA長2.6kb,半衰期約2h,編碼分子質量67*10^3~80*10^3的前體。
功能:近年來研究發現其存在於許多細胞中,對T細胞、肥大細胞、噬酸粒細胞呼吸道上皮細胞等的生長增殖分化、細胞的功能/細胞間信息傳遞等都具有重要調節作用。
IL-17
功能:IL-17是Th17細胞主要效應因子,由CD4+ T細胞分泌,能夠誘導上皮細胞、內皮細胞、成纖維細胞合成分泌IL-6、IL-8、G-CSF、PGE2,促進ICAM-1的表達。
研究發現IL-17 是T細胞來源細胞因子,該家族包括6個成員的配體(IL-17A~IL-17F)和5個受體(IL-17RA~IL-17RD和SEF)。IL-17是一種主要由活化的T細胞產生的致炎細胞因子,可以促進T細胞的激活和刺激上皮細胞、內皮細胞、成纖維細胞產生多種
細胞因子如IL-6、IL-8、粒細胞-巨噬細胞刺激因子(GM-CSF)和化學增活素及細胞黏附分子1(cellular adhesion molecule 1,CAM-1),從而導致炎症的產生。
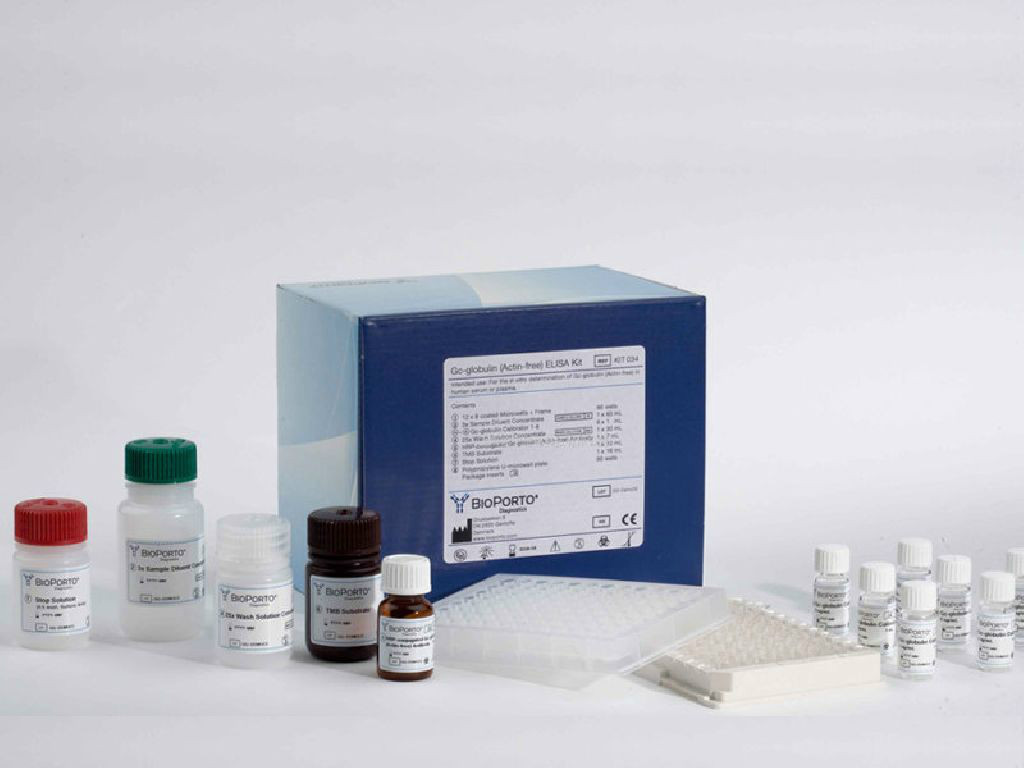
IL-17是T細胞誘導的炎症反應的早期啟動因子,可以通過促進釋放前炎性細胞因子來放大炎症反應。IL-17與受體結合後,可通過MAP 激酶途徑和核轉錄因子kB(nuclearfactor kB,NF-kB)途徑發揮其生物學作用。Th17細胞能夠分泌產生IL-17A、IL-17F、IL-6以及a腫瘤壞死因子(tumor necrosis factora, TNF-a)等,這些細胞因子可以集體動員、募集及活化中性粒細胞。Th17細胞產生的IL-17能有效地介導中性粒細胞動員的興奮過程,從而有效地介導了組織的炎症反應。
IL-18
結構:屬於IL-1配體家族,結構與IL-1蛋白家族相似。人IL-18cDNA編碼193個胺基酸,半胱氨酸天冬酶在N端將其水解為成熟的IL-18,發揮其生物學活性。其位於染色體11q22.2-22.3,由6個外顯子和5個內含子組成,cDNA全長約1.1kb。
功能:是一種作用強大的前炎症細胞因子,最具特徵的功能是調節細胞增生,分化及細胞外基質生成,故IL-18在糖尿病腎病(DN)的發生、發展中起重要作用。
它是一個前炎症因子,可調節多種細胞發育及細胞因子分泌。研究表明,它是獨特的依賴細胞因子周圍環境而刺激Thl和Th2細胞反應的細胞因子。能促進外周單個核細胞產生IFN-γ、IL-2和粒細胞巨噬細胞集落刺激因子 等細胞因子,增強NK細胞和Thl細胞的細胞毒作用,促進T細胞的增殖,並在Thl細胞分化和免疫反應中有促進和調節作用。在免疫調節、抗感染、抗腫瘤及慢性炎症性疾病發病過程中起著重要作用。
IL-19
結構:成熟區153個胺基酸,與IL-10有同源性;染色體1q32。
功能:對抗原呈遞細胞具有調節和促增殖效應。活化Stat3,受體為IL20R1/IL20R2。
IL-20
結構:成熟區164個胺基酸,與IL-10有同源性;染色體1q32
功能:結合IL-20R1/IL-20R2,重組IL-20小鼠腹腔注射可明顯刺激中性粒細胞的移動;參與上皮細胞發育,活化角質細胞Stat3,與牛皮癬有關。
IL-21
結構:成熟區131個胺基酸,與IL-2、IL-4、IL-15空間結構同源,受體包括IL2Rγ鏈; 染色體4q26-q27。
功能:促進骨髓NK細胞的增殖與分化,與抗CD40抗體協同刺激B細胞的增殖,與抗CD3抗體協同刺激T細胞的增殖。
IL-22/IL-TIF
結構:成熟區146個胺基酸,與IL-10有同源性;染色體12q15。
功能:活化多種細胞系的STAT1,3,包括TP-10(腎癌細胞系)和SW480(腸癌細胞系)。促進炎症時的急性期蛋白產生;結合IL22R/IL10R2 OR IL22BP。
IL-23
結構:與IL-12有同源性,異源雙聚體,α鏈為p19,含189個胺基酸,與IL-12 p35 同源性;染色體12q13;其β鏈為IL-12的p40。
功能:經Stat4活化PHA刺激的T細胞,促進其增殖和γ干擾素產生,並誘導記憶性T細胞的增殖。
IL-24/MDA-7
結構:與IL-10有同源性,206個胺基酸;染色體1q32。
功能:結合IL-22R1/IL-20R2 or IL-20R1/IL-20R2,活化Stat3信號轉導途徑,促進腫瘤細胞凋亡。
IL-25(IL-17E)
白細胞介素17E(Interleukin 17E,IL-17E),又稱作IL-25。
1、結構:與IL-17有同源性, 161個胺基酸;染色體14q11.2 。
2、功能:TH2細胞產生,刺激TH2細胞功能,參與速髮型變態反應;支持淋巴樣細胞增殖,刺激FDCP2的增殖。它是由活化的記憶T細胞產生的一種前炎細胞因子,可誘導多種趨化因子和細胞因子的表達,在炎症和造血過程中發揮重要作用。
3、染色體定位:染色體定位分析提示IL-17E位於14q11.2,由2個外顯子和1個內含子組成,與CKLFSF5(趨化素樣因子超家族成員5,Chemokine-like factor superfamily member 5)緊密連鎖,僅相距約500bp。CKLFSF5是我室在國際上首先克隆的趨化素樣因子超家族(Chemokine-like factor superfamily,CKLFSF)成員之一。CKLFSF在人類共有9個成員,已有的功能研究提示,CKLFSF代表一個從趨化因子到四次跨膜蛋白之間的過渡性蛋白家族。IL-17E與CKLFSF5的超近距離連鎖,提示它們之間可能有一定的相關性。
4、表達譜:人IL-17E是通過同源性分析、序列拼接獲得的,到目前為止,尚未用Northern Blot方法在任何組織中檢測到其mRNA的存在。IL-17E確切的生理性細胞來源亦尚屬未知。用GeneAtalas分析IL-17E的表達譜,發現在舌、支氣管上皮細胞和骨髓中,IL-17E表達水平很高;在腎上腺、腦橋、脊髓、胎腦、甲狀腺、腎臟、前列腺、肝臟中有中等程度的表達(見圖1)。
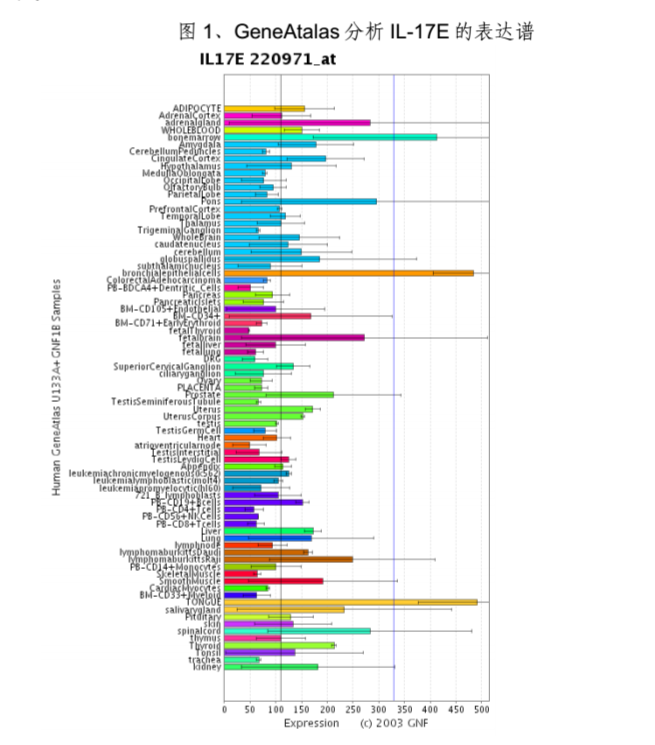 IL-25表達譜
IL-25表達譜套用RT-PCR技術,在腦、腎臟、肺、前列腺、睪丸、脊髓、腎上腺、氣管等多種組織中均可檢測到較低水平IL-17E的轉錄。Ikeda等用RT-PCR和免疫印跡的方法證明,肥大細胞可在IgE作用後產生IL-17E。免疫系統中IL-17E的表達調控仍屬未知。
5、蛋白結構:目前發現IL-17E有兩種cDNA,一種編碼177個胺基酸,另一種編碼161個胺基酸,兩種蛋白產物羧基端的159個胺基酸殘基完全相同,區別僅在於氨基端。信號肽預測和實驗證明,距羧基端145個胺基酸殘基處為切割位點,兩種不同的編碼產物分別切割掉了氨基端的33個和16個胺基酸殘基,生成相同的由145個胺基酸殘基組成的單體。成熟的IL-17E是一種分泌性糖蛋白,為同源二聚體分子,每個單體上有一個N-糖基化位點。
 IL-17家族同源性分析
IL-17家族同源性分析6、受體:IL-17Rh1(IL-17 receptor homolog 1)是IL-17E的受體。IL-17Rh1也是通過同源性分析、序列拼接獲得的,定位於3p21.1,編碼502個胺基酸。IL-17Rh1是I型跨膜分子,是IL-17R家族成員,與IL-17R胺基酸水平的同源性為26%,Northern Blot分析提示其在肝臟和腎臟高表達,在腦、結腸、小腸、骨骼肌亦有表達。IL-17Rh1可結合IL-17E和IL-17B,但與前者的親和力遠遠高於後者。IL-17E與IL-17Rh1結合後,可活化NF-kB,誘導IL-8等前炎細胞因子的表達,但具體的信號傳導通路尚未明確。
7、主要活性:IL-17E的生理功能目前仍不明確,推測其可能與炎症反應的精確調控有關。研究提示,IL-17E可刺激多種來源的細胞系表達IL-6、IL-8等前炎因子和G-CSF(Granulocyte colony stimulating factor,粒細胞集落刺激因子)等造血因子,這一特點與IL-17A十分相似,但目前已知的IL-17E的靶細胞譜比後者窄。
IL-17E轉基因小鼠出現嚴重的多器官慢性炎症,包括肝臟、肺部、心臟、腎臟、淋巴結、脾臟、膀胱。組織器官中有大量中性粒細胞、嗜酸性粒細胞、淋巴細胞、漿細胞和巨噬細胞等多種免疫細胞浸潤。小鼠還出現高中性粒細胞和高嗜酸性粒細胞血症,可能與G-CSF和IL-5升高有關。大部分轉基因小鼠在6周齡時出現黃疸、血清膽紅素和肝酶類升高等肝損表現,有多種細胞因子水平升高,特別是與Th2細胞相關的因子,包括IL-4、IL-5、IL-10、IL-13等,與此一致的是,轉基因小鼠出現血清IgE和IgG1的明顯升高;但與Th2細胞關聯不大的一些細胞因子,如IFN-g(Interferon-g,g-干擾素)、TNF-a(Tumor necrosis factor-a,a-腫瘤壞死因子)、IL-1b等表達水平也有升高。因此,轉基因小鼠體內的炎症反應並不僅由Th2細胞介導。另外,IL-17E可抑制關節軟骨基質的合成,並刺激一氧化氮的釋放和IL-6的產生,提示其可能參與退行性骨關節病的發病。
綜上所述,目前的實驗結果提示,IL-17E具有多效性,主要參與Th2細胞介導的免疫應答,還與某些前炎因子引起的組織特異免疫病理改變有關。IL-17E可引起並調控多種炎症反應,這提示它有可能在慢性炎症和自身免疫性疾病中發揮作用。
IL-26
結構:與IL-10有同源性,全長171個胺基酸;染色體12q15。
功能:T細胞產生,可能參與T細胞抗病毒作用。
IL-27(IL-30)
結構:與IL-12有同源性,異源雙聚體,α鏈為p28,與IL-12 p35同源;其β鏈為EBI3。
來源:IL-27由p28(IL-12的p35相關多肽)和EBI3(EB病毒誘導的基因3)組成異二聚體。其中p28與IL-12的p35亞基同源,EBI3與IL-12的p40亞基同源。人p28和EBI3基因分別定位於16p11和16p13.3。p28必須與EBI3結合,才具有IL-27生物學活性。
功能:由抗原呈遞細胞活化早期階段產生,促進naive T細胞增殖,與IL-12協同刺激T細胞的γ干擾素產生,促進早期Th1細胞。在T細胞增殖分化早期,可以促進CD4T細胞向Thl方向分化,同時IL-27可以協同IL-2促進初始T細胞產生IFN-γ;促進單核細胞產生IL-1、12、18和IFN等炎症細胞因子。它還可以抑制輔助性17T細胞和誘導型調節性T細胞的發育。研究還發現IL-27可以誘導小鼠B細胞產生LgG2a,抑制IL-4誘導的IgG1的合成;但IL-27可以誘導人B細胞產生LgG1.
歸屬:屬於IL-12/IL-6家族成員。主要由抗原呈遞細胞產生,能促進T細胞增殖並向T輔助淋巴細胞(Thl)細胞方向分化,分泌γ干擾素IFN,在抗感染免疫及抗腫瘤免疫等方面發揮作用,參與機體多種疾病的演變過程。
IL-28
結構:與干擾素及IL-10有低水平同源性,IL-28A與IL-28B有96%同源性;染色體定位19q13.13。IL-28A 200aa,IL-28B 198aa。
功能:抗病毒效應。
白細胞介素-28(IL-28A、IL-28B)和白細胞介素29(IL-29)是一組由病毒或雙鏈RNA誘導的多種細胞產生的新型白細胞介素 ,它們能結合一種由IL-10Rβ和IL-28Rα組成的異二聚體型Ⅱ類細胞因子受體,通過Jak STAT信號通路而發揮其抗病毒或其他防禦功能。
人IL-28A、IL-28B和IL-29是由外周血單個核細胞(PMBC)和樹突狀細胞(DC)等產生的細胞因子,它們組成一個新的細胞因子家族。其基因結構與IL-10相近似,但胺基酸水平與干擾素(IFN)更接近,故Kotenko等也將它們相應地稱為IFN-λ1(IL-29)、IFN-λ2(IL-28A)和IFN-λ3(IL-28B)。其基因均位於人19號染色體(19q13.13)。IL-29與IL-28胺基酸的同源性為81%;IL-28A與IL-28B為96%。IL-28A、IL-28B和IL-29與其相應的受體結合而發揮抗病毒感染的作用。
IL-29
結構:與干擾素及IL-10有同源性,200aa;IL-28A與IL-29有81%的同源性;基因定位19q13.13。
功能:抗病毒效應。
IL-31
結構:成熟IL-31分子由141個胺基酸組成,含4個α螺旋結構;基因定位於12q24.31。
功能:Th2細胞表達的細胞因子,活化多種Stat分子,參與變態反應和炎症性疾病。
IL-32
結構:定位於16 p13.3,有4種不同剪下體形式,分別命名為IL-32α,β ,δ,γ。
功能:誘導TNFα和MIP-2的表達; 活化NFκB;誘導p38MAPK的
磷酸化。
 白細胞介素32
白細胞介素32IL-33(IL-1F11)
又稱IL-1F11。
結構:定位於16 p13.3,有4種不同剪下體形式,分別命名為IL-32α,β ,δ,γ 。
功能:結合IL-1受體家族成員ST2,活化NF-κB和MAPK,促進產生Th2細胞因子,參與變態反應。
IL-34
結構:該蛋白由241個胺基酸殘基組成。
功能:IL-34是2008年首次報導的一種新型白細胞介素,目前已知IL-34具有增強單核細胞活力,調節髓樣細胞生長分化,加速破骨細胞形成等功能。
IL-35
結構:IL-35是最新發現的IL-12細胞因子家族成員,由兩個亞基組成的異二聚體,即EBI3和IL-12p35.EBI3由EB病毒感染的B淋巴細胞誘導產生,是編碼為34 kDa的糖蛋白,27%的胺基酸與IL-12p40相同;IL-12p35與其他單鏈細胞因子如IL-6同源.1997年Devergne等發現EBI3和IL-12p35可以聚合為新的造血因子,且在體內形成異二聚體,但未對其功能進行研究.
功能:目前認為Treg細胞及其分泌的細胞因子具有持久的免疫耐受效應,從而推斷IL-35在病毒感染的免疫耐受期發揮重要的作用。
IL-37
結構:除IL-18和IL-33以外,全部人類IL-1家族位於2號染色體的IL-1家族基因簇上。IL-IF7包括12個β鏈,與IL-1家族成員尤其是IL-8擁有共同的結構模型。存在5種剪下變異體(IL-1F7a-e);其中IL-1F7b(NM014439)是最大的,包括6個外顯子中的5個。此外,IL-1FTb可以形成同型二聚體。IL-1F7是目前唯一沒有發現鼠同系物的IL-1家族成員。通過蛋白酶-1剪下處理,重組IL-1F7b前體可以分裂為成熟的IL-1F7b。成熟的IL-1F7b轉運到細胞核中。這個過程需要蛋白酶-1的參與。
功能:對於在2000年的模擬研究中首次被發現的IL-1F7,人們仍然知之甚少。IL-1F7是一種天然的免疫應答抑制物,能夠抑制多種炎症因子的表達,基於其效應的基本本質,研究者認為IL-1家族的這一成員應該被命名為IL-37。研究IL-37有助於加強人們對炎症性疾病的認識,為炎症性疾病的治療提供新靶點。
IL-38
結構:白細胞介素(interleukin, IL)-38是最近發現的IL-1家族細胞因子的第10個成員。IL-38的特異性受體為IL-36R,它是IL-36的部分受體拮抗劑。
功能:IL-38可抑制Th17細胞產生IL-17和IL-22等炎症介質,也可抑制IL-36γ誘導產生IL-8,從而抑制炎症反應。
種內同源分子和種屬間差異
白細胞介素2
不同種屬的IL-2的生物學活性呈現下行性,即沿種系譜向上有約束性,向下無約束性。如人和猿的IL-2幾乎可以作用於所有哺乳動物的T細胞,但其它哺乳動物的IL一般很少可以作用於人。對IL-2的胺基酸序列分析表明這與其受體結合部位胺基酸序列較保守有關,以及與胺基酸排列順序和形成的空間構型也有很大關係。另外一個特點是,IL-2具有很強的種屬特異性,雞IL-2(ChIL-2)與哺乳動物IL-2的同源性僅為20~30%。
由人類由第4號染色體上的一個基因編碼。
白細胞介素3
人類的IL-3基因位於第5號染色體長臂區。
白細胞介素4/5
人IL-4基因與IL-3、IL-5一樣,位於第5號染色體上。
白細胞介素6
人類IL-6基因位於第7號染色體上;IL-6分子量在21~30KD之間,其差異是由於肽鏈的糖基化和磷酸程度不同所致。IL-6由2條糖蛋白鏈組成;1條為α鏈,分子量80KD;另1條為β鏈,分子量130KD。α鏈缺少胞內區,只能以低親合性與IL-6結合,所形成的複合物迅即與高親和性的β鏈結合,通過β鏈向細胞內傳遞信息。
白細胞介素13
其基因位於第5號染色體上,與IL-4基因緊密連線。IL-13分子的胺基酸順序與IL-4有20%~25%的同源性,在功能上也與IL-4有許多相似之處。
白細胞介素16
它與其他具有淋巴細胞趨化活性的蛋白無同源性。
白細胞介素21
Interleukin-21 (IL-21)是近年來發現的一類新細胞因子,與 IL-2 和 IL-15 具有同源性,含有 4 個IL-2 家族特徵的 α 螺旋結構,屬 IL-2 超家族。
白細胞介素34
IL-34和其他人體蛋白都沒有相似性,也沒有明顯的共有結構域和共有基序。它在進化過程中受到較多的約束,在胺基酸水平上,它在不同物種間保守性要高於其受體與其競爭相同受體的配體。
白細胞介素38
IL-38的基因序列與IL-1受體拮抗劑(IL-1Ra)和IL-36Ra的基因有較高的同源性。
白細胞介素-1家族
白細胞介素-1家族(Interleukin-1 family,IL-1F)的細胞因子與急性、慢性炎症有關,在天然免疫應答中發揮重要的作用。IL-1家族由11個成員組成,即IL-1F1~IL-1F11,其中IL-1F5、IL-1F6,IL-1F8、IL-1F9、IL-1F10和IF11是通過分析序列同源性、蛋白質的三維結構、基因位點和受體結合特徵發現並鑑定的細胞因子,2010年上述細胞因子被重新命名為IL-36Ra,IL-36-α,IL-36β,IL-36-γ,IL-38和IL-33。
白細胞介素-17家族
白細胞介素-17家族(Interleukin 17 family,IL-17家族),是與白細胞介素17(Interleukin 17,IL-17)具有較高同源性、在脊椎動物進化中高度保守的一組蛋白質,目前共有六個成員,IL-17A(原IL-17)、B、C、D、E和F。其中,IL-17B、C、D、E、F的編碼基因,是在人類基因組大規模測序過程中,通過同源性分析、EST序列拼接得到的。
IL-17家族成員與已知分子均無明顯同源性。IL-17E與IL-17家族其它成員間的同源性為15-20%。人與小鼠的IL-17E的同源性為80%。IL-17家族的六個成員羧基端的70個胺基酸殘基同源性較高,結構上都有五個較保守和另外兩個相對變化較大的半胱氨酸殘基(見圖3所示),這種結構與半胱氨酸結基序(cystine knot motif)極其相似[8]。胱氨酸結基序是在神經生長因子(nerve growth factor,NGF)、轉化生長因子β(transforming growth factor β,TGF-β)、血小板來源的生長因子BB(platelet-derived growth factor-BB,PDGF-BB)等生長因子中發現的一種由六個胱氨酸殘基形成的結構,在進化中比較保守,具有這種結構的生長因子組成了半胱氨酸結超家族(cystineknotsuperfamily)。
研究意義
1、臨床檢驗上作為免疫系統狀況的指示。
例:全身性感染患者中IL-1ra RN2等位基因和RN2/2基因型的分布頻率與正常對照相比明顯增加(0.34 vs 0.23, P<0.01;0.12 vs 0.05, P<0.05).IL-1α VNTR及IL-1β AvaI基因多態性(等位基因頻率及基因型分布)在兩組間均無顯著差異.另外,全身性感染患者中基因型A2/2,B2/2和RN2/2病死率明顯增加(分別為80%,81%和71%).如果患者同時具有A2,B2和RN2三種等位基因中的兩種,則全身性感染更為嚴重(APACHE II和MODS評分更高),病死率為55%~65%.相反,基因型為A1/1,B1/1或RN1/1的全身性感染患者病死率較低(0~13%).結論與IL-1A或IL-1B基因多態性不同,等位基因IL-1RN2的基因多態性對全身性感染具有易感性.等位基因A2,B2和RN2可能是全身性感染的高危基因標記物。
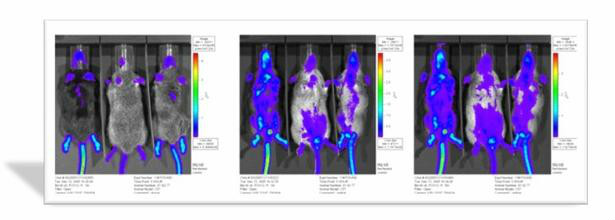 白細胞介素1β光素酶基因表達的轉基因小鼠
白細胞介素1β光素酶基因表達的轉基因小鼠2、作為細胞信號調節免疫系統功能,治療免疫疾病或抗腫瘤。
3、加深對人體生理功能的了解,加深對病情發生、發展的認識。
4、對生命過程的起源進行更深入的認識。
白細胞介素1
IL-1雖未廣泛用於人體研究,但其對免疫系統的特殊作用使它在臨床套用方面具有誘人的前景。另外,由於IL-1也參與機體的多種
病理過程,所以研究IL-1抑制物可能也具有實際意義。現已克隆出IL-1受體拮抗劑(IL-1 receptor antagonist,IL-1RA),該物質可在體內外封閉IL-1的活性,是一種較理想的IL-1封閉因子。
白細胞介素12
由於IL-12在抗
腫瘤免疫及
抗感染免疫中的重要作用,人們對其臨床套用寄予厚望;特別是IL-12可協同IL-2促進ctl和LAK細胞的產生表明,IL-12與IL-2聯用可望構成一種更有效的腫瘤免疫治療方法。
套用
白細胞介素2
由於IL-2能誘導和增強細胞毒活性,目前套用IL-2治療某些疾病、特別是對腫瘤治療的研究得到了廣泛開展,單獨使用IL-2或與LAK細胞等(詳見第四章)聯合使用治療腫瘤取得了一定的療效;還可望用於病毒感染、
免疫缺陷病及自身免疫病的治療。
但IL-2的副作用也日益引起人們的注意:IL-2可引起發熱、嘔吐等一般症狀,還可導致水鹽代謝紊亂和腎、肝、心、肺等功能異常;最常見、最嚴重的是
毛細血管滲漏綜合徵,使患者不得不中止治療。IL-2的副作用常與IL-2的劑量及用藥時間呈相關,停止用藥後症狀多迅速減輕或消失。IL-2引起副作用的機制是多方面的,但主要是間接性的,即IL-2誘導產生的某些因子或殺傷性細胞起著重要作用;現已知LAK細胞可通過溶解血管內組織而導致多種副作用。給予適當藥物(如吲哚美辛、哌替啶、對乙醯基氨酚等)、採取聯合用藥、改進給藥方式(如少量多次短時間輸注)和給藥途徑(如改全身用藥為腫瘤局部用藥)等將有效地減輕不良反應。
白細胞介素3
可以用來治療小兒骨髓增生異常綜合徵、白血病。
由於IL-3對早期階段造血細胞的作用較廣,可望用於放療或化療後患者的骨髓重鍵。
 信號傳遞
信號傳遞 白細胞介素1(IL-1)結合併激活其受體
白細胞介素1(IL-1)結合併激活其受體

 白細胞介素3
白細胞介素3
 白細胞介素6
白細胞介素6
 白細胞介素10
白細胞介素10

 IL-25表達譜
IL-25表達譜 IL-17家族同源性分析
IL-17家族同源性分析 白細胞介素32
白細胞介素32
 白細胞介素1β光素酶基因表達的轉基因小鼠
白細胞介素1β光素酶基因表達的轉基因小鼠