宮頸癌簡介
宮頸癌是女性最常見的惡性腫瘤,其死亡率僅次於乳腺癌。近年來,宮頸癌的發展趨勢逐漸偏向年輕化且呈逐年上升現象。宮頸癌雖然是惡性腫瘤,但其歷程漫長,從癌前病變發展到惡性的浸潤性宮頸癌需要5-10年的時間。人乳頭瘤病毒( HPV) 感染是宮頸癌的主要致病元兇,研究表明99.7% 的宮頸癌患者存在HPV感染。HPV感染與宮頸癌有高度相關性, HPV陰性者幾乎不會發生宮頸癌。因此,宮頸癌篩查至關重要。宮頸癌篩查項目中,臨床上以HPV檢測和TCT檢查較為常見。
基因組介紹
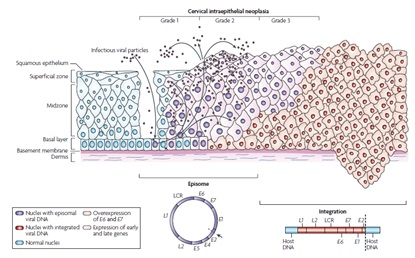
HPV是一種雙鏈的小DNA病毒,具有7900個鹼基對,由病毒蛋白外殼和核心DNA物質構成,無包膜。病毒基因組分為3個部分:早期基因區(E)、晚期基因區(L)及將早期區與晚期區分開的長調控區(LCR)。調控區主要調控病毒的轉錄,控制病毒蛋白和感染顆粒的產生。早期區編碼E6、E7、E1、E2、E4和E5蛋白質,主要參與病毒DNA的複製、轉錄。晚期區編碼L1、L2蛋白質,分別是病毒的主要和次要衣殼蛋白。
致癌機理
E6/E7是致癌基因,編碼病毒癌蛋白,在細胞轉化和維持轉化組織惡性表型的過程中起著至關重要的作用。宮頸病變直至浸潤癌的發展過程與HPV基因組整合至宿主細胞基因組密切相關,伴隨著E2基因的丟失和隨後E6/E7致癌基因的過度表達。E6/E7基因編碼的致癌蛋白是導致宮頸上皮癌變的重要因子,這兩種蛋白與細胞內兩種主要抑癌蛋白p53和pRb的結合以及調控可以明顯改變細胞生長周期和DNA修復,由此導致基因組的不穩定性是細胞轉化和永生化的必要條件,見右圖。
HPV導致宮頸病變的過程圖示:
在CIN I期,HPV主要以游離狀態存在於宿主細胞中,在病變進一步發展的過程中,HPV基因組會整合到宿主細胞基因組,隨著病變程度的增加,HPV最終以整合狀態存在。
檢測靶點
從低級別病變發展為癌的過程中,HPV基因組會發生整合。在整合過程中,E6/E7基因持續存在,L1基因可能會丟失。但由於L1基因相對保守,更適合於以通用引物為靶點的檢測,由於受限於現有的技術平台,幾乎所有的HPV檢測產品均以L1為檢測靶點。在宮頸高級別病變中,由於基因組的整合會使L1基因有丟失的可能,因此,以L1基因作檢測靶點會對HPV有漏檢的可能。相反,如果檢測靶點設計在E6/E7基因,不管HPV基因組是否發生整合,都可以檢測出HPV陽性的病人。
對56個浸潤性宮頸癌組織活檢樣本分別用L1區通用引物和E6/E7分型引物進行檢測比較發現,有23個樣本存在L1區缺失。研究發現,HPV 18的L1/E1區更容易丟失。幾乎所有的HPV18陽性的宮頸癌中病毒基因組整合到人基因組上;而HPV16陽性的宮頸癌中也有≤60%的病毒基因組發生整合。一項基於15,774例病人樣本的研究發現,跟型別特異性E6/E7引物PCR比較,通用引物MY09/11 PCR檢測會造成10.9%(522例)的漏檢;409例由MY09/11 PCR檢測結果為陰性的病人中,隨訪發現最終有104人(25.4%)發展為CIN2+。
綜上所述,雖然以L1基因為檢測靶點在技術上相對容易實現,但由於HPV基因組會整合到人基因組上,並可能由此造成L1基因的丟失,所以L1基因作為檢測靶點有漏檢的風險;以致癌基因E6/E7作為檢測靶點,不論基因組是否發生整合,都不會有漏檢的可能性。因此,HPV DNA檢測應該以致癌基因E6/E7作檢測靶點。