基本介紹
- 中文名:Ca泵
- 外文名:calcium pump
- 別稱:鈣離子泵
- 作用:催化質膜內側的ATP水解
- 套用領域:生物研究領域
簡介,結構與功能,結構,功能,轉移鈣離子,鈣泵循環,收縮和舒張,超載現象,
簡介
鈣離子泵(Ca泵或Ca2+泵)
Ca2+-Mg2+-ATP酶(即鈣泵)是存在於組織細胞及細胞器的膜上的一種蛋白酶,由於其離子運轉是藉助類似泵的機制來完成的,醫學上將離子的這種運轉方式稱為"泵"。通過對"鈣泵"的醫務研究,有些學者認為,人體疾病和衰老的過程就是由於各種原因所致機
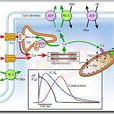
體"鈣泵"失調,引起細胞內鈣離子含量增加、細胞內、外鈣離子濃度差下降而形成的。有人將這種人體內鈣跨膜分布梯度降低的過程稱之為"機體緩慢死亡"過程。由此可見,鈣離子的正常分布也與人體生活活動有著非常密切的聯繫。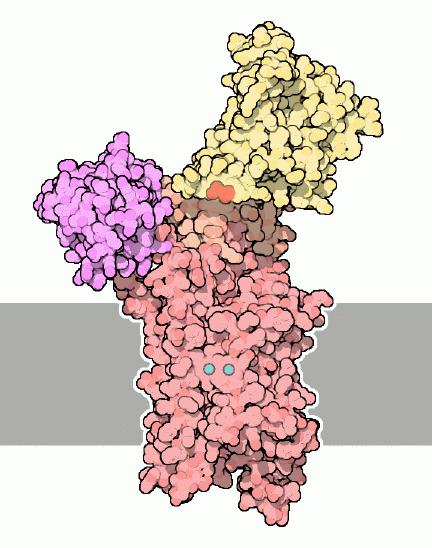 Ca泵示意圖
Ca泵示意圖
 Ca泵示意圖
Ca泵示意圖性質:調節鈣在生物膜中的激活轉移的結構或機制。它是由Ca2+-三磷酸腺苷酶(Ca2+-ATPase)在膜上組裝而成。在紅細胞質膜上的鈣泵把胞質游離Ca2+輸送到胞外;在肌紅細胞,肌質網上的鈣泵把Ca2+從肌漿運輸到肌質網內。
結構與功能
Ca2+泵分布在動,植物細胞質膜,線粒體內膜,內質網樣囊膜(SER-like organelle),動物肌肉細胞肌質網膜,植物葉綠體膜上上,是由1000個胺基酸的多肽鏈形成的跨膜蛋白,它是Ca2+激活的ATP酶,每水解一個ATP轉運兩個Ca2+到細胞外,形成鈣離子梯度.通常細胞質游離Ca2+濃度很低,約10-7~10-8摩爾/升,細胞間液Ca2+濃度較高,約5×10-3摩爾/升.胞外的Ca2+即使很少量湧入胞內都會引起胞質游離Ca2+濃度顯著變化,導致一系列生理反應.鈣流能迅速地將細胞外信號傳入細胞內,因此Ca2+是一種十分重要的信號物質.線粒體內腔,肌質網,內質網樣囊腔中含高濃度的Ca2+,濃度大於10-5摩爾/升,名為"鈣庫".在一定的信號作用下Ca2+從鈣庫釋放到細胞質,調節細胞運動,肌肉收縮,生長,分化等諸多生理功能.
結構
Ca離子的結合域是由4個α-螺旋組成的跨膜區(蛋白質編號leul).圖中所展示的就是一個通道螺旋(蛋白質編號1eul)。兩個藍綠色的球表示鈣離子,它們被負責收集的胺基酸所固定。這些胺基酸即是圖中的球和棍。這兩個鈣離子可以協調這些蛋白亞基在各個方向上的平衡。若Ca離子位置發生改變,則該蛋白的穩定性大大降低.可參看無Ca離子狀態時的鈣泵結構(蛋白質編號liwo)。例如:當加入一種可結合於Ca離子結合位點鄰近區域從而使鈣蛋白處於一個穩定但失活狀態的藥物分子時,鈣泵就會很快被溶解。
功能
(1)紅血球的細胞內外Ca2+的濃度梯度很大,可以認為這是由存在於膜上的Ca2+依賴性ATP酶所引起的Ca2+的主動排出;
(2)肌漿網是靠膜上的Mg2+、 Ca2+ATP酶來進行Ca2+的主動運輸的;
(3)線粒體膜依靠電子傳遞能,以1∶1之比攝取Ca2+和磷酸;
(4)小腸黏膜上皮細胞從食物中攝取Ca2+,此時維生素D是必需因子。所有這些都可稱作鈣泵,但狹義的是指(1)和(2),而(4)是橫貫細胞的運輸,其餘的都是膜內外之間的運輸。
轉移鈣離子
鈣泵是一個很奇怪的"機器",是由好幾個可運動部分組成。如圖所示(蛋白質編號1eul)它有很大一部分伸出內質網,還有一部分在內質網膜內起固定作用,整個形狀像一個貫穿膜的通道。每水解一個ATP,它可轉運兩個鈣離子(如圖藍色部分所示)進入肌質網,同時,轉運兩到三個氫離子離開肌質網。當泵出鈣離子時,鈣泵發生彎曲和收縮。
鈣泵循環
在鈣離子轉移的過程中,鈣泵發生一系列的構象變化。一般認為經歷四個步驟,較常見的鈣泵構象有兩種:左圖的結構(蛋白質編號liwo)為開放狀態,推測在其轉移位點有氫離子存在,儘管在其晶體結果中並未發現氫離子,但當處於開放型的結構變為上面右圖所示的結構時(蛋白質編號leul),允許鈣離子從胞外進入腔內,並將氫離子泵到胞質中。下面的兩步通過一個ATP分子改變鈣泵的構象以利於鈣離子的釋放。在該過程中,位於胺基酸序列351位的天冬氨酸磷酸化(用紅色表示),從上圖可以看出,該天冬氨酸與推測的ATP結合位點(接近天冬氨酸)位於距鈣離子較遠的位置。上述過程的調控是通過ATP結合域的變化使通道蛋白適當的呈開放或關閉狀態,進而控制鈣離子的流動。
收縮和舒張
只要我們稍微一動,就需要數以億萬計的肌球蛋白發動機(一種蛋白質分子)的工作。我們的肌肉細胞是通過鈣離子來協調如此大量的分子工作的。當肌細胞收到與它相連的神經傳遞的信號後,它就從肌質網(即肌肉細胞中的內質網,被大量肌動蛋白纖維和肌球蛋白纖維包圍)中釋放大量的鈣離子。這些鈣離子迅速地擴散並且粘附到運動纖維上的原肌球蛋白上,導致肌球蛋白結構發生改變並且使肌纖維(肌球蛋白發動機)發生相對滑動。這數以億萬計的肌球蛋白發動機的持續滑動,使肌肉持續收縮,直到鈣離子離開肌球蛋白。
神經—肌接頭的傳遞過程
神經—肌接頭的興奮傳遞是通過神經遞質和電變化兩個過程來完成的。即當衝動傳至軸突末梢時,接頭前膜因去極化而引起膜上的鈣通道開放,細胞間液中的一部分鈣的二價正離子移入膜內。促使囊泡與前膜接觸、融合,然後釋放出Ach。Ach擴散到終極膜,並與該處的受體結合,形成Ach—受體複合物.它使終板膜同時對所有小離子(包括鈉離子、鉀離子、氯離子等,但以鈉離子為主)的通透性都增加,鈉離子透入快而多,鉀離子透出慢而少,於是終板膜產生局部去極化,這一電變化稱為終板電位。當終板電位達到一定閾值時,可使終板膜鄰近的肌膜產生可擴布的鋒電位,沿著肌膜傳布,通過興奮—收縮耦聯導致肌肉收縮。Ca2+與肌鈣蛋白結從而出現肌肉收縮。
另外,終板膜上的膽鹼酯酶能使Ach迅速水解破壞。因此,運動神經末梢發生一次動作電位,只能引起一次肌細胞興奮,產生一次收縮。某些藥物如新斯的明、毒扁豆鹼等,可與膽鹼酯酶結合,使其失去活性,不能水解Ach,或水解得很慢。以致動作電位持續時間延長,常引起肌肉痙攣。另一些藥物如箭毒等,能與Ach競爭終板膜上受體,阻斷Ach的作用,從而影響神經—肌接頭的興奮傳遞,使肌肉鬆弛。外科手術時,可套用箭毒類藥物作為肌肉鬆弛劑。
神經—骨骼肌的興奮耦聯、傳遞
當神經衝動傳到肌細胞時,衝動引起軸突末梢去極化,電壓門控式鈣離子通道開放,鈣離子內流引起囊泡移動以至排放,將其內的乙醯膽鹼釋放入神經—肌肉接頭間隙內,乙醯膽鹼與存在於肌細胞膜上的乙醯膽鹼受體結合,引起終板膜上的特殊通道蛋白質開放,鈉離子的內流和鉀離子的外流使肌細胞產生動作電位,並將其迅速擴布到整個細胞膜,於是整個肌細胞便進入興奮狀態。肌細胞的興奮並不等於細胞收縮,這中間還需要一個過程。這個把肌細胞的電興奮與肌細胞機械收縮銜接起來的中介過程,稱為興奮收縮耦聯。具體的耦聯過程是:首先,細胞質膜的動作電位可直接傳遍與其相延續的橫管系統的細胞膜。橫管的動作電位可在三聯管結構處把興奮信息傳遞給縱管終池,使縱管膜對鈣離子的通透性增大,貯存於池內的Ca2+便會順其梯度擴散到胞漿中,使胞漿Ca2+濃度升高,Ca2+與肌鈣蛋白結合,從而出現肌肉收縮。
當神經衝動停止時,肌膜及橫管電位恢復,終池膜對Ca2+的通透性降低,由於Ca2+泵的作用,Ca2+回到終池,使肌漿內Ca2+降低,Ca2+與肌鈣蛋白分離,從而出現肌肉舒張。
舒張肌肉
在一段緊張的鈣誘導收縮後,鈣泵可以使肌肉舒張。鈣泵是在肌質網膜中發現的,在有些肌質網中,它的含量非常多,約占蛋白質總數的90%。通過ATP提供能量,鈣泵可將鈣離子泵回肌質網中,從而降低肌動蛋白和肌球蛋白周圍的鈣離子濃度,使肌肉得以舒張。鈣離子也被當作信號分子存在於其它細胞中,並且,類似的"泵"也在其他大部分細胞膜中發現。鈣泵不停地工作,從而使細胞質內的鈣離子濃度降到一個很低的水平。這樣,一旦再有信號傳入,細胞又可將大量的鈣離子釋放到細胞質中,引起肌肉收縮。
超載現象
各種原因引起的細胞內鈣濃度明顯增多並導致細胞結構損傷和功能代謝障礙的現象稱為鈣超載( calcium overload )。 細胞內鈣超載的發生機制:
1 . Na+ /Ca2+ 交換異常 生理條件下, Na+/Ca2+ 交換蛋白轉運方向是將細胞內 Ca2+ 運出細胞,與細胞膜鈣泵共同維持心肌細胞靜息狀態的低鈣濃度。 Na+ /Ca2+ 交換蛋白以 3 個 Na+ 交換 1 個 Ca2+ 的比例對細胞內外 Na+ 、 Ca2+ 進行雙相轉運。 Na+ /Ca2+ 交換蛋白的活性主要受跨膜 Na+ 濃度的調節,此外還受 Ca2+ 、 ATP 、 Mg2+ 、H+ 濃度的影響。已有大量的資料證實, Na+/Ca2+ 交換蛋白是缺血- 再灌注損傷和鈣超載時鈣離子進入細胞的主要途徑。
(1) 細胞內高 Na+ 對 Na+ /Ca2+ 交換蛋白的直接激活作用:缺血使細胞內 ATP 含量減少,鈉泵活性降低,造成細胞內鈉含量增高。再灌注時缺血的細胞重新獲得氧及營養物質供應,細胞內高 Na+ 除激活鈉鉀泵外,還迅速激活 Na+ /Ca2+ 交換蛋白,以加速 Na+ 向細胞外轉運,同時將大量 Ca2+ 轉入細胞內,造成細胞內 Ca2+ 超載。
(2) 細胞內高 H+ 對 Na+ /Ca2+ 交換蛋白的間接激活作用:質膜 Na+ /H+ 交換蛋白主要受細胞內 H+ 濃度的變化,以 1:1 的比例將細胞內的 H+ 排出胞外,而將 Na+ 攝入細胞,這是維持細胞內 PH 穩定的重要機制。缺血缺氧期,由於細胞的無氧代謝增強使 H+ 生成增加,組織間液和細胞內液 PH 明顯降低。再灌注使組織間液 H+ 濃度迅速下降,而細胞內 H+ 濃度很高,形成跨膜 H+ 濃度梯度。細胞膜兩側 H+ 濃度差可激活心肌 Na+ /H+ 交換蛋白,促進細胞內 H+ 排出,而使細胞外 Na+ 內流。如果內流的 Na+ 不能被鈉泵充分排出,細胞內高 Na+ 可繼發性激活 Na+ /Ca2+ 交換蛋白,促進 Ca2+ 內流,加重細胞鈣超載。
(3) 蛋白激酶 C ( PKC )活化對 Na+/Ca2+ 交換蛋白的間接激活作用:生理條件下,心功能主要受 β 腎上腺素能受體調節, α1 腎上腺素能受體的調節作用較小。但缺血 - 再灌注損傷時,內源性兒茶酚胺釋放增加, α 1 腎上腺素能受體的調節相對起重要作用。 α1 腎上腺素能受體激活 G 蛋白 - 磷脂酶 C ( PLC )介導的細胞信號轉導通路,促進磷脂醯肌醇分解,生成三磷酸肌醇( IP3 )和甘油二脂( DG ),促進細胞內 Ca2+ 的釋放; DG 經激活 PKC 促進 Na+ /H+ 交換,進而促進 Na+/Ca2+ 交換,使胞漿 Ca2+ 濃度增加。