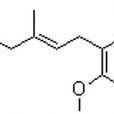
基本信息
中文名稱 霉酚酸
中文別名 麥可酚酸
英文名稱 mycophenolic acid from penicillium brevi-compactum
英文別名 mycophenolic acid from penicillium*brevi-compactu; Mycophenolic acid
分子式 C17H20O6
編號系統
CAS號:24280-93-1
MDL號:MFCD00036814
EINECS號:246-119-3
BRN號:1295848
PubChem號:24896987
物性數據
性狀:粉末
熔點(ºC):141
閃點(ºC):88
溶解性:溶於甲醇,乙醇;微溶於醚,氯仿;難溶於苯,甲苯;幾乎不溶於冷水。
分子結構數據
1、摩爾折射率:83.11
2、摩爾體積(m3/mol):248.1
3、等張比容(90.2K):674.8
4、表面張力(dyne/cm):54.6
5、極化率(10-24cm3):32.94
計算化學數據
1.疏水參數計算參考值(XlogP):3.2
2.氫鍵供體數量:2
3.氫鍵受體數量:6
4.可旋轉化學鍵數量:6
5.互變異構體數量:4
6.拓撲分子極性表面積93.1
7.重原子數量:23
8.表面電荷:0
9.複雜度:486
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:1
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
常溫常壓下穩定
貯存方法
2-8℃
藥理作用
霉酚酸酯作為主要的
免疫抑制劑已被國內外廣泛套用於預防、治療移植器官急性排異反應。霉酚酸酯在體內通過轉化為霉酚酸而發揮免疫抑制活性。在不同的移植群體中,均可發現個體之間霉酚酸
藥代動力學的巨大差異,並且體內、外因素會影響其藥代動力學。
關鍵字:霉酚酸酯,霉酚酸,藥代動力學,器官移植
霉酚酸酯(MMF)是霉酚酸(MPA)的2-嗎啉代乙基酯類衍生物。MPA能夠非競爭性地結合次黃嘌呤單核苷酸脫氫酶(IMPDH),後者是T、B
淋巴細胞增殖過程中鳥嘌呤核苷酸從頭合成的關鍵酶。在目前的國內外器官移植中,MMF已得到廣泛套用。
用途:來源於Penicillium stoloniferum及類似菌株的一類抗生素/抗菌藥。能在體內通過抑制次黃〔嘌呤核〕苷酸脫氫酶的作用阻斷嘌呤核苷酸的合成。阻止T細胞,淋巴細胞的分裂及B細胞中抗體的形成從而作為一種免疫抑制因子。在分子生物學中用於篩選含大腸桿菌黃嘌呤鳥嘌呤磷酸核糖轉移酶基因的細胞。
藥代動力學
吸收
Bullingham等認為,無論口服或
靜脈給藥,MMF均能快速且廣泛地被機體吸收,並在循環前完全代謝為其活性產物MPA。兩種給藥途徑的MPA藥時曲線基本相似。平均MPA達峰時間(tmax)約為1h。平均MPA半衰期(t1/2)約為17h,提示每日兩次用藥較為適當。兩種給藥途徑的MPA濃度-時間曲線下面積(AUC∞)無顯著性差異,約為105mg.h/L。
代謝
MPA經尿苷二磷酸葡萄糖苷酸轉移酶(UGT)代謝為無活性的霉酚酸葡萄糖苷酸(MPAG)。肝臟是UGT最活躍的臟器,也是MPA代謝的主要場所。
Bullingham等發現用藥後1h內,MPAG的血漿濃度低於同一時刻的MPA濃度,但隨後卻高出數倍。平均MPAGt1/2與MPA相近,而總MPAGAUC高出MPA四至五倍,相應地其平均血漿清除率比MPA低四至五倍。比較MPAG和MPA圖形的早期階段,兩者形狀相似,只是前者較後者延遲並且增寬。
90年代末,Shipkova等在移植受者血液內分離出MPA的其它兩種代謝產物:霉酚酸醯基葡萄糖苷酸(AcMPAG)和霉酚酸苯基葡萄糖苷酸(MPAG1s)。MPAG1s對IMPDH無抑制作用,不參與免疫反應;而在體外實驗中,AcMPAG被發現可以抑制重組人II型IMPDH(rh-IMPDH-II),並可抑制淋巴細胞增殖(3,4)。另一方面,AcMPAG能夠與血漿蛋白以及其它大分子共價結合,這被認為是它們免疫與毒性的機制。
腸肝循環
多藥耐藥相關蛋白2(MRP2)在肝細胞表面表達,其功能是將內源性結合物以及藥物代謝產物排泄入膽汁。Kobayashi等證實MPAG的膽汁排泄必須依賴MRP2才能完成。游離MPA(fMPA)也是MRP2的作用底物,但似乎MRP2優先選擇MPAG而不是MPA。
當膽汁進入小腸,MPAG在微生物的作用下被降解為MPA並被重新吸收進入體循環,此過程即為MPA的腸肝循環(EHC),在藥時曲線上表現用藥後6-12h出現的第二峰(峰值較第一次小)。目前已證實,EHC可使MPA-AUC平均增加37%。
研究表明,MPAEHC效應顯著影響MMF的體內代謝過程,機體內影響膽汁分泌和膽汁排泄的因素,如結腸炎、腹瀉和抗生素等可改變腸道吸收功能和/或腸道菌叢的數量,均可能使MMF的體內代謝過程發生顯著變化。
清除
MPAG通過腎小管分泌排泄入尿液。口服放射線標記的MMF可完全尋回給藥的劑量,其中93%出現在尿液中,6%於糞便中,大部分以MPAG的型式由尿液排出,極微量以MPA的型式由尿液排出。
Shaw等認為三種因素調節MPA清除率:(1)肝臟、胃腸道的UGT;(2)MPA-EHC;(3)MPA游離度。可以引起MPA清除率發生巨大改變或與之有關的因素包括:急性或慢性腎功能不全、伴隨免疫抑制劑如CsA和皮質類固醇、移植後時間。另一個可能的因素為種族差異。
游離MPA
MPA與白蛋白的結合率約為97%,穩定的移植患者fMPA占總MPA的1-3%,對IMPDH的抑制以及對於絲裂原刺激的淋巴細胞增殖的抑制均依賴於fMPA濃度,與白蛋白結合的特性以及患者自身因素會顯著改變fMPA和fMPA-AUC。Shaw等認為測定游離MPA濃度以及總MPA濃度有助於衡量MPA的暴露度,以下因素可顯著降低MPA與白蛋白的結合率:(1)腎移植術後早期腎功能差的患者;(2)慢性腎功能衰竭的患者;(3)肝移植術後早期的患者;(4)低白蛋白和/或高膽紅素的患者。
在一項小兒腎移植的研究中發現,fMPA-AUC是引起MMF相關副作用的重要因素,大於0.4mg.h/L時白細胞減少症或感染的風險增加。
知識介紹
影響β-內醯胺類抗菌作用素:
革蘭陽性菌與陰性菌的結構差異甚大,β-內醯胺類各藥與母核相聯接的側鏈不同可影響其親脂性或親水性。有效藥物必需能進入菌體作用於細胞膜上的靶位PBPs。影響抗菌作用的主要因素
① 藥物透過革蘭陽性菌細胞壁或陰性菌脂蛋白外膜(即第一道穿透屏障)的難易
② 對β-內醯胺酶(第二道酶水解屏障)的穩定性;
③ 對抗菌作用靶位PBPs的親和性。根據這些因素。
風險術語
R22 Harmful if swallowed。吞食有害。