簡介
醯鹵、酸酐、酯等被醇分解,生成酯和其他化合物的反應,稱為醇解反應。酯的醇解反應又稱為酯交換反應(見酯交換)。酯交換反應需要酸或鹼作催化劑。腈也能發生醇解反應。其反應如下:
 醇解反應
醇解反應醯鹵與醇(或酚)很快反應生成酯,利用這個反應可以製備某些醇或酚不能與羧酸直接生成的醇酯或酚酯。
反應機理
異丙醇鋁與醇發生作用會改變其原有的性質,它們的作用有兩種情況:
(1)溶解在異丙醇中。這種溶解作用,會使醇鹽配位數擴大,醇分子配位體取代其原有的配位體醇鹽分子,締合分子解體,締合度下降。
(2)溶解在與其自身有不同烷基的醇中。這種作用稱為醇解反應或醇交換反應。
AH(OR)3 + mRˊOH —→AI(OR)3-m (ORˊ)m +mROH
這類反應機理為雙分子親核取代反應(SN2):
 雙分子親核取代反應
雙分子親核取代反應這類反應受位阻因素的影響,反應速度依MeO> EtO> PrˊO> BuˊO順序下降,還受中心金屬原子的化學性質影響。
醇解反應公式
RnSnX4-n +(4-n)RˊOH —→RnSn(ORˊ)4-n +(4-n)HX
RnSnX4-n +(4-n)RˊSH —→RnSn(SRˊ)4-n +(4-n)HX
(C6H5)2SnCl2 +2C6H5CH2OH—→(C6H5)2Sn(OCH2C6H5)2 +HCl
(C2H5)3SnCl +NaOC2H5—→(C2H5)3SnOC2H5 +NaCl
(C4H9)3SnCl +C2H5SH—→(C4H9)3SnSC2H5 +HCl
NC5H4Sn(CH3)3 +n—C4H9OH—→ C5H5N +(CH3)3SNOC4H9-n
套用實例
醇解(alcoholysis)是苷或糖在酸的催化下與醇作用發生分子中苷鍵全部斷裂或部分斷裂的反應。通常是對全甲醚化的苷或糖進行甲醇解,以確定糖與苷元、糖基與糖基之間連線的位置。全甲醚化的苷或糖發生甲醇解後,原位於最末端的糖基轉變為全甲基化的單糖,其他糖基中原苷鍵所在—OH會以游離狀態存在,以此可以推斷苷鍵所在的位置。另外,甲醇解後所得不同類型單糖數目可推測多糖重複結構中這種鍵型單糖的數目。
苷或糖的甲醇解方法是將全甲醚化的苷或糖溶於無水甲醇與乾的HCl形成的1%~6%HCI/MeOH液中,糖的濃度為1%~2%,加熱回流到旋光度恆定。難甲醇解的可用封管加熱。冷後反應液用Ag2CO3中和或陰離子交換樹脂去酸,濃縮至糖漿備用。若需進一步用氣相色譜法定量分析,則濃縮時應避免甲基糖的揮發而損失。
有時也用酸催化的硫醇解,它與甲醇解相似。硫醇解可使酸中易破壞的糖,由於還原性端基生成硫代縮醛(酮)而得以保護。水解糖的硫代縮醛(酮)衍生物易結晶,也易純化。瓊脂多糖由此得瓊脂雙糖的硫代縮醛;角叉菜膠由此得角叉菜雙糖的硫代縮醛。前者是3,6-脫水-4-O-(β-D-吡喃半乳糖)-L-半乳糖,後者是3,6-脫水-4-O-(β-D-吡喃半乳糖)-D-半乳糖。酸水解易使3,6-脫水半乳糖結構破壞,硫醇解則各以二乙基二硫代縮醛出現而穩定。
 醇解反應
醇解反應硫醇解是將糖於0℃溶入濃鹽酸,緩緩加入乙硫醇,0℃放置數小時,熱至室溫,放置幾天即可。後處理是在甲醇懸液中加碳酸鉛中和,過濾,濃縮,產物柱色譜分離,可得結晶性的二乙基二硫縮醛衍生物,以溫熱的HgCl2和CdCO3水溶液使其分解恢復為糖。
酸催化的苯甲醇解也有報導,它的優點是所得到的苄基糖苷能通過Pd/C催化的氫解反應而釋放出糖。
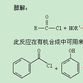
具體例子
醯氯和酸酐可以直接和醇作用生成相應的酯和酸。醯氯性質比較活潑,一般難以製備的酯和醯胺,都可以通過醯氯來合成。例如酚酯不能直接用羧酸與酚酯化製備,但用醯氯則反應可順利進行。
苯酐與甘油發生醇解反應並縮聚成醇酸樹脂,廣泛套用於塗料行業。
醯胺的醇解是可逆的,需用過量的醇才能生成酯並放出氨。酸或鹼對反應有催化作用。
 醇解反應
醇解反應 雙分子親核取代反應
雙分子親核取代反應 醇解反應
醇解反應