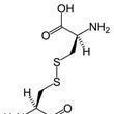
過硫化物差不多只用於生物化學的範疇。與過氧化物(R-O-O-R)相似,它的整體連結是R-S-S-R。
基本介紹
- 中文名:過硫化物
- 化學結構:R-S-S-R
- 核心結構:雙硫鍵
- 代表物質:FeS2
概述,結構,
概述
三個硫原子按序列連結有時被稱為三硫鍵,但其實只是兩個雙硫鍵。
雙硫鍵在一些蛋白質的摺疊及穩定性占有重要的地位,而這些蛋白質多是分泌在細胞外的環境。由於大部分細胞的區間都是還原環境,這令在原生質中的雙硫鍵十分不穩定(但亦有例外)。
胱氨酸是由兩個半胱氨酸以雙硫鍵連合而組成。蛋白質的雙硫鍵是在半胱氨酸殘基的硫醇之間形成。其他含有硫的胺基酸:蛋氨酸就不能形成雙硫鍵。一條雙硫鍵一般是將半胱氨酸的簡寫用連結符號來表示,例如“Cys26-Cys84雙硫鍵”,或簡化為“26-84雙硫鍵”,或更簡單的“C26-C84”,當中已暗示了雙硫鍵而不須明言。蛋白質雙硫鍵的原型是雙胺基酸肽的胱氨酸,它是以雙硫鍵將兩個半胱氨酸結合組成。雙硫鍵結構是以它在Cβ − Sγ − Sγ − Cβ原子之間的χss兩面角來描述,而一般都是接近±90°。
結構
雙硫鍵從以下方式穩定摺疊後的蛋白質:
它將蛋白質的兩部分緊握,使蛋白質形成摺疊的形狀。另一種說法則是它降低非摺疊形狀的蛋白質的熵,使其不穩定。
它會成為摺疊後蛋白質的疏水核心,亦即局部的疏水殘基會凝聚在雙硫鍵的周邊,透過疏水性的相互作用而緊扣在一起。
與1及2有關的,它會與蛋白質鏈的兩段連結,增加蛋白質殘基的局部有效濃度,並降低水分子的局部有效濃度。因為水分子會攻擊氨基之間的氫鍵及打破二級結構,雙硫鍵就可以穩定在附近的二級結構。例如,有研究顯示肽的不同部分在分隔後沒有結構,但在建立雙硫鍵後就有著穩定的二級結構及三級結構。
蛋白質的雙硫鍵是由硫醇雙硫交換反應來形成。disulfide species是指半胱氨酸在雙硫連線蛋白質中的特定配對,一般會以括弧來表示,例如“(26-84, 58-110)disulfide species”。disulfide ensemble則是一組有著相同編號雙硫鍵的disulfide species.並以1S ensemble、2S ensemble等來分別表示有一條、兩條等雙硫鍵的disulfide ensemble。因此,(26-84) disulfide species屬於1S ensemble,而(26-84, 58-110) species則屬於2S ensemble。而沒有雙硫鍵的species就會以R來表示,代表完全還原的意思。在一般的情況下,雙硫鍵的重新現置是比形成新雙硫鍵或是它們的還原來得要快。所以,在ensemble中的disulfide species比在 ensemble之間更快獲得平衡。
蛋白質的原始形式一般是一個單一的disulfide species,而有些蛋白質在功能上會轉變雙硫鍵的狀態,例如硫氧還蛋白。在多於兩個半胱氨酸的蛋白質中,可以生成非原始的雙硫鍵,而這些蛋白質差不多都是沒有摺疊的。當半胱氨酸的數量增加時,非原始的蛋白質會以幾何級數增加。
在真核生物細胞中,雙硫鍵一般是在糙面內質網內生成,而非原生質。這是因內質網的氧化環境及原生質的還原環境(參考谷胱甘肽)。所以雙硫鍵多會在分泌的蛋白質、溶酶蛋白質及膜蛋白質的外漿區域中找到。
但是亦有例外的情況。在原生質的蛋白質附近出現的半胱氨酸殘基會成為氧化感應器,當細胞的還原潛能轉弱時,它們氧化及觸發細胞反應。牛痘病毒亦會產生有著多個雙硫鍵的原生質蛋白質及肽,雖然原因不明,它們有著保護的效力抵抗細胞間的蛋白質加水分解。
雙硫鍵亦會在多種哺乳動物的精子染色質內的精蛋白之間產生。