茚三酮反應(ninhydrin reaction),反應機理,顯色反應方法,常用法,使各種胺基酸呈現不同顏色的方法,使顯色穩定的方法,反應套用,茚三酮顯色法測定殼聚糖含量,茚三酮法定性定量檢測絲氨酸,茚三酮真空熏顯手印,製備茚三酮/納米二氧化鈦複合物,茚三酮顯色反應的影響因素分析,谷氨酸濃度的影響,pH 值的影響,溫度及反應時間的影響,其它影響因素,
茚三酮反應(ninhydrin reaction)
胺基酸的α-NH
2所引起的反應。
α-胺基酸與
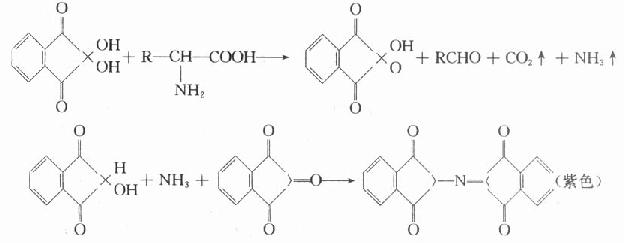
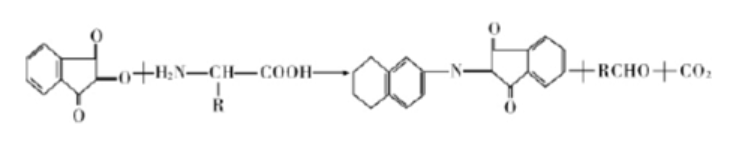
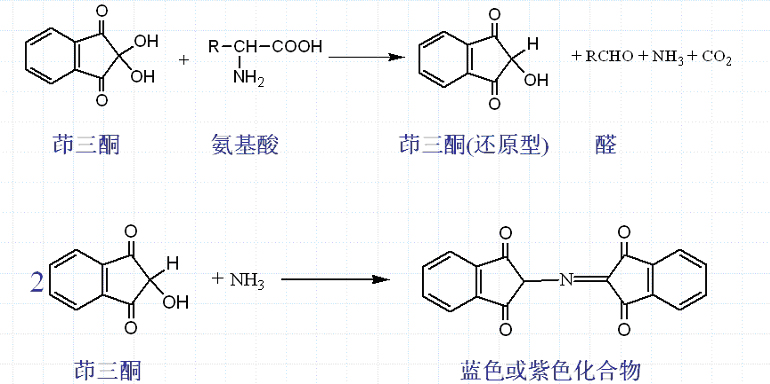
水合茚三酮一起在水溶液中加熱,可發生反應生成藍紫色物質。首先是胺基酸被氧化分解,放出氨和二氧化碳,胺基酸生成醛,水合茚三酮則生成還原型茚三酮。在弱酸性溶液中,還原型茚三酮、氨和另一分子茚三酮反應,縮合生成藍紫色物質。 所有胺基酸及具有游離α-氨基的肽都產生藍紫色,但
脯氨酸和
羥脯氨酸與茚三酮反應產生黃色物質,因其α-氨基被取代,所以產生不同的衍生物。此反應十分靈敏,根據反應所生成的藍紫色的深淺,在570nm波長下進行比色就可測定樣品中胺基酸的含量。也可在分離胺基酸時作為顯色劑定性、定量地測定胺基酸。
此反應十分靈敏,根據反應所生成的藍紫色的深淺,用分光光度計在570nm波長下進行比色就可測定樣品中胺基酸的含量(在一定濃度範圍內,顯色溶液的吸光率與胺基酸的含量成正比),也可以在分離胺基酸時作為
顯色劑對胺基酸進行定性或
定量分析。在法醫學上,使用茚三酮反應可採集嫌疑犯在
犯罪現場留下來的
指紋。因為手汗中含有多種胺基酸,遇茚三酮後起
顯色反應。
反應機理
除脯氨酸、羥脯氨酸和茚三酮反應生成黃色物質外,所有的α-胺基酸及一切蛋白質都能和茚三酮反應生成藍紫色物質。該反應分兩步進行,首先是胺基酸被氧化,產生 CO2 、NH3和醛,而水合茚三酮被還原成還原型茚三酮;第二步是所生成之還原型茚三酮與另一個水合茚三酮分子和氨縮合生成有色物質。此反應的適宜pH為5~7,同一濃度的蛋白質或胺基酸在不同pH條件下的顏色深淺不同,酸度過大時甚至不顯色。該反應十分靈敏,1:1 500 000濃度的胺基酸水溶液即能顯示反應,因此是一種常用的胺基酸定量方法。但也有些物質對茚三酮也呈類似的陽性反應,如β-丙氨酸、氨和許多一級胺化合物等。所以定性或定量測定中,應嚴防干擾物存在。
主要反應分為兩步 (如下圖所示):
第一步 胺基酸 + 弱酸→ 水合茚三酮 + 二氧化碳 + 醛類 + 氨氣
第二步 兩個水合茚三酮 + 氨→ 還原性茚三酮 (藍紫色)
顯色反應方法
顯色方法有下列數種:
常用法
將點有樣品的層析或電泳完畢的濾紙充分除盡溶劑,用 5g/L 茚三酮無水丙酮溶液噴霧,充分吹乾,置 65℃烘箱中約 30min(溫度不宜過高,避免空氣中氨,以免背景泛紅色),胺基酸斑點呈紫紅色。
使各種胺基酸呈現不同顏色的方法
用 0.4g 茚三酮,10g 酚和 90g 正丁醇的混合液顯色。
用 1g/L 茚三酮無水丙酮溶液顯色完畢後,再用鹽酸蒸汽熏 1min。
用 1g 茚三酮,600mL 無水乙醇,200mL 冰醋酸及 80mL2,4,6-三甲基吡啶混合液 80℃染色 5~10min。
使顯色穩定的方法
配製含醋酸鎘 2g 加蒸餾水 200mL 及冰醋酸 40mL 的貯存液。將上述貯存液加 200mL丙酮及 2g 茚三酮,即為顯色液。點有樣品的濾紙上浸有此顯色液後,放置於盛有一小杯濃硫酸的密閉玻璃容器中,25℃,18h,或較高溫度下適當縮短時間。背景色淺,胺基酸斑點也比較穩定。
用含 2g/LCoCl2(或 CuSO4)的 4g/L 茚三酮異丙酮溶液顯色時,胺基酸斑點呈紅色,也可在茚三酮顯色後噴以含鈷、鎘或銅等無機離子的異丙醇溶液,斑點自藍紫色變成紅色。
反應套用
茚三酮反應作為用來檢測α-胺基酸與多肽常用手段。其套用舉例如下:
茚三酮顯色法測定殼聚糖含量
殼聚糖是甲殼素的脫乙醯基衍生物,是一種分子量較大的鹼性多糖。由於分子間和分子內強烈的氫鍵作用,殼聚糖在水及大多數溶劑中的溶解性較差,可溶於醋酸等無機酸的稀溶液中。殼聚糖及其衍生物具有較強的生物活性,具有抗腫瘤、抗凝血、抗血栓、降血脂和增強免疫力等功能。殼聚糖還具有良好的生物降解性和生物相容性,被廣泛套用於生物醫學、環境科學、食品等領域。隨著殼聚糖產品的大量開發及上市,對其進行含量測定也逐漸受到了重視。
有研究根據殼聚糖與茚三酮作用形成的複合物在570nm 處有特徵吸收的特性,建立了利用分光光度法測定殼聚糖含量的方法。該測定方法的適宜條件為:在pH5. 5 的HAc-NaAc 緩衝體系中,當緩衝溶液用量為2. 00mL、茚三酮( 濃度為10. 00g/L ) 用量為1. 00mL、加熱煮沸20min 時,顯色效果最好。
在0. 004~0. 04 g/L 濃度範圍內,殼聚糖濃度與其吸光度值線性關係良好,所得標準曲線方程為:y = 23. 942x + 0. 1423,相關係數r2 =0. 9981。穩定性、重現性和回收率實驗結果表明,該顯色方法在2h 內穩定性良好,精密度可靠。
實驗中發現,殼聚糖與茚三酮作用顯色後,除了在570nm 處有顯著的紫外吸收外,在408nm 處也有一明顯吸收,並且與殼聚糖的濃度具有較好的線性相關性。估計是由於顯色過程中改變了殼聚糖結構所致,在今後的研究中可予以關注。實驗結果表明,利用茚三酮顯色法測定殼聚糖含量的實驗方法操作簡單,反應條件也比較容易控制,且重現性好,適用於樣品中微量殼聚糖的檢測。
茚三酮法定性定量檢測絲氨酸
隨著人們對絲氨酸生理作用的深入認識和醫藥保健事業的不斷發展,醫藥、食品、飼料等行業對絲氨酸的需求量正迅速擴大。雖然L-絲氨酸屬於非必需胺基酸,但它卻具有許多重要的生理功能及用途,在醫藥、食品、化妝品中均有較為廣泛的套用。因此,測定混合胺基酸中絲氨酸的含量對絲氨酸的開發利用具有重要意義。α-胺基酸與茚三酮在弱酸性溶液中共熱,反應後經失水脫羧生成氨基茚三酮,再與水合茚三酮反應生成紫紅色或藍色物質
脯氨酸等仲胺胺基酸與茚三酮反應生成黃色物質。絲氨酸和茚三酮在弱酸性條件下共熱可以生成紫紅色的縮合物質,且其顏色隨著絲氨酸的含量變化而有所不同為了快速簡便地檢測胺基酸水解液中絲氨酸的含量,有研究提出了一種基於胺基酸紙上層析的改進茚三酮顯色法,並將其套用於難以分離的胺基酸的檢測。首先,將茚三酮加入到展層劑中,再對胺基酸混合液進行層析。
在一定條件下將層析後的茚三酮與胺基酸進行顯色反應,根據不同顏色即可鑑別絲氨酸。然後,對不同劑量的絲氨酸標準液使用上述方法繪製絲氨酸標準液的吸光度-含量的標準曲線,用以計算胺基酸水解液絲氨酸的含量。結果表明:茚三酮法定性定量檢測絲氨酸的最佳實驗條件為溶液pH在4.5左右,顯色劑用量為每10mL展層劑中加入2.5mL0.1%茚三酮,並在105℃下加熱5min。
茚三酮真空熏顯手印
1910 年,英國科學家魯赫曼在實驗時,無意中合成一種新的化合物-水合茚三酮。隨後,魯赫曼發現水合茚三酮能與胺基酸反應生成一種紫色產物,這種紫色後被稱為魯赫曼紫。1954 年,兩位瑞典科學家奧登和霍夫施坦首先提出用茚三酮顯現潛在手印。至今,茚三酮一直是顯現滲透客體檢材上潛在指印的最常用、最有效的顯現方法。
茚三酮主要是通過與手印遺留物中的胺基酸發生反應,產生紫色的混合物達到顯現潛在手印的目的。茚三酮在真空加熱情況下可以升華,成茚三酮蒸汽。當茚三酮蒸汽遇到手印遺留物中的胺基酸時,茚三酮與胺基酸發生反應,變成紫色的混合物,從而顯現潛手印。操作時,可以利用真空熏顯櫃,如沒有真空熏顯櫃,也可以直接用酒精燈加熱方法。
操作方法如下:把樣品固定在真空加熱加濕熏顯櫃內,把錫箔碗放在加熱器上,碗中均勻撒放0.1 ~ 0.5g 茚三酮晶體。先把柜子抽到真空,再接通加熱電源,當到達一定溫度時,茚三酮晶體升華變成氣體,與樣品上手印遺留物中的胺基酸發生反應,顯出指紋。
由於真空加熱加濕熏顯儀能加熱,使茚三酮晶體直接升華成氣體,與手印中的胺基酸發生反應;真空條件則保證茚三酮晶體快速升華,變成氣體,並能在櫃內均勻擴散,有效與手印中的胺基酸發生反應,保證顯現質量;加濕能夠有效改善熏顯效果,明顯提高手印顯現率。
製備茚三酮/納米二氧化鈦複合物
製備方法包括:步驟1,配製前驅體溶液;步驟2,利用抽濾將前驅體溶液通過經脫水處理的濾膜,使濾膜飽和吸附前驅體溶液;步驟3,同樣利用抽濾將茚三酮溶液通過濾膜,反應生成茚三酮/納米二氧化鈦複合物。所述複合物對胺基酸具有較好的顯色靈敏度,可作為薄層層析板檢測胺基酸的顯色劑。將上述複合物摻入到薄層層析板的固定相中製得新型薄層層析板,利用該薄層層析板可實現層析分離與顯色過程一步完成,使用便捷。
茚三酮顯色反應的影響因素分析
茚三酮與谷氨酸的顯色反應靈敏度較高 ,但同時也受到多種因素的影響。
當實驗條件控制不好時 ,會造成實驗數據的較大偏離 ,從而產生較大的誤差。此顯色反應的影響因素主要有以下幾方面。
谷氨酸濃度的影響
實驗表明 ,谷氨酸與茚三酮水溶液在表 3所注條件下反應的最低顯色濃度為70μg/ mL 。隨谷氨酸濃度變大 ,顯色逐漸變深。當濃度大於 140μg/ mL 時 ,所顯顏色過深且其光密度值超出量程。當谷氨酸濃度在 80~140μg/ mL時 ,顏色變化明顯且顯色較穩定。
| 表1 濃度對顯色反應的影響 |
|---|
谷氨酸濃度(μg/ mL) | 顏色變化 |
60
70
100
150 | 基本無色
略帶淺藍
淺藍
深藍 |
注 :90 ℃下水浴 25 min ,谷氨酸標準液 5mL ,茚三酮水溶液 1mL ,p H6. 0。
pH 值的影響
以 100μg/ mL 的谷氨酸標準液在不同pH下進行顯色反應 ,測得結果如表 。
| 表 2 pH 值對顯色反應的影響 |
|---|
谷氨酸濃度(μg/ mL) | pH 值 | 顏色變化 |
100
100
100
100
100 | 2
4
6
8
10 | 無色
無色
淺藍
淺藍
淺藍 |
注 :90 ℃下水浴 25 min ,谷氨酸標準液 5mL ,茚三酮水溶液 1mL
由表 2可見 ,顯色反應隨 pH的不同顏色有明顯的變化。當 pH在 4 以下時不顯色 ,而 pH 在 6~10 時 ,顏色變化明顯。但因茚三酮的水溶液在鹼性條件下溶液本身帶有明顯的淡黃色 ,因此 pH選定在 6 左右較好 ,此時基本無顏色干擾且顯色穩定。
溫度及反應時間的影響
實驗表明 ,溫度和反應時間對此顯色反應的影響也很大。以 100μg/ mL 的谷氨酸標準液在 70 ℃進行顯色發應時 ,發現即使加熱30 min 也基本無顏色變化。當溫度為 80 ℃時 ,加熱 30 min 以上有顏色變化 ,而當溫度為 90 ℃時 ,加熱 15 min 左右即有明顯的顏色變化 ,沸水加熱時顏色變化也很明顯。但考慮到蒸發的影響 ,所以實驗選用 90 ℃作為最佳反應溫度。在顯色反應中 ,反應時間主要根據具體的顏色變化而定。一般來說 ,當谷氨酸濃度在 80~140μg/ mL 時 ,90 ℃加熱 20 min 以上即可完全反應。時間太短 ,反應不完全 ,顏色梯度不明顯 , 所以最佳反應時間在 20 ~25 min。
| 表 3 溫度及反應時間對顯色反應的影響 |
|---|
谷氨酸濃度
(μg/ mL )
| pH | 反應時間 (min) | 反應溫度( ℃) |
70 | 80 | 90 |
100
100
100
100 | 6. 0
6. 0
6. 0
6. 0 | 15
20
25
30 | 無色
無色
無色
無色 | 無色
無色
無色
淺藍 | 無色
淺藍
淺藍
淺藍 |
注 :谷氨酸標準液 5mL ,茚三酮水溶液 1mL 。
其它影響因素
茚三酮的不同溶劑對顯色反應也有影響。實驗表明 ,茚三酮的丙酮溶液在 80 ℃以上時顯色較好 ,而茚三酮的水溶液要在 90 ℃以上時顯色才明顯。茚三酮的用量對顯色反應的影響不大 ,可選擇 5mL (或 3mL) 被測液與 1mL (或 0. 5 mL) 茚三酮溶液反應。測定時 ,最好選擇谷氨酸標準樣與待測稀釋液一同水浴 ,這樣可提高測定的準確度。此外 ,當被測樣品中含有其它胺基酸時也可與茚三酮發生顯色反應 ,從而影響測定結果。但在谷氨酸發酵中 ,所產的谷氨酸含量一般是其它胺基酸的幾十倍 ,故此影響因素可忽略不計。
總之 ,茚三酮比色法作為一種穀氨酸的定量檢測方法 ,具有操作簡單、成本低的優點。只要控制好實驗條件 ,就能取得較好的測量結果。這對於一般實驗室的樣品分析及味素生產廠家的谷氨酸產品測定 ,有較好的實用價值。