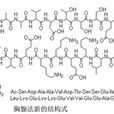
本品為化學合成的由二十八個胺基酸組成的多肽。為N-乙醯基-L-絲氨醯-L-α-天冬氨醯-L-丙氨醯-L-丙氨醯-L-纈氨醯-L-α天冬氨醯-L-蘇氨醯-L-絲氨醯-L-絲氨醯-L-α谷氨醯-L-異亮氨醯-L-蘇氨醯-L-蘇氨醯-L-賴氨醯-L-α-天冬氨醯-L-亮氨醯-L-賴氨醯- L-α-谷氨醯-L-賴氨醯-L-賴氨醯-L-α-谷氨醯-L-纈氨醯-L-纈氨醯-L-α-谷氨醯- L-α-谷氨醯-L-丙氨釀-L-α-谷氨醯-L-天冬醯胺。按無水、無醋酸物計算,含胸腺法新(C129 H215 N33O55 )應為 95.0%〜105.0% 。
基本介紹
- 中文名:胸腺法新
- 外文名:Thymalfasin
- 外觀:白色或類白色粉末或疏鬆塊狀物
- 水溶性:微溶
- 分子式:C129H215N33O55
- 分子量:3108.28
化合物藥典標準,結構式,性狀,比旋度,鑑別,檢查,含量測定,藥理毒理,藥理作用,毒理研究,藥代動力學,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,藥物相互作用:,藥物過量,
化合物藥典標準
結構式
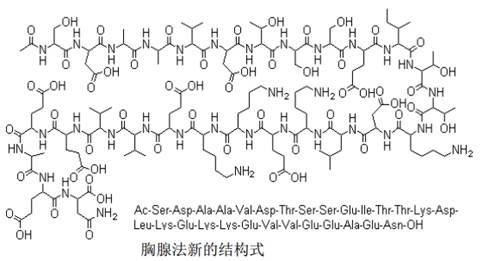
性狀
本品為白色或類白色粉末或疏鬆塊狀物。
本品在三氟醋酸中溶解,在水中微溶,在乙腈、乙醚和三氯甲烷中不溶。
比旋度
取本品,精密稱定,加0.02mol/L磷酸鹽緩衝溶液(pH 7.0)(取磷酸二氫鉀2.72g,加0.1mol/L氫氧化鈉溶液116.4ml溶解,用水稀釋至1000ml)定量稀釋製成每1ml中約含5mg的溶液,依法測定(2010年版藥典二部附錄ⅥE),以無水與無醋酸物計算,比旋度應為-100.0°至-110.0°。
鑑別
(1)取本品約2mg,加水1ml溶解後,加鹼性酒石酸銅試液1ml,即顯藍紫色。
(2)在含量測定項下記錄的色譜圖中,供試品溶液主峰的保留時間應與對照品溶液主峰的保留時間一致。
檢查
1胺基酸比值
取本品適量,加鹽酸溶液(1→2),於110℃水解24小時後,照適宜的胺基酸分析方法測定。以門冬氨酸、谷氨酸、丙氨酸、亮氨酸、異亮氨酸、賴氨酸的摩爾數總和除以19作為1,計算各胺基酸的相對比值,應符合以下規定:門冬氨酸3.4~4.6,谷氨酸5.4~6.6,絲氨酸2.4~3.6,蘇氨酸2.4~3.6,丙氨酸2.7~3.3,纈氨酸2.4~3.6,亮氨酸0.8~1.2,異亮氨酸0.8~1.2,賴氨酸3.4~4.6。
2溶液的澄清度與顏色
取本品適量,加0.02mol/L磷酸鹽緩衝溶液(pH 7.0)(取磷酸二氫鉀2.72g,加 0.lmol/L氫氧化鈉溶液116.4ml溶解,用水稀釋至1000ml)溶解並製成每1ml中含1.6mg的溶液,依法檢查(2010年版藥典二部附錄ⅨA和2010年版藥典二部附錄Ⅸ B),溶液應澄清無色。如顯渾濁,與1號濁度標準液比較,不得更濃。
3醋酸
取本品適量,精密稱定,加稀釋液[流動相A-甲醇(95:5)]溶解並定量稀釋製成每1ml中含2.0mg的溶液,作為供試品溶液。照合成多肽中的醋酸測定法(2010年版藥典二部附錄ⅦN)測定,含醋酸不得過5.0%。
4有關物質
取本品適量,加0.02mol/L磷酸鹽緩衝溶液(pH 7.0)溶解並稀釋製成每1ml中含胸腺法新0.5mg的溶液作為供試品溶液;精密量取供試品溶液2ml,置100ml量瓶中,用0.02mol/L磷酸鹽緩衝溶液(pH 7.0)稀釋至刻度,搖勻,作為對照溶液。照含量測定項下的色譜條件,取對照溶液20μl,注入液相色譜儀,調節檢測靈敏度,使主成分色譜峰的峰高約為滿量程的10%。再精密量取供試品溶液和對照溶液各20μl,分別注入液相色譜儀,記錄色譜圖。供試品溶液的色譜圖中如有雜質峰,除溶劑峰和醋酸峰外,單個雜質峰面積不得大於對照溶液主峰面積(2.0%),各雜質峰面積總和不得大於對照溶液主峰面積的2倍(4.0%)。
5水分
取本品,照水分測定法(2010年版藥典二部附錄ⅧM第一法)測定,含水分不得過5.0%。
含量測定
照高效液相色譜法(2010年版藥典二部附錄ⅤD)測定。
1色譜條件與系統適用性試驗
用十八烷基矽烷鍵合矽膠為填充劑;以乙腈-水-磷酸(140:860:1)為流動相A;以乙腈-水-磷酸(250:750:1)為流動相B;檢測波長為210nm。按下表進行梯度洗脫。理論板數按胸腺法新峰計算不低於2000,胸腺法新峰與相鄰雜質峰的分離度應符合要求。
時間(分鐘) | 流動相A(%) | 流動相B(%) |
0 | 100 | 0 |
30 | 50 | 50 |
31 | 0 | 100 |
35 | 0 | 100 |
35.1 | 100 | 0 |
45 | 100 | 0 |
2測定法
取本品適量,精密稱定,加0.02mol/L磷酸鹽緩衝溶液(pH 7.0)溶解並定量稀釋製成每1ml中含胸腺法新0.5mg的溶液,作為供試品溶液;精密量取20μl注入液相色譜儀,記錄色譜圖;另取胸腺法新對照品適量,同法測定。按外標法以峰面積計算,即得。
藥理毒理
藥理作用
本品治療慢性B型肝炎和增強免疫系統反應性的作用機制尚未完全闡明。多項體外試驗顯示,本品通過刺激外周血液淋巴細胞絲裂原來促進T淋巴細胞的成熟,增加抗原或絲裂原激活後T細胞分泌的干擾素α、干擾素γ以及白介素2、白介素3等淋巴因子水平,同時增加T細胞表面淋巴因子受體水平。本品還可通過對CD4細胞的激活,增強異體和自體的人類混合淋巴細胞反應。本品可能增加前NK細胞的聚集,而干擾素可使其細胞毒性增強。體內試驗顯示,本品可以提高經刀豆蛋白A激活後小鼠淋巴細胞白介素2受體的表達水平,同時提高白介素2的分泌水平。
毒理研究
遺傳毒性:本品遺傳毒性試驗結果陰性。
生殖毒性:本品對動物胎仔無明顯致畸作用。目前尚不清楚妊娠婦女使用本品後,是否會影響其生殖能力或對胎兒造成損害。只有在確實需要時,妊娠婦女才能使用本品。同樣,目前也不清楚本品是否能夠經人乳汁分泌,因此哺乳期婦女使用本品時應慎重。
藥代動力學
健康人單次皮下注射胸腺法新1.6mg,血藥峰濃度約為37.51ng/ml,達峰時間約為1.67小時,AUC0-15約為152.15ng/ml·h,半衰期約為1.65小時
適應症
1.慢性B型肝炎。
2.作為免疫損害病者的疫苗免疫應答增強劑。免疫系統功能受到抑制者,包括接受慢性血液透析和老年病患者,本品可增強病者對病毒性疫苗,例如流感疫苗或B肝疫苗的免疫應答。
規格
1.6mg。
用法用量
用前每瓶胸腺法新(1.6mg)以1ml注射用水溶解後立即皮下注射(不應作肌注或靜注)
治療慢性B型肝炎的推薦劑量:每次1.6mg,每周2次,兩次相隔3-4天。連續給藥6個月(共52針),其間不應間斷。
作為免疫損害病者的疫苗免疫應答增強劑:每次1.6mg,每周2次,兩次相隔3-4天。連續4周(共8針),第一針應在給疫苗後立即皮下注射。
不良反應
胸腺法新的耐受性良好。部分患者可有注射部位不適。慢性B肝患者接受本品治療時,可能出現ALT水平暫時波動至基礎值兩倍以上,此時通常應繼續使用,除非有肝衰竭的症狀和預兆出現。
禁忌
- 對本品成份過敏者禁用;
- 正在接受免疫抑制治療的患者如器官移植者禁用。
注意事項
- 當用來治療慢性B肝時,肝功能試驗,包括血清ALT、白蛋白和膽紅素應在治療期間作定期評估,治療完畢後應檢測B肝e抗原(HBeAg)、表面抗原HBsAg、HBV-DNA和ALT酶,亦應在治療完畢後2、4和6個月檢測,因為病人可能在治療完畢後隨訪期內出現應答。
- 本品應在醫師指導下套用。如患者自行在醫院外使用,應注意注射器具的消毒和處理。
孕婦及哺乳期婦女用藥
基礎研究顯示本品對動物胚胎沒有影響,但尚不明確本品是否會對孕婦胚胎產生影響,以及是否經由乳汁排泄,故此部分患者用藥應慎重,須遵醫囑。
兒童用藥
對18歲以下患者,本品的安全性和有效性尚未確定,故不推薦使用。
藥物相互作用:
本品可與α干擾素聯合使用,可提高免疫應答,與其他免疫藥物聯合使用時應慎重。本品不得與任何藥物混合注射。本品不得與任何藥物混合注射。
藥物過量
目前未見任何有關在人體用藥過量(治療或意外)的報告。