濕法煉銅用硫酸將銅礦中的銅元素轉變成可溶性的硫酸銅,再將鐵放入硫酸銅溶液中把銅置換出來,這種方法叫濕法煉銅。濕法煉銅技術是我國古代人發明的,其原理就是用置換反應製取金屬。我國是世界上最早使用濕法煉銅的國家。
基本介紹
原理簡介
詳細內容
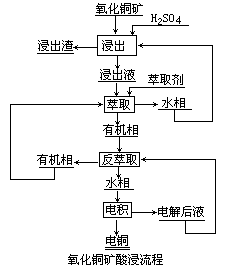 濕法煉銅
濕法煉銅
濕法煉銅用硫酸將銅礦中的銅元素轉變成可溶性的硫酸銅,再將鐵放入硫酸銅溶液中把銅置換出來,這種方法叫濕法煉銅。濕法煉銅技術是我國古代人發明的,其原理就是用置換反應製取金屬。我國是世界上最早使用濕法煉銅的國家。
 濕法煉銅
濕法煉銅濕法煉銅用硫酸將銅礦中的銅元素轉變成可溶性的硫酸銅,再將鐵放入硫酸銅溶液中把銅置換出來,這種方法叫濕法煉銅。濕法煉銅技術是我國古代人發明的,其原理就是用...
《濕法煉銅工藝·設備與控制》對濕法煉銅企業生產一線的操作工人、機電維修人員都有重要的參考價值,尤其是對剛參加工作的新職工,通過自學將會得到事半功倍的效果,對...
煉銅,精煉的銅,出自《戰國策·趙策一》。...... 用硫酸將銅礦中的銅轉變成可溶性的硫酸銅,再將鐵放入硫酸銅溶液中把銅置換出來,這種方法叫濕法煉銅。濕法煉銅技術...
張潛(1025—1105),字明叔,今江西省德興市(上饒市管轄)銀城鎮吳園人,北宋著名濕法煉銅家。張潛是西漢張良後裔,唐宋時家族逐漸南移,至德興新營定居後,三世同居,...
奧托昆普公司提出了濕法煉銅新工藝,即用NaOH 由淨化後的浸出母液中沉澱出Cu2O;在氯-鹼電解槽中再生NaOH;氯鹼電解的其他產物(氯氣、氫氣)也在工藝中循環利用;氯氣送...
西漢時期中國古老的冶銅方法。主要的反應原理是鐵置換硫酸銅生成銅和硫酸亞鐵。濕法煉銅是鐵、硫酸銅之間的反應,可能不純,形成鐵、銅混合物。化學式為:Fe+CuSO4...
濕法煉銅,古書記載“曾青得鐵則化為銅”,“曾青”即硫酸銅溶液,向其中加入鐵,由於鐵的金屬活潑性強於銅,所以可將銅元素置換,得到單質銅,這就是濕法煉銅。 ...
濕法冶金是將礦石、經選礦富集的精礦或其他原料經與水溶液或其他液體相接觸,通過化學反應等,使原料中所含有的有用金屬轉入液相,再對液相中所含有的各種有用金屬...
本書結合銅冶煉企業的實際情況,具體地總結了從精礦到電解銅、濕法煉銅、再生銅生產過程中各個環節的技術內容,主要包括冰銅熔煉與吹煉的基本原理、工藝,設備及實踐;...
銅錠濕法煉銅 一船適於低品位的氧化銅,生產出的精銅稱為電積銅。 現代濕法冶煉有硫酸化焙燒-浸出-電積,浸出-萃取-電積,細菌浸出等法,適於低品位複雜礦、氧化...
位於江西省德興市。唐、宋年間已經開採,用濕法煉銅(見膽銅法)。1956年開始普查勘探,發現有兩個大型斑岩銅礦區,並伴生有鉬、硫、金、銀等元素。1958年5月成立...
