基本介紹
- 中文名:汽液平衡比
- 外文名:Vapor-liquid equilibrium ratio
- 拼音:qì yè píng héng bǐ
- 學科:化學
- 領域:冶金相圖
- 相關概念:相圖、組分、相、獨立組分數
簡介
K值
相關概念
氣相
液相
組分數
相律
相圖分析
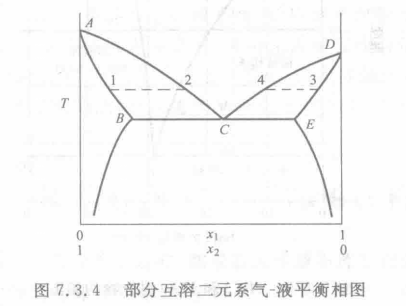 二元系氣液平衡相圖
二元系氣液平衡相圖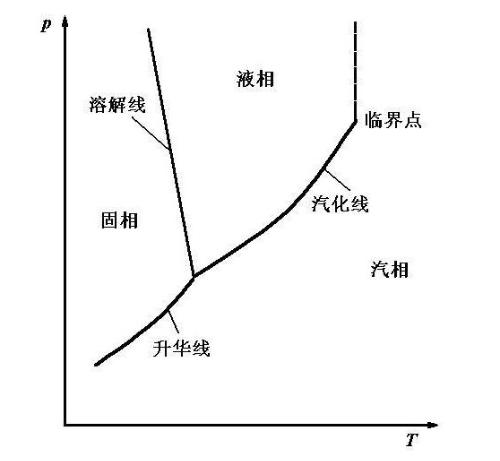
 二元系氣液平衡相圖
二元系氣液平衡相圖汽液平衡比(Vapor-liquid equilibrium ratio)是指在一定的條件下,多元系的氣、液相呈平衡時,氣相和液相中組分R的濃度分別為y和x,它們的比值稱為汽液平衡比K。...
汽液平衡,汽相與液相間的相平衡。它與氣液平衡有一些共同的規律,所以有時把它與氣液平衡合在一起進行研究。為簡便起見,常把汽相或氣相與液相之間的平衡合寫成...
氣液平衡 vapour-liquid equilibrium,是由n個組分的混合物構成一個封閉系統,並有氣-液兩相共存,一定的溫度和壓力下,兩相達到平衡時,各組分在汽液兩相中的化學位...
汽固平衡是汽相與固相間的相平衡。...... 的平衡,有氣液平衡、氣固平衡、汽液平衡、汽固平衡、液液平衡、液固平衡和固固平衡;相數多於2的系統,有氣液固平衡...
雙液系汽液平衡相圖是指兩種在常溫時為液態的物質,混合而成的二組分體系,若能按任意比例互相溶解,稱完全互溶雙液系;若只能在一定比例範圍內互相溶解,稱部分互...
以氣液平衡數據為目的的測定中,利用氣液平衡裝置常常附帶提供一些純物質的蒸氣壓,一般說來,這些數據可靠性差些,只有在缺乏專門蒸氣壓測定數據時,才引用這樣的數據...
相平衡常數指在一定溫度和壓力下,氣液兩相達到平衡狀態時,氣相中某一組分的摩爾分數與其液相中此組分的摩爾分數的比值。表達的是互成平衡的氣-液兩相組成之間的...
《多元氣-液平衡和精餾》是2002年1月由石油工業出版社石油工業出版社出版的圖書,作者是郭天民。...
電磁場對汽液平衡影響的研究Study on effect of electric field and magnetic field on vapor-liquid equilibrium,唐洪波著。...
汽液兩相流疏水器是套用“兩相流理論”“控制流體理論”開發的新一代節能環保產品,在火力發電機組運行中,為了提高蒸汽系統的效率和保證蒸汽設備的安全和經濟運行,...
閃蒸計算是指在已知系統總組成的情況下,求一定溫度、壓力下,達到平衡的氣液兩相組成與數量之比,它是氣液平衡計算的基本內容之一。 [1] ...
