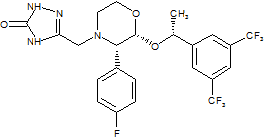藥品信息
基本信息
【商品名稱】意美®(EMEND®)
【通用名稱】阿瑞匹坦膠囊
【英文名稱】Aprepitant Capsules
【漢語拼音】Aruipitan Jiaonang
【主要成分】阿瑞匹坦
【規格】(1)80mg;(2)125mg
【劑型】口服膠囊
【包裝】鋁塑板包裝。
【貯藏】30℃以下原包裝保存。。
【有效期】48個月
【進口藥品註冊證號】
80mg:H20130543
125mg:H20130544
80mg和125mg:H20130545
【生產企業】
公司名稱:Merck Sharp & Dohme Australia Pty Ltd
地址:54-68 Ferndell Street, South Granville, NSW 2142, Australia
生產廠名稱:Merck Sharp & Dohme Corp.
地址:770 Sumneytown Pike, West Point, Pennsylvania 19486, USA
包裝廠名稱:Merck Sharp & Dohme Australia Pty Ltd
地址:54-68 Ferndell Street, South Granville, NSW 2142, Australia
【成分】
本品主要成分為阿瑞匹坦
化學名稱:5-[[(2R,3S)-2-[(1R)-1-[3,5-二 (三氟甲基) 苯基]乙氧基]-3-(4-氟苯基)-4-嗎啉基]甲基]-1,2-二氫-3H-1,2,4-三唑-3-酮
化學結構式:
分子式:C23H21F7N4O3
分子量:534.43
【性狀】
本品為硬膠囊,內容物為類白色小丸。
80mg:白色不透明硬膠囊,印有‘461’和‘80mg’的字樣。
125mg:不透明硬膠囊,白色囊身和粉色囊帽,印有‘462’和‘125mg’的字樣。
適應症
阿瑞匹坦膠囊與其它止吐藥物聯合給藥,適用於預防高度致吐性抗腫瘤化療的初次和重複治療過程中出現的急性和遲發性噁心和嘔吐。(參見“用法用量”)
用法用量
本品的劑型為口服膠囊。
在阿瑞匹坦膠囊與一種糖皮質激素和一種5-HT3拮抗劑聯合治療方案中,本品給藥3天。在開始治療前需仔細閱讀5-HT3拮抗劑的說明書。本品的推薦劑量是在化療前1小時口服125mg(第1天),在第2和第3天早晨每天一次口服80mg。
在一項在中國開展的臨床研究中,使用了以下治療方案預防高度致吐性抗腫瘤化療導致的噁心和嘔吐:
| 第1天
| 第2天
| 第3天
| 第4天
|
阿瑞匹坦*
| 口服125 mg
| 口服80 mg
| 口服 80 mg
| 無
|
地塞米松**
| 口服6 mg
| 口服3.75 mg
| 口服3.75 mg
| 口服3.75 mg
|
格拉司瓊†
| 靜脈輸注3 mg
| 無
| 無
| 無
|
*在第1天化療前1小時以及第2天和第3天早晨口服阿瑞匹坦。
**在第1天化療前30分鐘以及第2-4天的早晨服用地塞米松,服用劑量根據藥物相互作用確定。
†在第1天化療前30分鐘使用格拉司瓊。
一般信息
關於本品與糖皮質激素聯合套用時的其它信息參見“藥物相互作用”。
聯合使用的止吐劑可參見其說明書。
本品可以與食物同時服用,也可以不與食物同時服用。
不同年齡、性別、種族及身體質量指數(BMI)的患者不需要調整藥物的劑量。
重度腎功能不全的患者(肌酐清除率<30ml/min)和進行血液透析的終末期腎病患者均不需要調整本品的給藥劑量。
輕、中度肝功能不全(Child-Pugh分級評分5-9分)的患者不需要調整本品的給藥劑量。目前尚沒有重度肝功能不全(Child-Pugh分級評分>9分)的患者使用本品的臨床研究資料。
禁忌
禁用於對本品中任何成分過敏者。
本品不應與匹莫齊特、特非那定、阿司咪唑、西沙比利同時使用。阿瑞匹坦可對細胞色素P450的同功酶3A4(CYP3A4)產生劑量依賴性抑制,而使這些藥物的血藥濃度升高,從而有可能引起嚴重的或危及生命的不良反應(見“藥物相互作用”)。
注意事項
本品是一種劑量依賴性CYP3A4抑制劑,在主要通過CYP3A4代謝的藥物的患者中聯用時必須慎用;某些化療藥物是通過CYP3A4代謝的(參見藥物相互作用)。阿瑞匹坦125mg/80mg療法對CYP3A4的中度抑制作用可使這些同時服用藥物的血藥濃度升高(參見“藥物相互作用”)。
本品與華法林同時使用時,可導致凝血酶原時間的國際標準化比率(INR)明顯降低。需要長期服用華法林治療的患者,在每個化療周期開始使用本品的3天給藥方案後的兩周時間內,特別是在第7-10天,應該密切監測INR(見“藥物相互作用”)。
在本品服藥期間和服藥後28天內,可使性激素避孕藥的療效減低。因此,在使用本品治療期間和在本品最後一次給藥後的1個月內,應該選擇其他避孕措施或使用補救方法進行避孕(見“藥物相互作用”)。
【孕婦及哺乳期婦女用藥】
尚未在孕婦中進行充分和對照良好的研究。只有當對母親和胎兒的潛在收益超過潛在風險時,才可在妊娠期間使用阿瑞匹坦。
阿瑞匹坦可以分泌到大鼠的乳汁中。尚不清楚本品是否可以分泌到人的乳汁中。由於許多藥物可分泌到人乳汁中,並且本品對接受哺乳的嬰兒可能產生的不良反應,因此,必須根據藥物對母親的重要性決定是否停止哺乳或停止藥物治療。
【兒童用藥】
在兒童中使用本品的安全性和有效性尚未確定。
【老年用藥】
在臨床研究中,老年人(年齡365歲)使用本品的安全性和有效性與較年輕患者(<65歲)相當。因此,老年患者使用本品無需調整劑量。
藥物相互作用
阿瑞匹坦是CYP3A4的底物、較輕至中度(劑量依賴性)抑制劑和誘導劑。阿瑞匹坦也是CYP2C9誘導劑。
藥物相互作用數據均來自國外研究。在一項國內臨床研究中觀察到中國患者的阿瑞匹坦暴露水平較高。必須慎重監測臨床相關的藥物相互作用。
阿瑞匹坦對其它藥物的藥代動力學的影響
作為CYP3A4的中度(125mg/80mg)抑制劑,阿瑞匹坦可增加通過CYP3A4代謝的口服藥物的血漿濃度。阿瑞匹坦(125mg/80mg)也可增加通過CYP3A4代謝的靜脈用藥物的血漿濃度,但相對口服藥物程度較小。
本品不得與匹莫齊特、特非那定、阿司咪唑、或西沙必利聯合使用。阿瑞匹坦對CYP3A4的劑量依賴性抑制作用可導致這些藥物的血漿濃度升高,可能導致嚴重的或危及生命的反應(參見“禁忌”)。
研究表明,阿瑞匹坦可誘導通過CYP2C9代謝的S(-)華法林和甲苯磺丁脲的代謝。本品與這些藥物和其它已知的通過CYP2C9代謝的藥物如苯妥英聯合使用時,可導致這些藥物的血藥濃度降低。
本品與P-糖蛋白轉運蛋白的底物類藥物之間沒有相互作用,原因是在臨床藥物相互作用研究中,本品與地高辛之間未顯示有相互作用。
5-HT3拮抗劑:在臨床藥物相互作用研究中,阿瑞匹坦對昂丹司瓊、格拉司瓊或羥基多拉司瓊(多拉司瓊的活性代謝產物)的藥代動力學的影響沒有臨床意義。
糖皮質激素:
地塞米松:阿瑞匹坦125mg與第1天口服地塞米松20mg聯合治療以及本品每日80mg與第2至第5天口服地塞米松8mg聯合治療,可導致CYP3A4底物地塞米松在第1天和第5天的AUC增加2.2倍。因此,如果與阿瑞匹坦(125mg/80mg療法)聯合使用,地塞米松的常規口服劑量應減少約50%,使地塞米松的暴露水平與未使用本品時的暴露水平相似。在關於阿瑞匹坦預防化療誘導的噁心和嘔吐的臨床研究中,地塞米松的每日劑量大約減少50%(參見”用法用量“)。
甲基潑尼松龍:第1天口服阿瑞匹坦125mg,第2至第3天口服每日80mg,可使CYP3A4底物甲基潑尼松龍在第1天和第3天的AUC分別增加1.3倍和2.5倍,其中甲基潑尼松龍的給藥方案為第1天給予125mg,靜脈輸注,第2天和第3天口服40mg。因此,與阿瑞匹坦(125mg/80mg療法)聯合使用時,甲基潑尼松龍的常規靜脈輸注劑量必須減少約25%,而口服甲基潑尼松龍的常規劑量應減少約50%,使甲基潑尼松龍的暴露水平與未使用阿瑞匹坦時的暴露水平相似。
化療藥物:在臨床研究中,聯合使用阿瑞匹坦(125mg/80mg療法)和以下主要或部分通過CYP3A4代謝的化療藥物:依託泊苷、長春瑞濱、多烯紫杉醇和紫杉醇,無需根據潛在的藥物相互作用對這些藥物的劑量進行調整。
在國內臨床研究中,接受CYP3A4底物長春花鹼和長春新鹼的患者數量少,故與這些藥物相互作用信息有限。鑒於國內臨床研究觀察到中國患者的阿瑞匹坦暴露水平較高,必須特別注意監測接受長春花鹼和長春新鹼或其它通過CYP3A4代謝的化療藥物的患者安全。
多西他賽:在一項單獨的藥代動力學研究中,阿瑞匹坦(125mg/80mg療法)未對多西他賽的藥代動力學產生影響。
長春瑞濱:在一項單獨的藥代動力學研究中,阿瑞匹坦(125mg/80mg療法)未對長春瑞濱的藥代動力學產生影響。
華法林:在穩定接受長期華法林治療的健康受試者中,在第1天單次口服阿瑞匹坦125mg,在第2天和第3天口服每日80mg。儘管阿瑞匹坦對第3天測定的R(+)或S(-)華法林的血漿AUC沒有影響,但在阿瑞匹坦治療結束後5天內,S(-)華法林(CYP2C9底物)的谷濃度下降34%,而凝血酶原時間(報告為國際標準化比值或INR)縮短14%。因此,在接受長期華法林治療的患者中,在每個化療周期的為期3天的阿瑞匹坦治療後,必須在2周時間內對凝血酶原時間(INR)進行密切監測,尤其是7至10天內。
甲苯磺丁脲:第1天口服阿瑞匹坦125mg,第2天和第3天口服每日80mg,而在為期3天的阿瑞匹坦治療前和第4、8和15天單次口服甲苯磺丁脲500mg後,甲苯磺丁脲(CYP2C9底物)在第4天、第8天和第15天的AUC分別降低23%、28%和15%。
口服避孕藥:聯合使用阿瑞匹坦100mg膠囊,每日一次,為期14天與含35ug炔雌醇和1mg炔諾酮的口服避孕藥可使炔雌醇的AUC降低43%,炔諾酮的AUC降低8%。
在另一項研究中,在第1至21天口服含炔雌醇和炔諾酮的口服避孕藥,每日一次,在第8天口服阿瑞匹坦125mg,第9天和第10天口服阿瑞匹坦每日80mg,在第8天給予昂丹司瓊32mg靜脈輸注並單次口服地塞米松12mg,第9、10和11天口服地塞米松每日8mg。在這項研究中,炔雌醇在第10天的AUC下降19%,而在第9至21天,炔雌醇的谷濃度下降64%。儘管阿瑞匹坦對於第10天的炔諾酮AUC沒有影響,但在第9至21天,炔諾酮的谷濃度下降60%。
在阿瑞匹坦治療期間和治療後28天內,激素類避孕藥的有效性下降。在阿瑞匹坦治療期間和最後一次阿瑞匹坦治療後1個月內,應使用備選或備份避孕方法。
咪達唑侖:在第1天口服阿瑞匹坦125mg,第2至5天口服每日80mg,並在第1天和第5天單次口服咪達唑侖2mg後,阿瑞匹坦可使敏感的CYP3A4底物咪達唑侖在第1天和第5天的AUC分別增加2.3倍和3.3倍。聯合使用阿瑞匹坦(125mg/80mg)與這些藥物時,必須考慮到咪達唑侖或其它通過CYP3A4代謝的苯二氮卓類藥物(阿普唑侖、三唑侖)的血藥濃度升高的潛在影響。
在另一項關於咪達唑侖,靜脈輸注的研究中,在第1天口服阿瑞匹坦125mg,第2天和第3天口服阿瑞匹坦每日80mg,在為期3天的阿瑞匹坦治療前以及阿瑞匹坦治療第4、8和15天給予咪達唑侖2mg,靜脈輸注。與第1至3天的阿瑞匹坦治療期相比,本品可使咪達唑侖在第4天的AUC升高25%,而使咪達唑侖在第8天的AUC下降19%。這些效應不存在重要的臨床意義。咪達唑侖在第15天的AUC與基線期的觀察結果相似。
還完成了一項關於靜脈給藥的咪達唑侖和阿瑞匹坦的研究。在單次口服阿瑞匹坦125mg後1小時給予咪達唑侖2mg,靜脈輸注。咪達唑侖的血漿AUC增加1.5倍。這一效應無重要的臨床意義。
藥物過量
尚未獲得本品過量用藥的特定信息。健康受試者單次口服最大劑量為600mg的阿瑞匹坦通常具有良好的耐受性。在參加非CINV研究的患者中,阿瑞匹坦375mg,每日一次,最長為期42天基本上具有良好的耐受性。在33名癌症患者中,在第1天單次口服375mg阿瑞匹坦和在第2至5天口服250mg,每日一次,基本上具有良好的耐受性。
1名接受1440mg阿瑞匹坦治療的患者出現了睏倦和頭痛的症狀。
如果發生過量用藥,必須停止本品治療,並採取一般支持性治療和監測。由於阿瑞匹坦具有止吐活性,因此採用藥物誘導嘔吐的措施對阿瑞匹坦可能無效。
阿瑞匹坦無法通過血液透析清除。
藥理毒理
藥理作用
阿瑞匹坦是人P物質神經激肽1(NK1)受體的選擇性高親合力拮抗劑。對其他現有治療化療引起噁心嘔吐(CINV)和術後噁心嘔吐(PONV)的藥物的作用靶點5-羥色胺受體3(5-HT3)、多巴胺受體和糖皮質激素受體的親和力低或無親和力。
臨床前研究表明,NK1受體拮抗劑可抑制細胞毒化療藥物如順鉑,引起的嘔吐。阿瑞匹坦的臨床前和人體正電子發射斷面成像(PET)研究顯示,阿瑞匹坦可透過血腦屏障,占領腦內NK1受體。阿瑞匹坦可抑制順鉑引起的急性期和延遲期嘔吐,並增強5-HT3受體拮抗劑昂丹司瓊和糖皮質激素地塞米松對順鉑引起的嘔吐的止吐活性。
毒理研究
大鼠連續6個月經口給予阿瑞匹坦的重複給藥毒性試驗中,給藥劑量達最大可行劑量1000mg/kg、每日兩次(雌鼠和雄鼠的全身暴露水平分別近似或低於成人劑量的全身暴露水平),可導致肝臟重量增加伴隨肝細胞肥大、甲狀腺重量增加伴隨甲狀腺濾泡細胞肥大和/或增生和垂體細胞空泡形成。該結果是大鼠中肝臟CYP酶誘導產生的種屬特異性結果,這些病理變化在給予其它與阿瑞匹坦結構和藥理作用不同的肝臟CYP酶誘導物的大鼠中同樣可以觀察到。
犬連續9個月經口給予阿瑞匹坦的重複給藥毒性試驗中,在35mg/kg每日兩次的劑量下(全身暴露水平大於或等於成人劑量全身暴露水平的13倍),毒性表現為血清鹼性磷酸酶活性略微升高和白蛋白/球蛋白比值下降;在325mg/kg每日兩次的劑量下(全身暴露水平為成人劑量全身暴露水平的31倍),可觀察到體重增加幅度顯著減少、睪丸退變和前列腺萎縮;在500mg/kg每日兩次的劑量下(全身暴露水平為成人劑量全身暴露水平的70倍),可觀察到肝臟重量略微增加,但無組織學相關性。犬連續1年每日給予阿瑞匹坦32mg/kg(全身暴露水平為成人劑量全身暴露水平的6倍),未觀察到毒性。
遺傳毒性:阿瑞匹坦Ames試驗、人類淋巴母細胞(TK6)基因突變試驗、大鼠肝細胞DNA斷裂試驗、中國倉鼠卵巢細胞(CHO)細胞染色體畸變試驗和小鼠微核試驗結果均為陰性。
生殖毒性:阿瑞匹坦最大可行劑量1000mg/kg、每日兩次,對雌雄大鼠生育力或生殖行為未見影響,雄性大鼠該劑量下的暴露量低於人推薦劑量下的暴露量,雌性大鼠的暴露量相當於人的1.6倍。
妊娠大鼠和兔經口給予阿瑞匹坦,劑量分別高達1000mg/kg、每日兩次和每日25mg/kg(暴露量分別相當於人推薦劑量時暴露量的1.6倍和1.4倍),未見對胎仔的損傷;在這些劑量下,阿瑞匹坦可轉運到大鼠和兔胎盤中。在大鼠和兔中,胎仔血漿中的阿瑞匹坦濃度約為母體血漿阿瑞匹坦濃度的27%和56%。
哺乳期大鼠給予阿瑞匹坦1000mg/kg、每日兩次,乳汁中可觀察到較高濃度的阿瑞匹坦。在這個劑量下,乳汁藥物平均濃度為血漿藥物平均濃度的90%。
致癌性:在SD大鼠和CD-1小鼠中進行了為期2年的致癌性試驗。大鼠給藥劑量為0.05-1000mg/kg、每日2次,最高劑量下的暴露量約為人推薦劑量125mg/天時暴露量的0.7-1.6倍。雄性大鼠在5-1000mg/kg、每日2次劑量下甲狀腺濾泡細胞腺瘤和甲狀腺濾泡細胞癌發生率增加。雌性大鼠在5-1000mg/kg、每日2次劑量下肝細胞腺瘤、125-1000mg/kg、每日2次劑量下肝細胞癌與甲狀腺濾泡細胞腺瘤發生率增加。
小鼠給藥劑量為2.5-2000mg/kg/天,最高劑量下的暴露量約為人推薦劑量時暴露量的2.8-3.6倍。雄性小鼠在劑量為125-500mg/kg可見皮膚纖維肉瘤。
藥代動力學
吸收
阿瑞匹坦的平均絕對口服生物利用度約為60%至65%,阿瑞匹坦在大約4小時(Tmax)可達到平均峰血漿濃度(Cmax)。與標準早餐同服阿瑞匹坦膠囊,對於阿瑞匹坦的生物利用度不存在有臨床意義的影響。
在臨床劑量範圍內,阿瑞匹坦的藥代動力學為非線性。在健康年輕成人中,在餐後單次口服80mg至125mg劑量後,AUC0-¥的增加程度比劑量的增加程度大26%。
在第1天單次口服125mg阿瑞匹坦,第2天和第3天口服80mg,每日一次後,第1天和第3天的AUC0-24hr分別約為19.5μg·hr/mL和20.1μg·hr/mL。第1天和第3天的Cmax分別為1.5μg/mL和1.4mcg/mL,並在大約4小時(Tmax)內達到。
健康中國青年受試者接受阿瑞匹坦125mg單次口服劑量(第1天)或者阿瑞匹坦3天治療方案(包括第1天125mg單次口服以及第2-3天80mg單次口服),阿瑞匹坦的中位Tmax約為用藥後5小時,第1天和第3天時AUC0-24hr分別約為48μg·hr/mL和67.1μg·hr/mL。第1天和第3天時,約4小時(Tmax)達到的Cmax值,分別為3.3μg/mL和4.3μg/mL。
分布
阿瑞匹坦與血漿蛋白的結合率大於95%。在人體中,穩態表觀分布容積(Vdss)的幾何平均值約為66L。
阿瑞匹坦可穿透大鼠胎盤,並可穿透大鼠和雪貂的血腦屏障。在人體中進行的PET研究提示,阿瑞匹坦可穿透血腦屏障(參見“藥理毒理”,作用機制)。
代謝
阿瑞匹坦可進行廣泛的代謝。在健康年輕成人中,單次口服300mg[14C]-阿瑞匹坦後72小時內,阿瑞匹坦大約占血漿放射性標記物的24%,表明血漿中存在大量代謝產物。在人類血漿中發現了7種阿瑞匹坦代謝產物,它們僅有微弱的活性。阿瑞匹坦的代謝作用主要通過嗎啉環和側鏈上的氧化作用發生。使用人類肝臟微粒體的體外研究提示,阿瑞匹坦主要通過CYP3A4代謝,少數通過CYP1A2和CYP2C19代謝,而CYP2D6、CYP2C9或CYP2E1對其無代謝作用。
清除
阿瑞匹坦主要通過代謝進行清除;阿瑞匹坦無法通過腎臟排泄。在健康受試者中單次口服300mg[14C]-阿瑞匹坦後,尿液和糞便中分別回收5%和86%的放射性標記物。
阿瑞匹坦的表觀血漿清除率約為60至84mL/min。表觀終末半衰期約為9至13小時。
患者中的特徵
性別
單次口服阿瑞匹坦後,阿瑞匹坦在女性中的AUC0-24hr和Cmax比男性分別高9%和17%。阿瑞匹坦在女性中的半衰期比男性短大約25%,而在男性和女性中的Tmax相似。這些差異無臨床意義。無需根據性別對本品進行劑量調整。
老年人
老年人(365歲)在第1天單次口服125mg阿瑞匹坦,第2至5天口服80mg阿瑞匹坦每日一次後,阿瑞匹坦在第1天和第5天的AUC0-24hr分別比年輕成人升高21%和36%;第1天和第5天的Cmax分別比年輕成人高10%和24%。這些差異無臨床意義。在老年患者中,無需對本品進行劑量調整。
兒童
尚未在年齡小於18歲的患者中對本品的藥代動力學進行評估。
人種
單次口服本品後,西班牙人的AUC0-24hr大約比高加索人和黑人高27%和31%。西班牙人的Cmax比高加索人和黑人高19%和29%。單次口服本品後,亞洲人的AUC0-24hr和Cmax分別比高加索人高74%和47%。中國人的藥物暴露水平AUC0-24hr和Cmax高於非中國受試者,這些差異無重要臨床意義,進一步的藥代比價研究正在進行中。目前不推薦根據人種對本品進行劑量調整。
身體質量指數(BMI)
身體質量指數對阿瑞匹坦的藥代動力學沒有臨床顯著性影響。
肝功能不全
本品在輕度至中度肝功能不全患者中具有良好的耐受性。在輕度肝功能不全患者(Child-Pugh評分為5至6)中,第1天單次口服125mg阿瑞匹坦,第2天和第3天口服80mg每日一次後,阿瑞匹坦在第1天和第3天的AUC0-24hr分別比接受相同療法的健康受試者低11%和36%。在中度肝功能不全患者(Child-Pugh評分為7至9)中,阿瑞匹坦在第1天和第3天的AUC0-24hr分別比接受相同療法的健康受試者高10%和18%。AUC0-24hr的這些差異無臨床意義;因此,在輕度至中度肝功能不全患者中,無需對本品進行劑量調整。
尚未獲得重度肝功能不全患者(Child-Pugh評分大於9)中的臨床或藥代動力學數據。
腎功能不全
在重度腎功能不全患者(CrCl小於30mL/min)和需要接受血液透析的終末期腎病(ESRD)患者中,單次口服了240mg阿瑞匹坦。
在重度腎功能不全患者中,體內所有阿瑞匹坦(結合了蛋白的和未結合蛋白的)的AUC0-¥和Cmax與健康受試者相比分別下降21%和32%。在接受血液透析的終末期腎病患者中,體內所有阿瑞匹坦的AUC0-¥和Cmax分別下降42%和32%。由於在腎病患者中,阿瑞匹坦的蛋白結合率僅有中度下降,因此在腎功能不全患者中,具有藥理學活性的非蛋白結合藥物的AUC與健康受試者相比未受到顯著影響。在給藥後4或48小時進行的血液透析對阿瑞匹坦的藥代動力學不存在顯著的影響;只有不到0.2%的劑量在透析液中回收。
在重度腎功能不全患者或接受血液透析的終末期腎病患者中,無需對本品進行劑量調整。
指南推薦
目前,阿瑞匹坦已得到《美國國家癌症綜合網路臨床套用指南》(NCCN)、《國際癌症姑息治療學會》(MASCC)、歐洲腫瘤內科學會(ESMO)等權威指南一致推薦,作為預防腫瘤化療後引起的急性和遲發性噁心嘔吐的一線用藥/推薦用藥。
臨床數據研究
高度致吐性化療(HEC)
國內臨床研究
在中國開展的一項隨機、雙盲、安慰劑對照、平行分組、多中心、Ⅲ期臨床研究中,在接受化療(包括順鉑370mg/m2)的412例中國患者中對阿瑞匹坦治療方案與標準治療方案用於預防化療引起的嘔吐(CINV)的作用進行了比較。阿瑞匹坦治療方案包括:第1天阿瑞匹坦服用劑量為125mg,第2-3天劑量為80mg/天,與格拉司瓊(3mg靜脈輸注,第1天)和地塞米松(第1天6mg,第2-4天3.75mg)進行聯合治療。標準治療方案包括安慰劑與格拉司瓊(第1天3mg靜脈輸注)和地塞米松(第1天10.5mg,第2-4天7.5mg)進行的聯合治療。
在第1周期中,對急性期(順鉑治療後0-24小時)、延遲期(順鉑治療後25-120小時)和總觀察期(順鉑治療後0-120小時)阿瑞匹坦的止吐活性進行了評價。主要療效評價是基於總觀察期中報告為完全緩解(沒有出現嘔吐和沒有使用補救治療)的患者比例。次要療效評價是基於報告如下情況的患者比例:在急性期和延遲期中報告為完全緩解,在總觀察期、急性期和延遲期中沒有出現嘔吐,以及在總觀察期中沒有對日常生活和首次嘔吐發作的時間造成影響。探索性評價是基於報告如下情況的患者比例:在急性期、延遲期和總觀察期中報告為完全控制和總體控制,在總觀察期中未出現任何顯著噁心和未出現噁心(具體見表1)。
表1合併分析的主要研究結果的總結根據治療組和階段,接受高度致吐性化療的患者百分比—第1周期
|
|---|
| 阿瑞匹坦治療組*
%
(n/m)†
| 標準治療組**
%
(n/m)†
| P值
|
完全緩解(無嘔吐和沒有補救治療)
|
總觀察期‡
| 69.6
(142/204)
| 57.0
(118/207)
| 0.007
|
急性期§
| 79.4
(162/204)
| 79.3
(165/208)
| 0.942
|
延遲期װ
| 74.0
(151/204)
| 59.4
(123/207)
| 0.001
|
無嘔吐(患者日誌中無嘔吐或乾嘔)
|
總觀察期
| 70.6
(144/204)
| 57.0
(118/207)
| 0.003
|
急性期
| 80.4
(164/204)
| 79.8
(166/208)
| 0.882
|
延遲期
| 74.0
(151/204)
| 59.4
(123/207)
| 0.001
|
完全控制(無嘔吐,沒有補救治療,噁心最大VAS¶<25mm) |
總觀察期
| 63.2
(129/204)
| 54.6
(112/205)
| 0.074
|
急性期
| 76.0
(155/204)
| 77.7
(160/206)
| 0.698
|
延遲期
| 66.7
(136/204)
| 57.1
(117/205)
| 0.041
|
*阿瑞匹坦治療方案:在第1天口服阿瑞匹坦125mg,第2天和第3天口服阿瑞匹坦80mg,每日一次;第1天時,阿瑞匹坦與格拉司瓊3mg(靜脈輸注)和地塞米松6mg(口服)進行聯合治療;第2-4天時,阿瑞匹坦與地塞米松3.75mg(口服,每天一次)進行聯合治療。
**標準治療方案:第1天時,安慰劑與格拉司瓊3mg(靜脈輸注)和地塞米松10.5mg(口服)進行聯合治療;第2-4天時,安慰劑與地塞米松7.5mg(口服)進行聯合治療。
†接受順鉑和研究藥物以及至少有一個治療後有效性評價的患者數。
‡總觀察期:順鉑治療後0-120小時。
§急性期:順鉑治療後0-24小時。
װ延遲期:順鉑治療後25-120小時。
¶視覺模擬量表(VAS)評分範圍:0=未出現噁心;100=噁心極其嚴重。
阿瑞匹坦治療方案在總觀察期和延遲期中的完全緩解(主要終點)和未出現嘔吐(次要終點)均顯示優效性。另外,對於首次出現嘔吐時間這一次要終點,阿瑞匹坦治療方案相對於標準治療方案對患者具有更佳的治療受益。此外,對於一些探索性終點,例如總觀察期和延遲期中的完全控制、總體控制、未出現顯著噁心和未出現噁心,阿瑞匹坦治療方案的治療受益在數值上優於標準治療方案。
根據性別進行的亞組分析顯示,女性患者在總觀察期中達到完全緩解的比例(阿瑞匹坦治療方案的64.7%相對於標準治療方案的32.9%)高於男性患者(阿瑞匹坦治療方案的72.1%相對於標準治療方案的70.1%)。阿瑞匹坦治療方案的治療受益始終更佳。
全球臨床研究
在2項對照、隨機化臨床研究中,在1094名接受包含順鉑,370mg/m2的化療的患者中對阿瑞匹坦治療方案與標準治療方案預防化療引起的嘔吐(CINV)進行了比較。其中部分患者還接受了其它化療藥物,例如吉西他濱、依託泊苷、氟尿嘧啶、酒石酸長春瑞濱、多柔比星、環磷醯胺、紫杉醇或多西他賽。阿瑞匹坦療法為第1天口服阿瑞匹坦125mg,第2天和第3天每日口服80mg,第1天給予昂丹司瓊32mg靜脈輸注並口服地塞米松12mg,第2至4天口服8mg,每日一次。標準療法為安慰劑加第1天給予昂丹司瓊32mg靜脈輸注並口服地塞米松20mg,第2至4天口服8mg,每日兩次。該臨床試驗中採用了靜脈輸注昂丹司瓊32mg為對照,由於在研究中發現昂丹司瓊高劑量使用引起心臟不良事件增加(劑量依賴性QT間期延長),該劑量已不再被推薦使用,請參考所選擇的5-HT3拮抗劑的說明書以選擇合適的劑量。
在第1周期中,對阿瑞匹坦在急性期(順鉑治療後0至24小時)、延遲期(順鉑治療後25至120小時)和總觀察期(順鉑治療後0至120小時)的止吐療效進行了評估。根據以下複合參數對有效性進行評估:完全緩解(定義為未出現嘔吐發作和未使用補救治療)和完全控制(定義為未出現嘔吐發作、未使用補救治療和最大噁心視覺模擬量表[VAS]評分小於25mm)。對每項研究和2項研究合併後的結果進行評估(具體見表2)。
表2合併分析的主要研究結果總結
接受高度致吐性化療並產生緩解的患者百分比,按不同的治療組和時期—第1周期
|
|---|
| 阿瑞匹坦治療組*
(N=521)†
%
| 標準治療組**
(N=524)†
%
| p值
|
完全緩解(無嘔吐和沒有補救治療)
|
總觀察期‡
急性期§
延遲期װ
| 67.7
86.0
71.5
| 47.8
73.2
51.2
| <0.001
<0.001
<0.001
|
完全控制(無嘔吐、沒有補救治療,噁心最大VAS¶<25mm)
|
總觀察期
急性期
延遲期
| 59.5
82.4
63.7
| 44.9
69.6
47.8
| <0.001
<0.001
<0.001
|
*阿瑞匹坦治療方案:在第1天口服阿瑞匹坦125mg,第2天和第3天口服阿瑞匹坦80mg每日一次,第1天給予昂丹司瓊32mg靜脈輸注並口服地塞米松12mg,第2至4天口服8mg,每日一次。
**標準治療方案:在第1天給予安慰劑加昂丹司瓊32mg靜脈輸注,並口服地塞米松20mg,第2至4天口服8mg,每日兩次。
†N:接受順鉑、研究藥物和至少1次治療後有效性評估的患者人數。
‡總觀察期:順鉑治療後0至120小時。
§急性期:順鉑治療後0至24小時。
װ延遲期:順鉑治療後25至120小時。
¶視覺模擬量表(VAS)評分範圍:0=未出現噁心;100=噁心極其嚴重。
在合併分析中,接受阿瑞匹坦治療的患者在第1周期獲得完全緩解和完全控制的比例顯著高於接受標準治療的患者。在接受阿瑞匹坦治療和標準治療的患者中,第1周期的急性期和延遲期觀察到的完全緩解和完全控制的比例有顯著的統計學差異。對這兩個研究分開分析,也可觀察到上述結果。
使用功能生活指數-嘔吐(FLIE)評估噁心和嘔吐對患者日常生活的影響,這是經過驗證的患者報告的結局參數。在混合分析中,根據FLIE總評分,接受阿瑞匹坦治療的患者中,噁心和嘔吐對日常生活未產生影響的比例顯著(p<0.001)高於接受標準療法的患者。同上,也可觀察到這些結果。
多周期擴展期:在相同的2項臨床研究中,共有851名患者繼續參加最多6個化療周期的多周期擴展期。在所有周期中,阿瑞匹坦療法的有效性得以維持。
中度致吐性化療(MEC)
在一項隨機、雙盲臨床研究中,共有866名患者接受了包含環磷醯胺,750-1500mg/m2;或環磷醯胺500-1500mg/m2和多柔比星(60mg/m2)或表柔比星(100mg/m2)的化療,研究比較了阿瑞匹坦加昂丹司瓊/地塞米松療法與標準療法(安慰劑加昂丹司瓊8mg口服(第1天2次,第2天和第3天每隔12小時)加地塞米松20mg口服,第1天)。
在第1周期,對阿瑞匹坦在急性期(化療後0至24小時)、延遲期(化療後25至120小時)和總觀察期(化療後0至120小時)的止吐活性進行了評估。根據以下複合參數對有效性進行評估:完全緩解(定義為未出現嘔吐發作和未使用補救治療)和噁心和嘔吐對日常生活的影響(見表3)。
表3關鍵的研究結果總結
接受中度致吐性化療並產生緩解的患者百分比,按不同的治療組和時期—第1周期
|
|---|
複合參數
| 阿瑞匹坦治療組*
(N=433)†
%
| 標準治療組**
(N=424)†
%
| p值
|
完全緩解(無嘔吐和沒有補救治療)
|
總觀察期‡
急性期§
延遲期||
| 51
76
55
| 42
69
49
| 0.015
0.034
0.064
|
未對日常生活產生影響(功能生活指數-嘔吐[FLIE]總評分大於108)
|
總觀察期
| 64
| 56
| 0.019
|
*阿瑞匹坦治療方案:在第1天口服阿瑞匹坦125mg,在第2天和第3天口服80mg,第1天2次口服昂丹司瓊8mg,第1天口服地塞米松12mg。
**標準治療方案:安慰劑加昂丹司瓊8mg,口服(第1天2次,第2天和第3天每隔12小時),第1天口服地塞米松20mg。
†N:入選完全緩解的主要分析的患者人數。
‡總觀察期:化療後0至120小時。
§急性期:化療後0至24小時。
||延遲期:化療後25至120小時。
在這項研究中,在接受阿瑞匹坦治療的患者(51%)中,第1周期內出現總觀察期內完全緩解(主要終點)的比例顯著(p=0.015)高於接受標準治療的患者(42%)。未經調整的完全緩解的絕對差異(8.3%)提示了20%的相對改善率(相對風險比=1.2,阿瑞匹坦療法/標準療法)。此外,在接受阿瑞匹坦治療的患者中,第1周期出現急性期和延遲期內完全緩解的比例高於接受標準治療的患者。
在這項研究中,根據FLIE總評分大於108,在接受阿瑞匹坦治療的患者中,第1周期內噁心和嘔吐未對日常生活產生影響的比例顯著高於接受標準治療的患者,有統計學差異。
多周期擴展期:共有744名患者繼續參加最多4個化療周期的多周期擴展期。在所有周期內,阿瑞匹坦療法的有效性得以維持。
在第2項多中心、隨機、雙盲、平行分組的臨床研究中,在848名接受包含任何靜脈輸注的奧沙利鉑、卡鉑、表柔比星、伊達比星、異環磷醯胺、伊立替康、柔紅黴素、多柔比星;環磷醯胺,靜脈輸注(小於1500mg/m2);或阿糖胞苷,靜脈輸注(大於1g/m2)的化療方案的患者中對阿瑞匹坦療法與標準療法進行了比較。隨機接受阿瑞匹坦療法的患者包括76%的女性和24%的男性。接受阿瑞匹坦療法的患者因各種腫瘤類型接受了化療,包括52%的乳腺癌患者、21%的胃腸道癌(包括結腸直腸癌患者)、13%的肺癌患者和6%的婦科癌症患者。阿瑞匹坦療法為第1天口服EMEND125mg,第2天和第3天每日口服80mg,第1天2次口服昂丹司瓊8mg,第1天口服地塞米松12mg。標準療法為安慰劑加昂丹司瓊8mg口服(第1天2次,第2天和第3天每隔12小時),第1天口服地塞米松20mg。
在第1周期,對阿瑞匹坦在急性期(開始化療輸注後0至24小時)、延遲期(開始化療輸注後25至120小時)和總觀察期(開始化療輸注後0至120小時)的止吐活性進行了評估。根據以下主要終點和關鍵的次要終點對有效性進行評估:在總觀察期(化療後0至120小時)內未出現嘔吐、阿瑞匹坦療法預防化療引起的嘔吐(CINV)的安全性和耐受性評估,以及在總觀察期(化療後0至120小時)內的完全緩解(定義為未出現嘔吐和未使用救援治療)。
表4研究2關鍵的研究結果總結
在研究2中,接受中度致吐性化療並產生緩解的患者百分比,按不同的治療組和時期–第1周期
終點
| 阿瑞匹坦治療組*
(N=430)†
%
| 標準治療組**
(N=418)†
%
| p值‡
|
主要終點
|
未出現嘔吐
|
總觀察期§
| 76
| 62
| <0.0001
|
關鍵的次要終點
|
完全緩解¶
|
總觀察期
| 69
| 56
| 0.0003
|
*阿瑞匹坦治療方案:在第1天口服阿瑞匹坦125mg,第2天和第3天口服80mg,第1天2次口服昂丹司瓊8mg加第1天口服地塞米松12mg。
**標準治療方案:安慰劑加昂丹司瓊8mg口服(第1天2次,第2天和第3天每隔12小時),第1天口服地塞米松20mg。
†N:接受化療、研究藥物和至少1次治療後有效性評估的患者人數。
‡在檢驗次要終點的顯著意義時,使用Hochberg程式進行多因素調整。
§總觀察期:化療後0至120小時。
¶完全緩解:未出現嘔吐和未接受救援治療。
在這項研究中,接受阿瑞匹坦療法的患者在第1周期的總觀察期未出現嘔吐(主要終點)的比例(76%)顯著(p<0.0001)高於接受標準療法的患者(62%)。此外,接受阿瑞匹坦療法的患者在第1周期的總觀察期(0-120小時)出現完全緩解的比例高於接受標準療法的患者。無論年齡、性別或腫瘤類型(乳腺、胃腸道、肺或其它)如何,根據未出現嘔吐和完全緩解終點評估,阿瑞匹坦均優於標準療法。