基本介紹
- 中文名:尖晶石型鐵氧體
- 外文名:spinel type ferrites
- 別稱:磁性尖晶石
- 化學式:MeFe2O4
- 晶體類型:面心立方晶體
- 套用:新材料研發
簡介
晶體結構
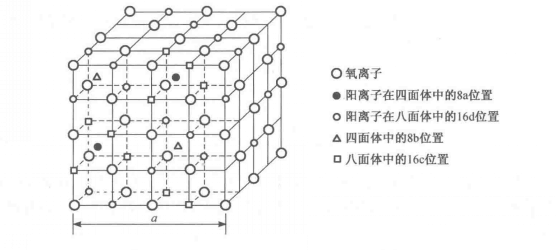 陽離子在尖晶石點陣中的分布
陽離子在尖晶石點陣中的分布 陽離子在尖晶石點陣中的分布
陽離子在尖晶石點陣中的分布尖晶石型鐵氧體(spinel type ferrites) 晶體結構與天然礦物尖晶石MgAl2O4相同的鐵氧體。又稱磁性尖晶石。分子式為MFe2O4,式中M為二價金屬離子,常見的有Mn...
旋磁鐵氧體已廣泛套用於微波通信領域。按照晶體類型分,旋磁鐵氧體可分為尖晶石型、石榴石型和磁鉛石型(六角型)鐵氧體。鐵氧體歷史沿革 編輯 ...
氧化法是將亞鐵離子和其他可溶性重金屬離子溶液混合,在一定條件下用空氣(或其他方法)部分氧化Fe,從而形成尖晶石型鐵氧體。例如用鐵氧體法處理含鉻廢水時,就是採用...
一般密度高、晶粒均勻、結晶各向異性較大的尖晶石型鐵氧體都可製成磁特性較好的矩磁材料。[1] 矩磁鐵氧體套用 矩磁鐵氧體具有矩形磁滯回線,並且矯頑力較大。...
一般軟磁鐵氧體的晶體結構都是立方晶系尖晶石型,套用於音頻至甚高頻頻段(1千赫-300兆赫)。但是具有六角晶系磁鉛石型晶體結構的軟磁材料卻比尖晶石型的套用頻率...
鐵氧體材料按其晶體結構劃分,大致可以分為立方晶系尖晶石型、石榴石型和六角晶系磁鉛石型三個主要系列。它們的晶體結構各不相同,性能差別也較大。它們的靜磁性和...
微波鐵氧體材料分為多晶和單晶兩種。多晶材料按晶體結構分,主要有尖晶石型、石榴石型和磁鉛石型三種。微波鐵氧體器件的種類很多,按功能有隔離器、環行器、開關、...
中和法就是將三價鐵離子和組成鐵氧體材料的其它金屬鹽溶液, 用鹼中和, 在一定條件下, 直接在水溶液中形成尖晶石型鐵氧體。其離子反應方程式為:2Fe3++ M 2+...
軟磁鐵氧體的一種。屬尖晶石型結構。由鐵、錳、鋅的氧化物及其鹽類,採用陶瓷工藝製成。它具有高的起始導磁率。一般在1千赫至10兆赫的頻率範圍內使用。可製作...
1.2.1尖晶石型鐵氧體的晶體結構0031.2.2納米晶鐵氧體的製備方法0061.3鐵氧體-聚合物複合材料0091.3.1鐵氧體-聚苯胺複合材料的研究現狀009...
2.7軟磁鐵氧體的微觀結構與性能的關係29第3章 軟磁鐵氧體的基本特性3.1鐵氧體的磁性來源及亞鐵磁性313.2磁疇和磁疇壁333.3尖晶石型鐵氧體的磁性34...
旋磁鐵氧體又稱旋磁鐵氧體,一種可在微波波段(包括從米波至毫米波)使用的鐵...單晶型的現不常用。多晶型的,按結構分,主要有:(1)尖晶石型,如MgFe2O4系...
鋇鐵氧體是一種磁性材料,用於磁粉,方性磁鋼、磁性膠片、玩具。...... 它的晶體結構和尖晶石型鐵氧體不一樣,因為它含有鋇(Ba)、鉛(Pb)等離子,其半徑與氧離子...
鎳鋅鐵氧體概述 編輯 ferrite分子式:Ni-Zn性質:高頻軟磁鐵氧體,具有尖晶石...普通電感、可調電感、耐電流電感均屬於傳統型鎳鋅鐵氧體電感系列,生產和市場比較...
利用鐵氧體材料(見磁性材料)的旋磁效應製成的微波器件。...... 微波鐵氧體材料有許多品種,根據材料的成分和晶體結構分類,有石榴石型、尖晶石型和磁鋁石型(六角...
鎳鋅矩磁鐵氧體Ni-Ga rectar}ular lcxy (erril。具有矩形磁滯回線、尖晶石型結構的鐵氧體。化學式為NiO.2nQ)Fe2}3v矯頑力238 . U- 557 . 2AIm o在...
鎂錳旋磁鐵氧體 又稱鎂錳微波鐵氧體。鎂、錳、鐵的氧化 物為主要成分的一種旋磁鐵氧體。具有尖晶石型結構。其組 成(mol })為:IVIg}42 }- 5#},'....
(111)面內近鄰的磁矩方向相反20世紀50年代曾對許多反鐵磁體如FeONiOCoO[kg1]-FeO等進行了中子衍射研究,對尖晶石型鐵氧體如FeOMnFeO及石榴石型鐵氧體如YFeO[...
4. 尖晶石型鐵氧體的模板合成與催化性能研究,山西省教育廳科技研究開發項目,3萬,2009年7月楊巧珍論著一覽 王晶,楊巧珍,董平,張俊玲,海綿狀NiFe2O4團簇的合成與...
2. 胡源,周克清,桂宙.尖晶石型磁性鐵氧體/二硫化鉬納米複合材料及其製備方法,中國,專利號:ZL201310376218.2.3. 胡源,周克清,桂宙.金屬雙氫氧化物/二硫化鉬納米...
④鐵氧體:包括尖晶石型──MO· (M 代表NiZn、MnZn、MgZn、CaZn等),磁鉛石型──Ba3Me2Fe24O41(Me代表Co、Ni、Mg、Zn、Cu及其複合組分)。軟磁材料的...
