代文(纈沙坦膠囊),適應症為治療輕、中度原發性高血壓。
基本介紹
- 藥品名稱:代文?
- 藥品類型:處方藥、基本藥物、醫保工傷用藥
- 用途分類:血管緊張素Ⅱ受體拮抗藥
成份
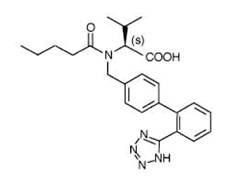
化學名稱:(S)-N-戊醯基-N-{[2'-(1H-5-四唑基)-4-二苯基]甲基}-纈氨酸。
化學結構式:
分子式:C24H29N5O3
分子量:435.5
性狀
適應症
規格
用法用量
用藥2周內達確切降壓效果,4周后達最大療效。降壓效果不滿意時,每日劑量可增加至160mg,或加用利尿劑。
腎功能不全(嚴重腎衰見【注意事項】)及非膽管源性、無淤膽的肝功能不全患者無需調整劑量。
纈沙坦可以與其他抗高血壓藥物聯合套用。
不良反應
在一項使用320mg纈沙坦治療的642名高血壓患者中進行的為期6個月的開放擴展試驗,不良事件的總發生率同安慰劑對照試驗中觀察到的相似。
10個安慰劑對照試驗報告的不良事件發生情況,患者服用纈沙坦10-320mg/日,直至12周。2316名患者中1281人,660人分別服用80mg、160mg,不良事件的發生率與用藥劑量及用藥時間無關,因此,將各種劑量下發生的不良事件合併統計。不良事件的發生率與性別、年齡、種族無關。
根據系統器官分類,臨床研究、上市後使用經驗和實驗室檢查的不良反應列於下表。
不良反應按發生率由高到低分為如下幾類:非常常見(≥1/10);常見(≥1/100,[1/10);不常見(≥1/1000,[1/100);罕見(≥1/10000,[1/1000);非常罕見([1/10000)。從每個組中,不良反應按嚴重性由高到低排列。
對於上市後使用經驗和實驗室檢查的所有不良反應報告.不適於按照發生頻率進行分組.因此其發生率記為“未知”。
高血壓患者的臨床試驗中還觀察到以下不良事件(無論是否與研究藥物有關):關節痛、無力、背瘸、腹瀉、頭暈、頭痛、失眠、性慾降低、噁心、水腫、咽炎、鼻炎、竇炎、上呼吸道感染、病毒感染。

禁忌
妊娠(見【孕婦和哺乳期婦女】)。
注意事項
極少數情況下,嚴重缺鈉和/或血容量不足患者(如:大劑量套用利尿劑),套用本品治療開始時,可能出現症狀性低血壓。應該在用藥之前,糾正低鈉和/或血容量不足,例如將利尿劑減量。如果發生低血壓,應該讓患者平臥,必要時靜脈輸注生理鹽水。血壓穩定後可以繼續本品治療。
腎動脈狹窄
12例因單側腎動脈狹窄導致的繼發性腎血管性高血壓患者短期服用本品,沒有引起腎血流動力學、肌酐、尿素氮(BUN)明顯變化。由於其他作用於腎素-血管緊張素-醛固醇系統(RAAS)的藥物可能使單側或雙側腎動脈狹窄患者的BUN和肌酐升高,建議作為安全手段監測BUN和肌酐。
腎功能不全
腎功能不全患者需要調整劑量,但由於沒有嚴重病例的資料(肌酐清除率[10ml/min),因此使用時需要注意。
肝功能不全
肝功能不全患者不需要調整劑量。
纈沙坦主要以原型從膽汁排泄,膽道梗阻患者排泄減少(見【藥代動力學】),對這類患者使用纈沙坦應特別小心。
對駕駛和操作機器的影響
與其它抗高血壓藥一樣,服藥患者在駕駛、操作機器時應小心。
孕婦及哺乳期婦女用藥
鑒於血管緊張素Ⅱ拮抗劑的作用機制,不能排除對胎兒的危害。已經有報告表明:在妊娠第2個和第3個3個月時,子宮內給予血管緊張素轉化酶抑制劑(作用於RAAS的一種特定類別的藥物)會給發育中的胎兒帶來損傷,或者導致胎兒死亡。此外,在回顧性資料中有在妊娠第1個3個月時使用血管緊張素轉化酶抑制劑存在先天缺陷的潛在性風險。已有孕婦無意中服用纈沙坦時,發生自然流產、羊水過少和新生兒腎功能不全的報告。與其它直接作用於RAAS的藥物相似,妊娠期婦女不應使用本品(見禁忌)。對於有懷孕可能的婦女,醫生在處方作用於RAAS的藥物時應告知其該類藥物在妊娠期的潛在風險。如果用藥期間發現妊娠,應儘早停用纈沙坦。
哺乳
尚不清楚纈沙坦是否在人乳中排泄。纈沙坦在哺乳大鼠的乳汁中有排泄。因此本品不宜用於哺乳期。
兒童用藥
老年用藥
藥物相互作用
由於纈沙坦幾乎不經過代謝,臨床沒有發現誘導或抑制細胞色素P450系統的藥物發生相互影響。
雖然纈沙坦大部分與血漿蛋白結合,但是體外實驗沒有發現它在這一水平與其他血漿蛋白結合藥物(如雙氯芬酸、呋塞米、華法令)發生相互作用。
鉀:與保鉀利尿劑(如螺內脂、氨苯喋啶、阿米洛利)聯合套用時,補鉀或使用含鉀製劑可導致血鉀濃度升高和引起心力衰竭患者血清肌酐升高。因此,聯合用藥時需要注意。
非甾體類抗炎藥(NSAIDs)包括選擇性環氧化酶2抑制劑(COX-2);同時服用血管緊張素II受體拮抗劑和非甾體類抗炎藥,會降低抗高血壓作用。此外,對於老年患者、血容量減少患者(包括接受利尿劑治療者)、或有腎功能損害者,同時使用血管緊張素II受體拮抗劑和非甾體類抗炎藥,可能會使腎功能惡化的風險升高。因此,對於正在使用非甾體類抗炎藥的患者,如要開始或調整纈沙坦的治療,建議監測腎功能。
藥物過量
若服藥時間不長,應該催吐治療,否則常規治療給予生理鹽水靜脈輸注。血液透析不能清除纈沙坦。
藥理毒理
腎素一血管緊張素一醛固酮系統(RAAS)的激活劑是血管緊張II,是由血管緊張I在血管緊張素轉化酶(ACE)作用下形成的。血管緊張素II與種組織細胞膜上的特異受體結合。它有很多生理作用,包括直接或間接參與血壓調節。血管緊張素II是一種強的縮血管物質,具有直接的升壓效應,同時還可促進鈉的重吸收,刺激醛固酮分泌。
纈沙坦是一種口服有活性的強力特異性血管緊張素(Ang II)II受體拮抗劑,它選擇性地作用於AT1受體亞型,血管緊張素II的已知作用就是由AT1受體亞型引起的。在使用本品之後,AT1受體封閉,血管緊張素II血漿水平升高,它會刺激未封閉的AT2受體,同時抗衡AT1受體作用。纈沙坦對AT1受體沒有任何部分激動劑的活性。纈沙坦與AT1受體的親和力比AT2受體強20000倍。
ACE將血管緊張素I轉化為血管緊張素II,並降解緩激肽。血管緊張素II受體拮抗劑一纈沙坦對ACE沒有抑制作用,不引起緩激肽和P物質的瀦留,所以不會引起咳嗽。比較纈沙坦與ACE抑制劑的臨床試驗證實纈沙坦組乾咳的發生率(2.6%)顯著低於ACE抑制劑組(7.9%)(P<0.05)。在一項對曾接受ACE抑制劑治療後發生乾咳症狀的患者進行的臨床試驗發現,纈沙坦組、利尿劑組、ACEI組分別有19.5%、19.0%、68.5%患者出現咳嗽(P<0.05)。纈沙坦對其他已知的在心血管調節中起重要作用的激素受體或離子通道無影響。
藥效
纈沙坦降低升高的血壓,同時不影響心率。
對大多數患者,單劑口服2小時內產生降壓效果,4-6小時達作用高峰,降壓效果維持至服藥後24小時以上。重複給藥時,治療2-4周后達最大降壓療效,並在長期治療期間保持療效。與噻嗪類利尿劑合用可進一步增強降壓效果。
突然終止纈沙坦治療,不引起高血壓“反跳”或其他不良反應。
在對高血壓患者進行的多劑量研究中,纈沙坦對總膽固醇、空腹甘油三酯、空腹血糖和尿酸水平沒有明顯影響。
臨床前安全信息
在對幾種動物進行的臨床前安全性研究中,除了發現兔中的胎兒毒性之外,沒有全身或者靶器官毒性的表現。在大鼠妊娠最後三個月和哺乳期間給予600mg/kg藥物,其後代的生存率略微降低,發育略微遲緩(見孕婦和哺乳期婦女用藥)。主要臨床前安全性研究結果是由於藥物的藥理作用引起,沒有任何臨床意義。
在小鼠和大鼠中,沒有致突變性,染色體誘裂性或者致癌性的證據。
藥代動力學
在研究的劑量範圍內,藥代動力學曲線呈線性。重複給藥時,纈沙坦的藥代動力學沒有變化;每天服用一次時,纈沙坦很少引起蓄積,在男性和女性中,血漿濃度相似。
纈沙坦絕大部分(94-97%)與血清蛋白(主要是白蛋白)結合。穩態分布容積較低(約為17升),與肝血流量(30升/小時)相比,血漿清除速度相對較慢(大約2升/小時)。纈沙坦主要以原型排泄,70%從糞便排出,30%從尿排出。
進餐時服用纈沙坦,使AUC減少48%,但是無論是否進餐時服用,8小時後的血藥濃度相似。AUC或Cmax減少對臨床療效無明顯影響,本品可以進餐時或空腹服用。
特殊臨床情況下的藥代動力學
老年人
與青年志願者相比,一些老年人(>65歲)纈沙坦系統暴露量稍增高,但無臨床意義。
腎功能不全患者
由於纈沙坦僅有30%從腎排泄,腎功能與纈沙坦組織濃度間無明確相關性。因此,腎功能不全患者不必調整劑量(對嚴重腎衰、見注意事項)。尚未見關於透析患者的研究,但鑒於纈沙坦與血清蛋白高度結合,不大可能經透析清除。
肝功能不全患者
大約70%的纈沙坦以原型經膽汁排泄,纈沙坦不經生物轉化,因此,纈沙坦系統暴露量與肝功能不全無關。對非膽管源性、無淤膽的肝功能不全患者,不必調整劑量。膽汁性肝硬變或膽道梗阻患者,纈沙坦的AUC增加約1倍(見【注意事項】)。
貯藏
包裝
有效期
執行標準
批准文號
160mg:國藥準字H20040216
