興起
手性藥物
手性是自然界最重要的屬性之一,也是生命物質區別於非生命物質的重要標誌。自然界中構成生命體的基礎物質核苷酸、胺基酸和單糖以及由它們構成的生物大分子核酸、蛋白質和糖類都具有獨特的手性特徵。許多物理、化學 、生物功能的產生都起源於分子手征性的精確識別和嚴格匹配,例如酶催化的高度化學、區域和立體選擇性作用,手性藥物的手性對其生物應答關係等。
手性直接關係到藥物的藥理作用、臨床效果、毒副作用 、藥效發揮及藥效時間等。正是由於藥物和其受體之間的這種立體選擇性作用,使得藥物的一對對映體不論是在作用性質還是作用強度上都會有差別。在 20 世紀 60 年代,歐洲曾以消旋體的反應停(Thalidomide)作為抗妊娠反應的鎮靜劑,一些妊娠婦女服用此藥後,出現多例畸變胎兒。後經研究證實(R)-構型才真正起鎮靜作用,而(S)-構型則有強致畸作用。在農業化學品中,手性問題同樣重要,如芳氧基丙酸類除草劑 fluazifop-buty,只有(R)-異構體是有效的。
大量的事實和慘痛的教訓使人們認識到,對於手性藥物,必須對它們的立體異構體進行分別考察,了解它們各自的生理活性和各自的毒性等。美國FDA 1992 年提出的法規就要求申報手性藥物時,應該對它的不同異構體的作用敘述清楚。在藥物中,手性化合物的重要性主要在於以下幾點:
(1)不同立體異構體展現不同的生理活性,有的無效異構體可能是極其有害的;
(2)新醫藥 、新農藥,如各種抑制劑 、阻斷劑 、拮抗劑等對手性的要求越來越嚴格;
(3)環境保護問題得到普遍重視,減少不必要異構體生產就意味著減少對環境的污染,同時也能降低生產成本 。
近年來,手性藥物的套用越來越廣泛,按 1998年的統計,全球最暢銷的 500 種藥物中,單一對映異構體藥物占一半以上,占其總銷售額的 52%。1995 年全球手性藥物的年銷售總額為 614 億美元,1997 年達到 900 億美元,到 2000 年已達到 1230 億美元 。在這樣規模的市場推動下,世界各大製藥公司紛紛把注意力轉向單一對映異構體藥物的開發,同時一大批中小公司也加入其中,形成手性技術的開發熱潮。
手性技術發展
自 19 世紀 Fischer 開創不對稱合成反應研究領域以來,不對稱反應技術得到了迅速的發展。其間可分為四個階段:
(1)手性源的不對稱反應(chiralpool);
(2)手性助劑的不對稱反應 (chiral auxil-iary);
(3)手性試劑的不對稱反應(chiral reagent);
(4)不對稱催化反應 (chiral catalysis 或 asymmetriccatalytic reaction)。
傳統的不對稱合成是在對稱的起始反應物中引入不對稱因素或與非對稱試劑反應,這需要消耗化學計量的手性輔助試劑。不對稱催化合成一般指利用合理設計的手性金屬配合物或生物酶作為手性模板控制反應物的對映面,將大量前手性底物選擇性地轉化成特定構型的產物,實現手性放大和手性增殖。簡單地說,就是通過使用催化劑量級的手性原始物質來立體選擇性地生產大量手性特徵的產物。它的反應條件溫和,立體選擇性好,(R)-異構體或(S)-異構體同樣易於生產,且潛手性底物來源廣泛,對於生產大量手性化合物來講是最經濟和最實用的技術。因此,不對稱催化反應已為全世界有機化學家所高度重視,特別是不少化學公司致力於將不對稱催化反應發展為手性技術和不對稱合成工藝。2001 年諾貝爾化學獎就授予在不對稱催化氫化、和不對稱催化氧化方面做出突出貢獻的 Knowles K W、野依良治和 Sharp-less K B 三位化學家 。
工業套用
化學不對稱催化合成反應的研究開始於20 世紀60年代。1966 年,野依良治設計了以希夫鹼與銅合成的絡合物催化劑,進行均相不對稱催化環丙烷化反應,開創了首例均相不對稱催化反應的先河。1968年,化學家 Knowles 和 Horner 幾乎同時將手性膦配體引入 Wilkinson 催化劑,成功地實現了不對稱催化氫化反應,1980 年,Sharpless 首次報導了用手性鈦酸酯及過氧叔丁醇對烯丙基醇進行不對稱環氧化。近三十年來,化學不對稱催化合成得到快速發展 。
不對稱催化氫化反應
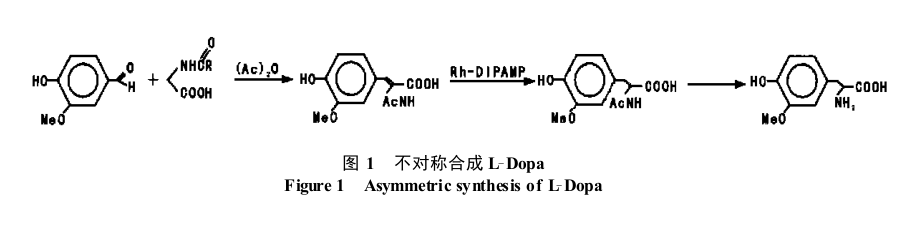
不對稱催化氫化反應是在手性催化劑作用下,氫分子將含有碳碳、碳氮、碳氧雙鍵的烯烴、亞胺和酮類等前手性底物加成轉化為手性中心含氫的產物的反應。Knowles 等製得手性膦-銠催化劑用於不對稱氫化反應,這是世界上第一個在工業上使用的不對稱催化反應。
例:L-多巴的合成。20 世紀 70 年代中期 , 孟山都公司成功運用 Knowles 的不對稱催化氫化技術工業合成了治療神經系統帕金森病的藥物———左旋多巴,其合成路線見圖。
不對稱催化氧化反應
雙鍵不對稱催化氧化在手性藥物生產中具有重要地位,它包括不對稱環氧化和不對稱雙羥基化。
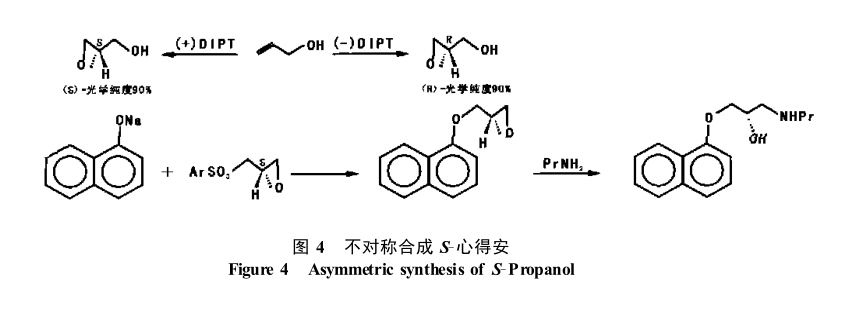
例:心得安的合成。1989 年 ,Sharpless K B 通過不對稱催化環氧化反應使烯丙醇環氧化,生產手性縮水甘油,年產量約為 10 t 。後者可轉化為治療心臟病和高血壓的 β-腎上腺素能受體阻滯劑心得安,而(R)-對映體則具有避孕效果,Arco 開發了工業生產工藝,見圖。
不對稱催化環丙烷化反應
光學活性的環丙烷類化合物具有重要的生物活性。工業上主要利用不對稱環丙烷化反應合成除蟲菊酯或生產擬除蟲菊酯類農藥,如 20 世紀 90 年代日本住友公司開發了二肽抑制劑 Ciclastatin,它是一種重要的新型農藥,具有對害蟲殺滅作用快、對人類和哺乳動物低毒的優點。
不對稱催化羰基還原反應
Corey 小組用噁唑硼烷作催化劑製備手性 α-羥基酸和手性 α-胺基酸等重要原料。Merck 公司則利用手性硼烷對酮進行不對稱還原,製得手性醇,然後進一步反應得到水溶性的碳酸酐酶阻滯劑 MK-0417,它可降低眼球內壓力,用於治療青光眼疾病。
不對稱催化羰基合成反應
羰基合成是一類重要的有機合成反應,可合成醛、醇 、酸類手性化合物,這些手性分子均為合成手性藥物和農藥的中間體,如 20 世紀 90 年代 Boots等公司利用手性催化劑[ Pd(TPTS)3]開發出一種消炎鎮痛解熱新藥布洛芬。
不對稱雙鍵轉移反應合成 L-薄荷醇
薄荷醇有三個手性碳,具有特徵香味和局部麻醉作用,多以天然產物為原料製備。日本高砂香料公司採用化學合成法,其中烯丙基胺在 Rh-BINAP催化劑上發生不對稱雙鍵轉移異構化生成手性烯胺是關鍵的一步。每年生產 9 t L-薄荷醇。其中間體香茅醛光學純度最高可達 99%,而天然香茅醛很少超過 80%。高砂香料公司還運用手性催化技術生產其他萜類香精香料如香茅醇和鈴蘭香料等,年總產量約 1500 t。
生物催化套用
生物催化的不對稱合成是以微生物和酶作為催化劑、立體選擇性控制合成手性化合物的方法,具有高區域和立體選擇性、反應條件溫和、環境友好的特點。有機合成和精細化工行業越來越多地利用生物催化轉化天然或非天然的底物,獲得有用的中間體或產物。然而,有些生物催化劑價格較高,並且對底物的適用有一定的局限性。目前,工業上一般採用化學-酶合成法,在某些合成的關鍵性步驟,採用純酶或微生物催化合成反應,而一般的合成步驟則採用化學合成法,以實現優勢互補。目前常用生物催化的有機合成反應主要有水解反應、酯化反應、還原反應和氧化反應等。
新進展
不對稱催化反應開始於 20 世紀 60 年代後期,而在 90 年代得到迅速發展,無論是在基礎研究還是在開發套用上都取得了很大的戰功。為了獲得高對映選擇性、高反應活性的催化劑,人們不斷開發出新的手性配體,並提出許多新概念,如 Corey E J 的化學酶、Soai K 的不對稱自催化、Kagan 的 雙不對稱誘導、Yamamoto H 的 BLA與 LBA、Shibasaki M 的雙金屬多功能催化劑、Sharpless K B 的手性配體促進等,以指導手性催化劑的設計。
一般說來,為了獲得高光學純度的產物,通常採用光學純的催化劑。最近 Brown J M 和 Faller J W 等提出了“不對稱去活化”的方法,即採用手性分子作為去活化劑,使外消旋催化劑中的一種對映體被選擇性地中毒而失去活性,另一種對映體則催化反應生成非外消旋產物。 而Mikami K 則提出了一種在概念上完全相反的策略,即“不對稱活化”。不對稱活化是指一種手性甚至外消旋催化劑可以被另一種手性活化試劑通過分子識別對映選擇性地活化,從而反應生成光學活性產物。例如野依良治以外消旋的TolBINAP-RuCl2 作為催化劑,手性二胺(S , S )-DPEN 作為活化劑,催化潛手性酮的不對稱還原反應,產物的對映體含量可達 95 %,收率 100%,這樣無需使用價格昂貴的光學純手性催化劑,也取得了非常好的 結果。 此外,1995 年,Burk 用 Rh-Duphos 在超臨界 CO2(SCF)中對脫氫胺基酸成功地進行了催化氫化。超臨界CO2 對環境無污染,後處理容易,對底物及 H2 溶解度大,更重要的是通過壓力的微小變化可以改變溶劑的所有性質,因而可以更好地適應反應的要求,是近幾年來剛興起的一種新的套用技術。
以前,生物催化總是被視為在醫藥工業具有潛在的套用價值。現在,生物催化不僅僅成為實驗室進行不對稱合戰的有力手段,而且許多商品的生產已經利用了生物催化過程 。展望 21 世紀的發展前景,以手性金屬有機絡合物為催化劑和以微生物及酶為催化劑的不對稱催化技術必將比翼齊飛,充分發展,為人類作出更大貢獻。