負碳離子是指帶有負電荷的含碳離子。一類重要的活性中間體。
基本介紹
- 中文名:負碳離子
- 外文名:carbanion
- 主要反應:正性分子或基團的結合
- 實質:廣義的路易斯酸-鹼反應
- 舉例:親核加成反應
定義,性質,舉例,
定義
負碳離子具有一對孤對電子 ,占有sp3雜化軌道。在許多有機反應中,C-H鍵在鹼的作用下發生異裂,質子轉移到鹼上,形成負碳離子如圖1所示: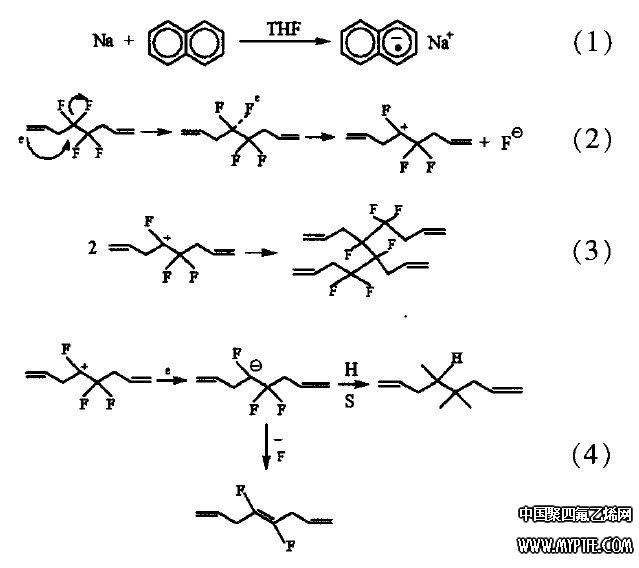 圖1
圖1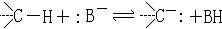 圖1
圖1
 圖1
圖1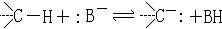 圖1
圖1性質
負碳離子極其活潑,除很少數情況外,至今尚未分離成功。然而大量實驗事實已證明了它的存在。
舉例
典型的反應有:親核加成反應、親電取代反應、芳香族親核取代反應、重排反應和消除反應等。其中麥可加成反應套用範圍最廣泛,它一般是通過負碳離子中間體歷程來進行的。典型的麥可加成反應就是α,β-不飽和羰基化合物與HY在強鹼作用下發生的1,4或1,2加成反應。HY是指相鄰具有羰基、硝基、氰基等負性基團的負碳離子的共軛酸,如丙二酸二乙酯HCH(COOC2H5)2型化合物。反應一般分二步進行(圖2): 圖2
圖2
 圖2
圖2第一步是在強鹼作用下親核試劑 Y-加成在碳-碳雙鍵上,形成A結構。同時,A結構中的負電荷進一步移到羰基的氧原子上,形成B結構。第二步是A或B與HY反應,由A得到1,2加成物,由B得到1,4加成物。一般來說,A、B結構可以互相轉移,但由於B比A結構穩定,所以主要得到1,4加成物。
負碳離子一般通過烴類(RH)與強鹼(BM)的反應,或鹵代烴(R—X)與活潑金屬(MⅠ或MⅡ)的反應來製備,如下列反應(圖3)所示: 式中MⅠ為鋰、鈉等鹼金屬;MⅡ為鎂等鹼土金屬。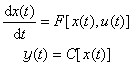 圖3
圖3
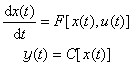 圖3
圖3