蒸氣壓滲透法(vapor pressure osmometry, VPO)是測定溶質數均分子量的一種方法。常用來測定高分子化合物的分子量。
基本介紹
- 中文名:蒸氣壓滲透法
- 外文名:vapor pressure osmometry
- 縮寫:VPO
- 目的:測定溶質數均分子量
定義,簡介,蒸氣壓滲透計,蒸氣壓,液體蒸氣壓,固體蒸氣壓,
定義
蒸氣壓滲透法(vapor pressure osmometry, VPO)是測定溶質數均分子量的一種方法。
簡介
常用來測定高分子化合物的分子量,其測定高分子分子量的範圍依賴於溫差的測定精度,一般測定上限為30000,下限則由試樣的揮發性所決定,對於不揮發物質,最低可測至40。可以證明,蒸氣壓滲透法所測定的分子量是數均分子量。
蒸氣壓滲透法的原理:在一恆溫密閉的容器中充有某揮發性溶劑的飽和蒸氣,若在此蒸氣中置一滴不揮發性溶質的溶液和一滴純溶劑,因為溶液面上溶劑的飽和蒸氣壓低於純溶劑的飽和蒸氣壓,於是溶劑分子就會自氣相凝聚在溶液滴的表面,並放出凝聚熱,從而使溶液的溫度升高。而對於純溶劑來說,其揮發速度和凝聚速度相等,溫度不發生變化,那么這兩個液滴之間便產生溫差。當溫差建立起來以後,熱量將通過傳導、對流、輻射等方式自溶液相散失到蒸氣相。達到“定態”時,測溫元件所反映出的溫差不再升高。假定溶液符合理想溶液的性質,則此時溶液滴和溶劑滴之間的溫差△T將和溶液中溶質的摩爾分數成正比。用A代表比例係數,則: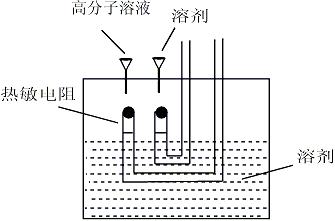 蒸氣壓滲透計原理示意圖
蒸氣壓滲透計原理示意圖
 蒸氣壓滲透計原理示意圖
蒸氣壓滲透計原理示意圖△T=A·n2/(n1+n2)≈A·n2/n1=A·w2M1/w1M2
其中,n1、n2表示溶劑和溶質的摩爾數;w1、w2代表溶劑和溶質的重量;M1、M2是溶劑和溶質(高分子)的分子量。
蒸氣壓滲透計
測定數均分子量的一種儀器。利用溶質的濃度F}溶液的蒸氣壓成比例的關係,在兩個熱敏電阻探頭土分別滴上一滴純溶劑和一滴溶液,並把它置於恆溫的溶劑蒸氣氛圍中,由於液的蒸氣壓低於純溶劑的蒸氣壓,引起溶劑分子向溶液探頭上滲透,使原先已達熱平衡的由熱敏電阻所組成的惠斯登電橋產生不平衡的甩信號,從信弓的大小可推算出溶質的分子量。
蒸氣壓
我們通常所說的蒸氣壓為液體的蒸氣壓,當氣相和液相達到平衡時,氣相蒸氣所具有的壓力稱為該溫度下的飽和蒸氣壓,簡稱蒸氣壓。無論是固體或液體,蒸氣壓大的稱為易揮發性物質,蒸氣壓小的稱為難揮發性物質。
液體蒸氣壓
定義
當液體蒸發速率與凝結速率相等時,氣相和液相達到平衡,此時,氣相蒸氣的密度不再改變,它所具有的壓力稱為該溫度下的飽和蒸氣壓,簡稱蒸氣壓,用符號p表示,單位是Pa或kPa。
形成原理
在一定溫度下,將純水注入一密閉容器中,由於分子的熱運動,一部分動能較高的分子自水面逸出,擴散到水面上部的空間,形成氣相,這一過程稱為蒸發。同時,氣相的水分子也會接觸到水面並被吸引到液相中,這一過程稱為凝結。開始,蒸發過程占優勢,但隨著水蒸氣密度的增加,凝結的速率增大,當蒸發速率與凝結速率相等時,氣相和液相達到平衡,此時,氣相蒸氣的密度不再改變,它所具有的壓力稱為該溫度下的飽和蒸氣壓,簡稱蒸氣壓。
影響因素
蒸氣壓與物質的本性和溫度有關。不同的物質蒸氣壓不同,如在293 K時,水的蒸氣壓為2.34 kPa,而乙醚的蒸氣壓為57.6 kPa;同一種物質,溫度不同,蒸氣壓也不同,一般隨溫度升髙而增大。
固體蒸氣壓
定義
當固體升華速率與凝華速率相等時,氣相和固相達到平衡,此時,氣相蒸氣的密度不再改變,它所具有的壓力稱為該溫度下的飽和蒸氣壓,簡稱蒸氣壓,用符號p表示,單位是Pa或kPa。
影響因素
一般固體的蒸氣壓都很小,但冰、碘、樟腦、萘等的蒸氣壓較大。固體的蒸氣壓也隨溫度升髙而增大。

