硼氫化錳是一種無機化合物,又稱硼氫化亞錳或四氫硼酸錳(II),由硼氫化鈉和氯化錳(II)反應得到。硼氫化錳可以用作儲氫材料,也能用於科學研究,如探究其物理、化學性質及配位化合物的結構。
基本介紹
- 中文名:硼氫化錳
- 外文名:Manganese(II) Borohydride
- 化學式:Mn(BH4)2
- 式量:84.62
- 危險性:強還原劑、可燃
歷史,物理性質,化學性質,配合物,用途,儲存,
歷史
2009年,Rodovan Cerný用球磨法製備出硼氫化錳(II):
所用原料的硼氫化物純度為95%,氯化錳的純度為99.999%(5N)。
物理性質
硼氫化錳的原子組成分析如下:
化學性質
硼氫化錳受熱按下式分解:
- Mn(BH4)2 → Mn + 2 B + 4 H2
該反應為放熱反應。
硼氫化錳可以和鹽酸反應。
配合物
硼氫化錳也能形成較簡單的配合物,如KMn(BH4)3、K2Mn(BH4)4和K3Mn(BH4)5等。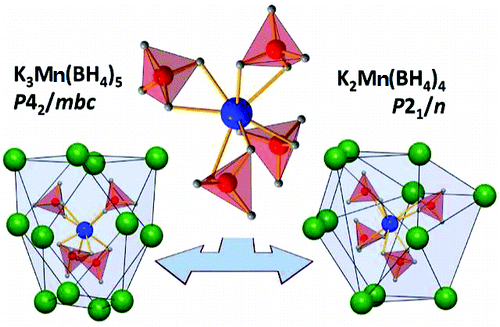 硼氫化錳簡單配合物結構圖
硼氫化錳簡單配合物結構圖
 硼氫化錳簡單配合物結構圖
硼氫化錳簡單配合物結構圖用途
硼氫化錳是有潛力的儲氫材料。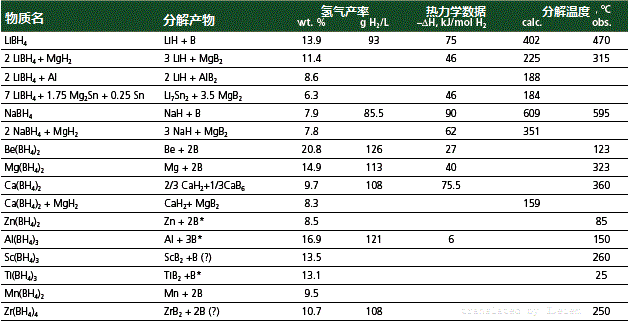 硼氫化物釋放氫氣的能力
硼氫化物釋放氫氣的能力
 硼氫化物釋放氫氣的能力
硼氫化物釋放氫氣的能力相關硼氫化物放出氫氣的能力如右圖。
儲存
避光、密封儲存,遠離酸類和氧化劑。