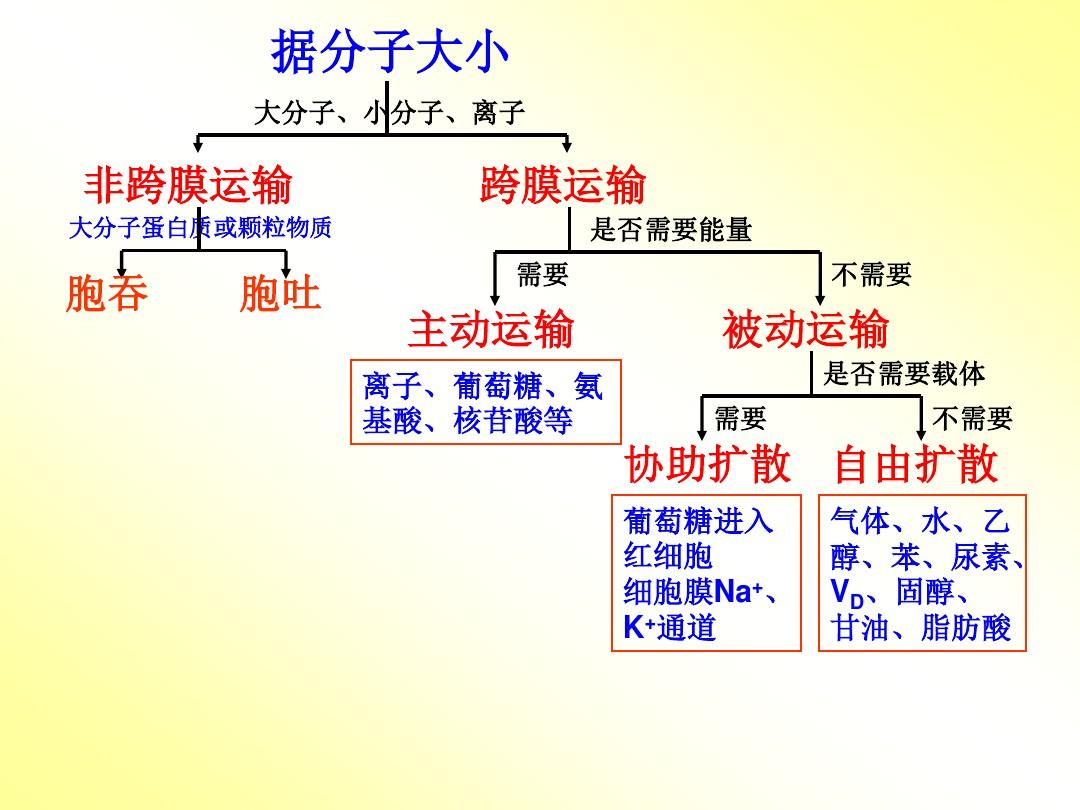
主動運輸
主動運輸(activetransport)是通過消耗能量,膜運輸蛋白由低濃度側向高濃度側逆濃度梯度轉運離子或分子的運輸方式。根據能量利用方式的不同,主動運輸分為ATP驅動泵運輸和協同運輸兩種類型。
ATP驅動泵
ATP驅動的跨膜轉運蛋白即ATP驅動泵,具有催化ATP水解的酶活性,可利用ATP水解釋放的能量逆濃度梯度跨膜轉運離子或分子,共有四種類型,即P類、V類, F類和ABC超家族類。P類、V類及F類都與離子轉運有關。Na
+-K
+ 泵和Ca
2+泵屬於P類轉運蛋白,此類轉運蛋白的胞內α亞基可結合併催化ATP水解,使自身發生磷酸化。F類和V類轉運蛋白負責轉運質子,也稱為H泵。F類轉運蛋白主要存在於細菌的質膜和真核細胞線粒體內膜上,負責將H
+運入線粒體,供ATP合成,也稱為ATP合酶。V類轉運蛋白負責將過多的H
+泵出細胞,以維持細胞內pH值的穩定。ABC超家族轉運蛋白主要介導糖類、脂類、胺基酸、無機酸分子,肽類如谷胱甘肽銜生物以及生物體內的次生代謝物和外來毒索的運輸。
 鈉鉀泵
鈉鉀泵Na+-K+泵
是運輸Na+和K+離子的跨膜運輸蛋白,因具有ATP酶活性,故又稱Na+-K*ATP酶。Na+-K+泵由α、 β兩個亞單位組成,胞質面有3個Na+和1個ATP結合位點,胞外表面有2個K+結合位點和烏本苷(Na+-K+泵的抑制劑)結合位點。Na+-K+泵每秒可水解1000個ATP分子,每水解1個ATP分子向胞外運出3個Na+,向胞內運進2個K+。
 Na+-K+ 泵的工作原理
Na+-K+ 泵的工作原理Na+-K+泵的工作原理是:當Mg2+存在時,胞質中的Na+與此酶的Na+離子位點結合,酶的α亞基被激活,消耗ATP發生酶的自身磷酸化,同時ATP水解為ADP;自身磷酸化後酶構象改變,將Na+轉運到胞外,此時Na+與變構的α亞基親和力降低,從酶上釋放,處於該構象的酶與膜外側K+親和力高,結合K+離子後,刺激酶去磷酸化並恢復原構象,將K+離子轉運到胞內並釋放,完成一次運輸。
細胞消耗大量的ATP來維持細胞內外Na+、 K+離子梯度差,具有重要的生理意義,如調節細胞滲透壓、維持膜電位,驅動某些營養物質的主動吸收(如葡萄糖的轉運)等。氰化物等有毒物質可使ATP供能中斷,造成Na+-K+泵的工作停止。
Ca泵
又稱鈣ATP酶,是運輸Ca2+離子的跨膜運輸蛋白,存在於細胞膜或某些細胞器膜上,具有ATP酶活性,可發生磷酸化與去磷酸化反應,將Ca2+逆濃度泵出細胞或泵入某些細胞器,維持細胞內Ca2+的低濃度水平(≤10-7mol/L),此濃度是細胞外液(約10-3mol/L)的萬分之一。如同Na+-K+泵的工作原理一樣,Ca2+泵每水解一個ATP分子,通過自身構象變化,將胞質中2個Ca2+逆濃度轉運到細胞外或泵入肌質網,通過細胞內Ca2+濃度的變化調節細胞運動、肌細胞收縮、細胞分泌. 神經遞質的釋放及細胞信號轉導等。
除Na+-K+泵,Ca2+泵外,體內還有兩種重要的離子泵,一種是位於胃腺壁細胞膜和腎小管細胞膜上的H+-K+ATP酶,主要功能是分泌H+,另一種是分布在細胞器膜上的H+-ATP酶,可將H+由胞質泵入容酶體、胞內體及突觸囊泡等結構內,維持細胞器內特定的pH值。
ATP供能的ABC超家族轉運
ABC (ATP-binding cassette)轉運蛋白由兩個跨摸結構域和兩個ATP結合域組成,當ATP結合域與ATP結合後,兩個ATP結合域發生二聚化,伴隨著ATP水解成ADP,二聚體解離。ABC轉運蛋白的工作原理是:胞內疏水性底物分子首先轉移到質膜內側,進入質膜內葉,繼而底物分子側向擴散至ABC轉運蛋白並與之結合,ABC轉運蛋白將底物分子轉運到質膜內葉,脫離膜脂游離到細胞外,完成物質的轉運。ABC轉運蛋白是一個超家族,已在哺乳類細胞鑑定其家族成員有近50種,在參與藥物代謝,物質吸收和代謝廢物排泄的肝臟、小腸及腎等組織細胞廣“泛存在,主要是介導生物體內的次生代謝物的運輸。
多藥耐藥性(multidrug resistance,MDR)是腫瘤細胞在某種抗腫瘤藥物作用下出現耐藥性,並對其他多種結構和作用機制不同的抗腫瘤藥物也產生交叉耐藥性。MDR蛋白是ABC家族中的一員,負責將細胞中親脂性小分子物貢轉運出細胞。臨床上使用的抗腫瘤藥物多為脂溶性小分子,當癌細胞中MDR蛋白高表達時,MDR蛋白會將進入細胞的親脂性抗癌藥物轉運出胞,使抗癌藥物失去殺傷癌細胞的作用,故此產生多藥耐藥性。
協同運輸
協同運輸(co-transport)是指一種物質順濃度梯度的被動運輸驅動了另一種物質逆濃度梯度進行主動運輸的過程。如果兩種物質運輸方向相同,稱為同向運輸,如果方向相反,稱為對向運輸。動物細胞的協同運輸通常是由膜兩則的Na
+電化學梯度來驅動,植物細胞和細菌通常是由H
+電化學梯度來驅動。
同向運輸
是兩種溶質分子向同一方向的穿膜運輸。在這種方式中,物質逆濃度梯度穿膜運輸方向與其所依賴的離子順濃度梯度的穿膜運輸方向相同。小腸上皮細胞吸收葡萄糖的過程就是與Na
+的同向協同運輸。在小腸上皮細胞內,葡萄糖濃度比腸腔高,儘管如此,腸腔內的葡萄糖仍逆濃度不斷運輸進人小腸上皮細胞內。葡街糖逆濃度轉運的動力來自小腸上皮細胞內外的Na
+離子的勢能:Na
+-K
+ATP 酶不斷地向細胞外“泵”Na
+,結果是細胞外高濃度的Na
+順電勢差通過小腸上皮細胞頂面的Na
+載體蛋白再被動回流到小腸上皮細胞內,但Na
+載體蛋白結合Na
+的同時與葡萄糖偶聯,順勢將葡萄糖攜帶到胞內。在胞內Na
+釋放後,Na
+載體蛋白構象變化,失去與葡萄糖分子的親和力而與之分離,葡萄糖釋放到細胞內。 在小腸上皮細胞的基底面,葡萄糖由其特定的載體蛋白再經易化擴散轉運至血液。Na
+與葡萄糖的同向運輸保證了葡萄糖吸收和運輸的方向性。
 葡萄糖與Na+的協同運輸
葡萄糖與Na+的協同運輸對向運輸
是在離子濃度梯度驅動下,由同一種載體蛋白將兩種不同的離子或分子分別向膜的相反方向轉運的穿膜運輸過程。高等動物的細胞都有一種或多種對向運輸載體,如Na+-H+交換載體(Na+-H+exchange carrier),它可以通過Na+順濃度梯度內流把H+泵出細胞,從而清除細胞代謝產生的過量H+,細胞內pH維持在7.2左右。
被動運輸
被動運輸(passive transport)是物質順濃度梯度且不消耗細胞代謝能(ATP)所進行的運輸方式,運輸動力來自質膜內、外側物質的濃度梯度勢能或電位差。被動運輸分為簡單擴散和易化擴散。
簡單擴散
簡單擴散(simple diffusion)是脂溶性小分子物質穿膜運輸的方式,被運輸的小分子物質在膜兩側存在濃度差,即可順濃度進行擴散。小分子物質擴散的速度取決於分子的大小和其脂溶性,如疏水性氣體小分子O
2、CO
2、N
2,等能迅速通過細胞膜。乙醇等脂溶性高的小分子也能迅速通過細胞膜。H2O、尿素、甘油等分子帶有強極性,脂溶解度低,故通過膜比較緩慢。更大的親水性分子如葡物糖和各種帶電的分子如胺基酸及核苷酸等都不能經簡單擴散的方式進行運輸。
易化擴散
易化擴散(facilitated diffusion)又稱協助擴散,是藉助於膜上運輸蛋白的協助順濃度梯度運輸物質的方式。葡萄糖、胺基酸,核苷酸等親水性營養物質以及Na+,K+,Ca2+等帶電荷的離子都能通過易化擴散進行跨膜運輸。介導易化擴散的運輸蛋白有載體蛋白和通道蛋白,據此,易化擴散又分為載體蛋白介導的易化擴散和通道蛋白介導的易化擴散兩種類型。介導主動運輸的蛋白也稱為載體蛋白。
載體蛋白介導的易化擴散
運輸過程是通過載體蛋白發生可逆的構象變化實現的。載體蛋白是膜上與物質運輸有關的穿膜蛋白,對所運輸的物質具有高度選擇性,當載體蛋白一端表面的特異結合部位與專一的溶質分子結合,引發載體蛋白空間構象改變,將運送的溶質分子從結合的一側轉運到膜的另一側;變構的載體蛋白對被轉運物質的親和力同時發生改變,於是被轉運的溶質分子與載體蛋白分離而被釋放,載體蛋白又恢復到原來的構象。載體蛋白通過周而復始的構象變化被反覆循環使用。
易化擴散的速率取決於膜兩則溶質分子的濃度差。隨著濃度差增大,運輸速度加快,但當溶質分子與載體蛋白結合的位點飽和時,運輸速率達到飽和,不會再增大。載體蛋白的活性可被調節,其中激索起主要調節作用。
大多數哺乳類動物細胞膜上都含有協助葡萄糖從血液擴散到細胞內的葡萄糖轉運蛋白(glucose transporter, GLUT), 以易化擴散方式將能萄糖轉運人細胞,如人紅細胞膜上約有5萬個葡萄糖轉運蛋白,其數量相當於膜蛋白質總量的5%,最大轉運速度約為每秒轉運180個葡萄糖分子。葡萄糖轉運蛋白家族包括GLUT1-GLUT14,均參與葡萄糖的運輸。GLUT1分布於多種細胞的質膜上,對葡萄糖親和力高,易於葡萄糖吸收進人細胞。GLUT2 主要分布在肝細胞、胰島β細胞(嚙齒類)及小腸和腎具吸收功能的上皮細胞,與葡萄糖的結合具有高泡和度和低親和性特點。GLUT3分布於腦內神經元細胞,對葡筍糖有很高的親和力和運輸容量,即使在血糖水平略低時也能迅速從細胞外液轉運葡萄糖,保障神經元的能量供應。GLUT4分布於肌細胞和脂肪細胞膜上,胰島索可調節GLUT4的數量。正常情況下,靶細胞的GLUT4以囊泡形式貯存在細胞內,當餐後血糖升高時,刺激胰島細胞分泌胰島索,胰島素刺激靶細胞,使含GLUT4的胞內囊泡迅速移至細胞表面,GLUT4 插入質膜中,以提高葡萄糖的攝取,保證血糖的穩定。相反,當機體處於飢餓狀態時,血糖濃度降低,在胰高血糖素作用下,肝糖原降解,產生大量葡萄糖,細胞內葡萄糖糖濃度高於細胞外,葡萄糖結合到載體蛋白細胞內側的結合部位上,將葡筍唐運到細胞外。糖尿病病人常伴有GLUT4數量不足或功能下降,血糖升高時,葡萄糖不能順利進人靶細胞,導致血糖持續增高,是產生胰島索抵抗的原因之一。
通道蛋白介導的易化擴散
運輸過程藉助於穿越脂雙分子層的通道蛋白完成。通道蛋白中心是親水性小孔,不同種類的通道蛋白可分別運輸離子,水等小分子。主要運輸離子的通道蛋白也稱為離子通道,對離子具有高度親和力和高度選擇性。離子通道運輸速率高,每秒運輸離子數量多達幾百萬個,載體蛋白每秒運載的分子數目則不足一千個。某些離子通道蛋白星關閉狀態,在接受特定信號刺激時發生構象的變化而開啟,開放時間不超過幾毫秒,隨即關閉,相當於閘門,也稱為閘門離子通道。
根據閘門離子通道開啟信號的不同分為3類。第一類是電壓門通道,通道的開、閉受膜電位變化控制,如Na+通道、K+通道等。第二類是配體門通道,通道的開、閉受化學物質調節,研究較深入的是乙醯膽鹼受體通道。第三類是應力激活通道,通道蛋白感受機械應力而改變構象,開啟通道。如內耳聽覺毛細胞頂部的聽毛就具有這種通道,聲波刺激在耳蝸內轉換成機械振動,可引起聽毛傾斜,牽動聽毛上應力活化的K+通道,K+流人內耳毛細胞,使毛細胞發生去極化,產生聽覺信號。
閘門離子通道的瞬時開關有利於細胞各種功能活動依次進行。神經衝動引起骨骼肌收縮的整個反應過程至少有4種閘門離子通道被依次激活,順序開放和關閉。
①當衝動到達神經末梢,神經細胞膜發生去極化,膜電位降低,引起神經末梢膜上的電壓閘門Ca2+通道開放,膜外高濃度的Ca2+迅速進人神經末梢,刺激分泌神經遞質——乙醯膽鹼。
②釋放的乙醯膽鹼與肌肉細胞膜上的配體閘門通道上的特異部位結合,閘門瞬間開放,Na+大量進入細胞,引起肌細胞膜電位改變,膜局部去極化。
③肌肉細胞膜的局部去極化又使其膜上的電壓閘門Na+通道開放,更多的Na+進入肌細胞,去極化擴展到整個肌細胞膜。
④肌細胞膜去極化又引起肌細胞內肌質網上的Ca2+通道開放,從肌質網內流人細胞質,肌細胞內Ca2+濃度急劇升高,引發肌原纖維收縮。
胞吞胞吐
大分子和顆粒物質通過細胞膜包圍形成囊泡,通過囊泡的形成和融合來完成運輸過程,故被稱作小泡運輸(vesicular transport),又稱批量運輸(bulk transport),包括
胞吞作用和
胞吐作用。
胞吞作用
細胞質膜內陷將外來的大分子或顆粒物質包圍形成小囊泡並轉運到細胞內的過程稱為胞吞作用(endocytosis)。根據胞吞作用對向的大小、狀態機特異性,將其分為三大類:吞噬作用、胞飲作用及受體介導的胞吞作用。
吞噬作用
吞噬作用主要是指某些特定的免疫相關細胞捕獲較大的顆粒物質或大分子物質時,細胞膜凹陷,將顆粒包裹後,轉運到細胞內,吞噬過程中細胞膜形成的小泡稱為吞噬體(phago-some)或吞噬泡(phagocytic vesicle)。中性粒細胞、單核細胞及巨噬細胞等都具有吞噬功能,對顆粒物質的吞入是由質膜下微絲和結合蛋白的介導。這幾種細胞廣泛分布於動物體內,對入侵機體的病毒和細菌等微生物具有清除作用,對機體自身的代謝物如衰老死亡的細胞也具有清除作用。
胞飲作用
當胞吞作用吞人的物質為液體時,稱為胞飲作用(pinocytosis)。當胞外的溶質達到一定濃度時,可通過胞飲作用被攝人細胞內,這個過程中所形成的小囊泡的直徑小於150 nm,小囊的形成受格線蛋白及結合素蛋白的介導。根據細胞外物質是否吸附在細胞表面,將胞飲作用分為兩種類型。一種是液相內吞(fluid-phase endocytosis),這是一種非特異性的固有內吞作用,通過這種內吞作用,細胞把細胞外液及其中的可溶物吞入細胞內。另一種是吸附內吞(ab-sorption endocytosis),細胞外大分子或小顆粒物質先以某種方式吸附在細胞表面,因此具有一定的特異性。如小腸上皮細胞、血管內皮細胞等具有吞飲作用。
受體介導的胞吞作用
通過與細胞膜表面特定受體結合,攝取細胞外蛋白、多糖或其他化合物的過程,稱為受體介導的胞吞作用(receptor-mediated endocytosis)。因此,這種吞飲作用對攝入小泡的物質具有選擇性,因此攝入的特異性強,效率更高。動物細胞對許多重要物質的吸收都是通過受體介導的胞吞作用來完成,包括多種蛋白質、生長因子、鐵及維生素B12等。如動物細胞對卵黃蛋白的攝入過程,需要卵黃蛋白首先結合到細胞表面的受體,然後質膜凹陷將形成的卵黃蛋白及受體複合物包裹,形成小泡,隨後小泡脫離細胞膜進入胞質,完成吞飲作用。此外,動物細胞通過受體介導的胞吞作用獲取所需的大部分膽固醇。
胞吐作用
將細胞內的分泌泡或其他膜泡中的物質通過質膜運輸到細胞外的過程稱為胞吐作用( ex-ocytosis),是指大分子或顆粒狀物質由細胞內排到細胞外的過程,分為連續性分泌和調節型分泌兩種。連續性分泌( constitutive secretion)又稱固有分泌,存在於所有真核細胞中,指分泌蛋白在內質網合成後,轉運到高爾基複合體,並在此形成分泌泡,分泌泡與質膜融合,將分泌物排出細胞外。分泌的物質主要用於質膜的更新,包括膜脂、膜蛋白、胞外基質、營養及信號分子等。調節型分泌( regulated secretion)主要存在於特化的分泌細胞,分泌的蛋白合成之後被儲存在分泌囊泡中,只有當細胞受到相應胞外刺激信號後,才啟動胞吐過程。這種分泌方式只存在於分泌激素、酶、神經遞質的細胞內,如血糖升高后,細胞會發出信號釋放胰島素,從而降低血糖。
 鈉鉀泵
鈉鉀泵 Na+-K+ 泵的工作原理
Na+-K+ 泵的工作原理 葡萄糖與Na+的協同運輸
葡萄糖與Na+的協同運輸