氯化浸出(chloridizing leaching)用各種氯化劑作浸出劑使目的組分呈可溶性金屬氯化物形態轉入浸出液中的礦物浸出工藝。常用的氯化浸出劑為鹽酸、氯鹽和氯氣等。
基本介紹
- 中文名:氯化浸出
- 外文名:chloridizing leaching
- 常用試劑:鹽酸、氯鹽和氯氣等
- 學科:濕法冶金
基本概念
發展歷程
特點
分類
鹽酸浸出
工藝介紹
典型案例
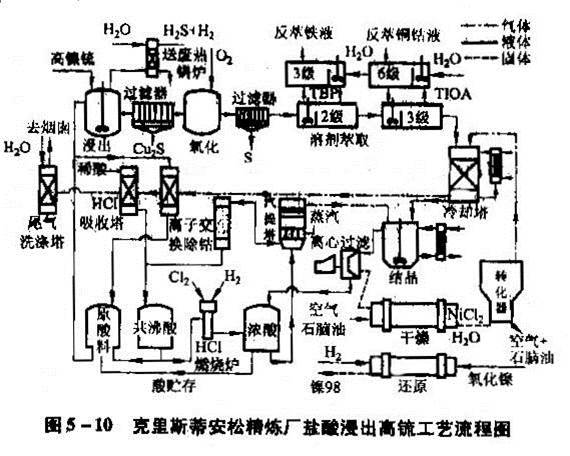
液氯浸出
工藝介紹
典型案例
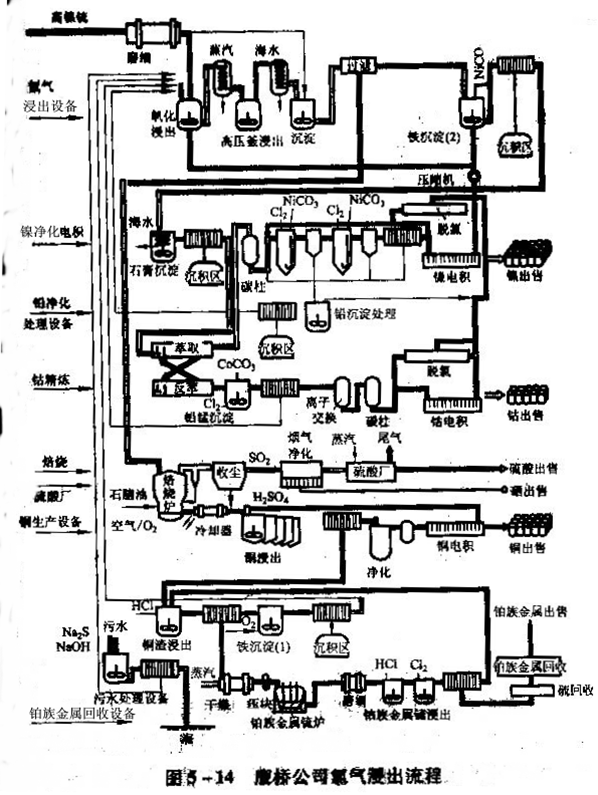
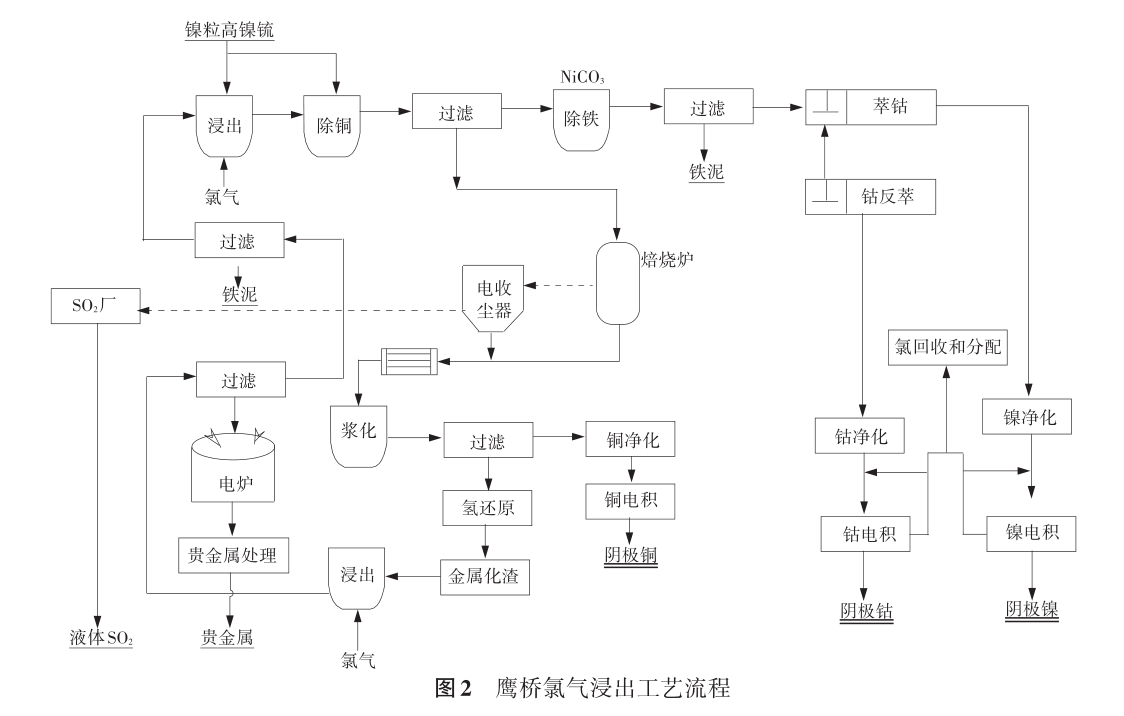
氯化浸出(chloridizing leaching)用各種氯化劑作浸出劑使目的組分呈可溶性金屬氯化物形態轉入浸出液中的礦物浸出工藝。常用的氯化浸出劑為鹽酸、氯鹽和氯氣等。


氯化浸出(chloridizing leaching)用各種氯化劑作浸出劑使目的組分呈可溶性金屬氯化物形態轉入浸出液中的礦物浸出工藝。常用的氯化浸出劑為鹽酸、氯鹽和氯氣等。...
電浸出(electro dissolution,electrolytic leaching)是指利用電解池陽極反應使物料中的有價金屬溶解入溶液的浸出方法。也稱電化學浸出。將物料(可加入石墨粉來提高導電...
氯化焙燒是加熱物料在低於其熔點溫度下使物料中某些組分與氯化劑作用生成氯化物的焙燒方法。被氯化的物料可以是氧化物、碳化物、硫化物以及金屬或合金。...
浸出毒性通常指固體廢物遇水浸瀝,浸出的有害物質遷移轉化,污染環境。浸出毒性包括無機元素及化合物,如鎘、鉛、汞、砷、六價鉻、氰化物等;有機農藥類,如滴滴涕、...
氯化銨法是一種氯化銨法從氟碳鈰精礦提取氯化稀土的方法。氯化銨法是一種氯化銨法從氟碳鈰精礦提取氯化稀土的方法,首先將氟碳鈰原精礦磨細,並與NaCO↓混合,其...
高鎳鋶選擇性浸出法(selective leaching me-thud of high nickel matte)是指用浸出劑選擇性地使高鎳鋶中的鎳、鈷進入溶液而被提取的高鎳鋶處理方法。在浸出過程...
它不易燃,曾作為滅火劑,但因它在500攝氏度以上時可以與水反應,產生二氧化碳和有毒的光氣、氯氣和氯化氫氣體,加之它會加快臭氧層的分解,所以被停用。四氯化碳的...
對於高鎳鋶的處理主要有五種方法:傳統的Hybinette工藝,硫酸加壓浸出工藝,氯化浸出工藝,加壓氨浸工藝及羰基法。傳統的Hybinette精煉工藝成熟可靠,具有操作簡單,生產...
在鈷鎳生產中浸出主要有酸性浸出、氯化浸出、氨浸出以及高壓氧浸等等。主要用到的輔料有濃硫酸、濃鹽酸、氯氣,二氧化硫、氨水、空氣、氯酸鈉、雙氧水、二氧化錳、亞...
化學選礦是基於礦物組分的化學性質的差異,利用化學方法改 變礦物的性質,使目標組分或雜質組分選擇性地溶於浸出溶劑中,從而達到分離 的目的。...
